德国化学家哈伯因研制合成氨作出重大贡献而获得1918年诺贝尔化学奖,如今可以用电化学的方法合成氨,装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )
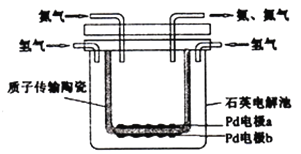
A. Pd电极b为阴极 B. 阴极的反应式为:N2+6H++6e-=2NH3
C. H+由阳极向阴极迁移 D. 陶瓷可以隔离N2和H2
高三化学单选题中等难度题
德国化学家哈伯因研制合成氨作出重大贡献而获得1918年诺贝尔化学奖,如今可以用电化学的方法合成氨,装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )

A. Pd电极b为阴极 B. 阴极的反应式为:N2+6H++6e-=2NH3
C. H+由阳极向阴极迁移 D. 陶瓷可以隔离N2和H2
高三化学单选题中等难度题
德国化学家哈伯因研制合成氨作出重大贡献而获得1918年诺贝尔化学奖,如今可以用电化学的方法合成氨,装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )

A. Pd电极b为阴极 B. 阴极的反应式为:N2+6H++6e-=2NH3
C. H+由阳极向阴极迁移 D. 陶瓷可以隔离N2和H2
高三化学单选题中等难度题查看答案及解析
二十世纪初德国化学家哈伯和工程师博施成功地开发了合成氨的生产工艺,为社会的发展和进步做出了重大贡献。如今科学家为提高氨的产量,以及对各种氨的化合物的研究仍做着各种有益的探索。试回答下列问题:
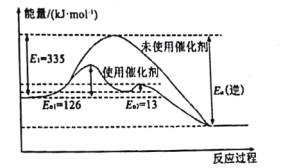
(1)N2(g)+3H2(g)2NH3(g) △H =-92.4kJ·mol-1如图所示,合成氨反应中未使用催化剂时,逆反应的活化能Ea(逆)=___kJ·mol-1。
(2)①在一定条件下,分别将lmolN2和3molH2置于容积恒定的密闭容器中,达化学平衡状态时,NH3的体积分数为10%,若保持其他条件不变,起始时改为充入2molN2和2molH2,达新平衡后,NH3的体积分数为___10%(填“>”、“<”或“=”)。
②某温度下,n(N2):n(H2)=1:3的混合气体在刚性容器内发生反应,起始时气体总压为p0Pa,平衡时气体总压为0.9p0Pa,气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学反应平衡常数(记作Kp),则此温度下,该反应的化学平衡常数Kp=___(用含p0的代数式表示)。
(3)合成氨需要的H2来源比较广泛,氢气的储存制备等问题也日益得到解决。在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)MHx+2y(s)△H<0达到化学平衡。下列有关叙述正确的是(______)
a.容器内气体压强保持不变
b.吸收ymolH2需1molMHx
c.若向容器内通入少量氢气,新平衡后c(H2)比原平衡大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用现代手持技术传感器可以探究压强对化学平衡移动的影响,如以2NO2(g)N2O4(g)为例。在恒定温度和标准压强(100kPa)条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞后并保持活塞位置不变(不考虑温度的变化)。测定针筒内气体压强变化如图所示:
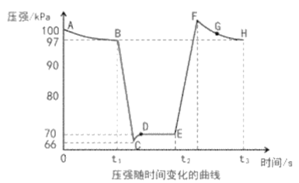
①B、E两点对应的正反应速率大小为vB___vE(填“>”、“<”或“=”)。
②E、F、G、H四点时对应气体的平均相对分子质量最大的点为___。
(5)NH3能够和Ag+形成Ag(NH3)2+,溶液中存在Ag+(aq)+2NH3(aq)Ag(NH3)2+(aq)常温下,K[Ag(NH3)2+]=1.10×107,反应AgCl(s)+2NH3(aq)
Ag(NH3)2(aq)++Cl-(aq)的化学平衡常数K=1.936×10-3,则Ksp(AgCl)=___。
高三化学综合题困难题查看答案及解析
德国人弗里茨•哈伯(Fritz Haber)由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量.下列说法中正确的是( )
A.N2和H2在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.由氨制取硝酸过程中,氮元素被还原
高三化学选择题中等难度题查看答案及解析
1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖。氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途。
Ⅰ.以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(g) ΔH = a kJ/mol。
为研究平衡时CO2的转化率与反应物投料比()及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应,并绘出下图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。

(1)a 0 (填“>”或“<”),判断依据是__________________。
(2)①投料比:Ⅰ Ⅱ(填“>”或“<”)。
②若n(CO2)起始 =10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为_________________。
③A点平衡常数与B点平衡常数间的关系:KA KB (填“>”或“<”或“=”)。B点正反应速率与C点正反应速率间的关系为:v (B)_________v (C) (填“>”或“<”或“=”)。
(3)若按曲线Ⅰ的投料比投料,在上述实验中压缩容器体积至5L,在上图中画出反应达平衡时的二氧化碳的转化率与温度之间的关系曲线。
(4)为提高CO2转化率可以采取的措施是 。
a.使用催化剂
b.及时从体系中分离出部分CO(NH2)2
c.将体系中的水蒸气液化分离
Ⅱ.氨气可用于工业上生产硝酸,其尾气中的NO2可用氨水吸收生成硝酸铵,25℃时,将10molNH4NO3溶于水,溶液显酸性,向该溶液中滴加1L某浓度的氨水,溶液呈中性,则滴加氨水的过程中水的电离平衡将_________(填“正向”、“逆向”或“不”) 移动, 此中性溶液中NH3·H2O的物质的量为________mol。(25℃时,NH3·H2O的电离平衡常数Kb=2×10-5)
高三化学填空题简单题查看答案及解析
德国化学家哈伯(F.Haber)从1902年开始研究由氮气和氢气直接合成氨。合成氨为解决世界的粮食问题作出了重要贡献。其原理为N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ/mol
(1)若已知H-H键的键能为436.0kJ/mol,N-H的键能为390.8kJ/mol,则NN的键能约为_____kJ/mol
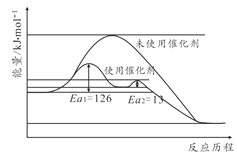
(2)合成氨反应不加催化剂很难发生,催化剂铁触媒加入后参与了反应降低了活化能。其能量原理如图所示,则加了催化剂后整个反应的速率由______决定(填“第一步反应”或者“第二步反应”),未使用催化剂时逆反应活化能______正反应活化能(填“大于”“小于”或者“等于”)
(3)从平衡和速率角度考虑,工业生产采取20MPa到50MPa的高压合成氨原因______
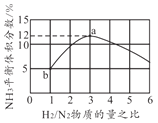
(4)一定温度下恒容容器中,以不同的H2和N2物质的量之比加入,平衡时NH3体积分数如图所示,则H2转化率a点______b点(填"大于”“小于”或者“等于”)。若起始压强为20MPa,则b点时体系的总压强约为______MPa。
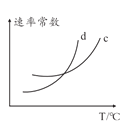
(5)若该反应的正逆反应速率分别表示为v正=K正,v逆=K逆∙c2(NH3),则一定温度下,该反应 的平衡常数K=______(用含K正和K逆的表达式表示),若K正和K逆都是温度的函数,且随温度升高而升高,则图中c和d分别表示______和______随温度变化趋势(填K正或者K逆)。
(6)常温下,向20mL的0.1mol/L的盐酸中通入一定量氨气反应后溶液呈中性(假设溶液体积变化忽略不计)则所得溶液中c(NH4+)=_______
高三化学综合题困难题查看答案及解析
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,有关说法正确的是 ( )
A、达到化学平衡时,N2将完全转化为NH3
B、达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C、达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应的速率都为零
高三化学选择题简单题查看答案及解析
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
(10分)哈伯因发明了氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,。右图表示某温度时,向1L容器中加入1mol氮气,3mol氢气,该反应在110S内反应进行的程度:
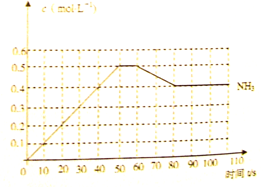
(1)此反应在50~60s时化学平衡常数为=________(列出计算式不用试算)。
(2)反应进行到60s时,改变的条件可能是________。
A.加入催化剂 B.扩大容器的体积
C.升高温度 D.减小氨气的浓度
在该条件下,氮气的化学反应速率________(填“变小”、“变大”或“不变”)
(3)该反应在80S后化学平衡常数为,则
________
(填“>”,“<”或“=”),此时氮气的转化率为________。
(4)若在110s后向该平衡体系中再加入1mol氨气,则再次达平衡后,氨气在平衡体系中的体积分数________。(填“变小”、“变大”或“不变”)
高三化学填空题简单题查看答案及解析
哈伯因发明了用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是
A.达到化学平衡时,N2完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应速率都为零
高三化学单选题中等难度题查看答案及解析