-
(8分)
(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为___________________
(2)写出工业上制取漂白粉的化学反应方程式:_________________
(3)写出氯气实验室制法方程式:_____________________
(4)ClO2被称为“第四代”饮用水消毒剂,因其高效率、无污染而被广泛使用。北京永利科技有限公司已用电解法批量生产ClO2。其反应原理为4ClO-+4H+ 4ClO2↑+O2↑+2H2O,相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是______________
4ClO2↑+O2↑+2H2O,相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是______________
-
氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺(NH2Cl)、二氯胺(NHCl2)和三氯胺(NC13) 。氯胺消毒时首先发生水解,生成具有强烈杀菌作用的次氯酸。
(2) NH2Cl中氯元素的化合价为_______,其电子式为________。
(2) NH2Cl水解的离子方程式为____________。
(3)三氯胺在常温下为黄色黏稠的油状液体,有毒,在弱酸性溶液中稳定性较好。将0.01mol NCl3通入100mL0.5mol/LNa2SO3溶液中,转移电子的物质的量为___________。
(4)已知:
2NH3(g)+ 3Cl2(g)=N2(g)+ 6HCl(g) △H1=-469kJ·mol-1
N2(g)+ 3Cl2(g)=2NC13(g) △H2=+520kJ·mol-1
NH3(g)+3Cl2(g)=NC13(g)+3HCl(g) △H3
则△H3=_________ kJ·mol-1。
-
氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺(NH2Cl)、二氯胺(NHCl2)和三氯胺(NCl3)。氯胺消毒时首先发生水解,生成具有强烈杀菌作用的次氯酸。
(1)NH2Cl中氯元素的化合价为___________,其电子式为__________。
(2)NH2Cl水解的离子方程式为____________。
(3)三氯胺在常温下为黄色黏稠的油状液体,有毒,在弱酸性溶液中稳定性较好。将0.01 mol NCl3通入100mL0.5mol/LNa2S03溶液中,转移电子的物质的量为___________。
(4)己知:2NH3(g)+3C12(g)=N2(g)+6HCl(g)△H1=-469kJ/mol
N2(g)+3C12(g)=2NC13(g) △H2=+520kJ/mol
NH3(g)+3C12(g)= NC13(g)+ 3HCl(g)△H3
则△H3=__________kJ/mol
-
(15分)水是生命之源。饮用水消毒剂作为控制水质的一个重要环节,令世人关注。
⑴液氯消毒是最早的饮用水消毒方法。氯气溶于水能杀菌消毒的原因是:
________。近年来科学家提出,氯气能与水中的有机物发生反应,生成的有机氯化物可能对人体有害。
臭氧(O3)是优良的水消毒剂。但当水中含溴离子(Br-)时,臭氧可氧化溴离子(Br-)为溴酸盐 (BrO- 3)。而溴酸盐 (BrO- 3)是对人体有致癌作用的化合物,我国规定饮用水中BrO- 3含量在10μg / L以下。测定BrO- 3浓度可用离子色谱法。
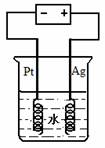
⑵水中的氯离子(Cl-)对BrO-3测定干扰很大,需要先除去氯离子(Cl-)。用右图的装置可除去水中的氯离子(Cl-)。
装置中Ag是________极(填电极名称),
Ag电极的电极反应式是________。
⑶ O3氧化溴离子的原理如下:

已知HBrO是一种弱酸,O3与HBrO反应很慢,BrO- 3主要是由BrO-与O3反应生成。
对影响生成BrO- 3速率的因素提出如下假设:(请你完成假设②和假设③)
假设①:反应的温度。
假设②:
假设③:________
⑷设计实验验证假设①。
验证实验操作:
a. 配制250 mL 50 mg / L KBr溶液,加入 15 mL 某种pH=7的缓冲溶液(维持溶液的pH基本不变),并将溶液分为2份。
b. ________
实验中要测定的量是
实验结论是________
-
氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl、NHCl2和NCl3)。
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质的结构式为________,二氯胺与水反应的化学方程式为_____________。将0.01 mol NCl3通入100 mL 0.5 mol/L Na2SO3溶液中,转移电子的物质的量为_______mol。
(2)已知部分化学键的键能和化学反应的能量变化如下表和下图所示。
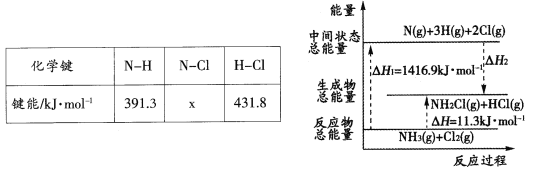
则反应过程中的△H2=____kJ·mol-1,表中的x=_____。
(3)在密闭容器中反应NH3(g)+Cl2(g) NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随 的变化如下图所示。
的变化如下图所示。
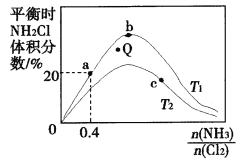
①a、b、c三点对应平衡常数的大小关系是(分别用Ka、Kb、Kc表示)_________。b点时,该反应的平衡常数为________;
②T2℃,Q点对应的速率: __________
__________ (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
③在氨氯比一定时,提高NH3的转化率的方法是__________(任写1种);
④若产物都是气体,实验测得NH2C1的体积分数始终比理论值低,原因可能是______________。
-
某校化学研究性学习小组对氯气的性质和用途进行了调查分析,了解了氯气能应用 于衣物漂白、水体的杀菌和消毒的原理。
(1) 氯气溶于水可用于漂白、消毒的原因是_______,反应的离子方程式为_______ ;
(2) 通常使用漂白液(NaClO溶液)作漂白剂而不用氯气的理由是_____(写出一项即可);
(3) 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应 (发生的反应均为放热反应)。最终生成物中含有Cl-、 ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离 子的物质的量(n)与反应时间(t)的变化曲线如下图所示。
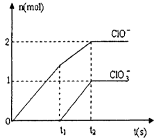
①O-t1时间内,Ca(OH)2与Cl2发生反应的化学方程式为_______;
②t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为_______
③该石灰乳中含有Ca(OH)2的质量是_______g;
-
二氧化氯是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂。回答下列问题:
(1)二氧化氯可溶于水,但常温下难以与水反应,加热时会发生反应生成等物质的量的次氯酸和氯气,同时放出氧气,该反应的化学方程式为_______________________,产物之一次氯酸的电子式为_____________。二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠和另一种氯的含氧酸盐,同时生成水,该反应的离子方程式为______________________。
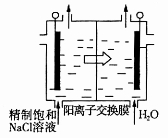
(2)工业上可利用电解法制备二氧化氯,如图为以石墨作电极制备二氧化氯的过程,写出产生二氧化氯气体的电极反应式:____________________。可利用滴定法测定电解过程中产生的二氧化氯,其过程如下:在锥形瓶中加入足量用硫酸酸化的碘化钾溶液,将生成的二氧化氯通入锥形瓶中至完全吸收,再向锥形瓶中滴加几滴淀粉溶液,用0.1 mo1·L‑1硫代硫酸钠标准液进行滴定(I2+2S2O32-==2I-+S4O62-),共用去100.00 mL标准液。则电解过程中产生的气体折算为标准状况下的体积为________mL
-
(1)自来水厂用氯气进行消毒,改善水质,因为氯气与水反应会生成盐酸和次氯(HClO)次氯酸具有杀菌消毒作用,其反应方程式为__________________________________;
(2)氯气与氢氧化钙溶液反应能制得漂白粉(次氯酸钙与氯化钙的混合物)。试写出反应的化学方式:________。
-
Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒。
(1)电解NaCl溶液生成氯气的化学方程式为 。
(2)Cl2溶于H2O、NaOH溶液即获得氯水、漂白液。
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是 。
②25℃,Cl2与H2O、NaOH的反应如下:
| 反应Ⅰ | Cl2+H2O Cl-+H++HClO K1=4.5×10-4 Cl-+H++HClO K1=4.5×10-4 |
| 反应Ⅱ | Cl2+2OH- Cl-+ClO-+ H2O K2=7.5×1015 Cl-+ClO-+ H2O K2=7.5×1015 |
不直接使用氯水而使用漂白液做消毒剂的原因是 。
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+;ClO发生的电极反应式是 。
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如图所示:
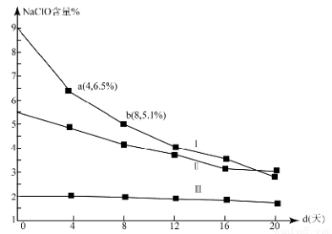
①分解速率v(Ⅰ) v(Ⅱ)(填“>”“<”或“=”),原因是 。
②NaClO分解的化学方程式是 。
③4d-8d,Ⅰ中v(NaClO)= mol/(L·d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
-
[化学—选修2:化学与技术]世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:
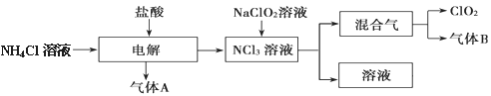
(1) ClO2中所有原子________________(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用____________ 。
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是________ 。
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3) 欧洲国家主要采用氯酸钠氧化浓盐酸制备。化学反应方程式为__________________ 。缺点主要是产率低、产品难以分离,还可能污染环境。
(4) 我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是____________ ,此法相比欧洲方法的优点是__________________________________ 。
(5) 科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为_________________________________________ 。此法提高了生产及储存、运输的安全性,原因是_______________________________________。
4ClO2↑+O2↑+2H2O,相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是______________







