-
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀硫酸中,观察现象如下:
下列有关三种金属的说法正确的是( )
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
A.在地壳中的含量Mg > Ti,说明金属在地壳中的含量越低,活泼性越弱
B.反应中产生H2速率不同的原因是因为c(H+)不同
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.利用电解装置,Cu可以与稀硫酸反应产生H2
高三化学选择题中等难度题查看答案及解析
-
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
金属[
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和稀盐酸不发生化学反应
高三化学选择题中等难度题查看答案及解析
-
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和稀盐酸不发生化学反应
高三化学选择题中等难度题查看答案及解析
-
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀硫酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是( )
A. 在地壳中的含量Mg > Ti,说明金属在地壳中的含量越低,活泼性越弱
B. 反应中产生H2速率不同的原因是因为c(H+)不同
C. 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D. 利用电解装置,Cu可以与稀硫酸反应产生H2
高三化学选择题中等难度题查看答案及解析
-
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和稀盐酸不发生化学反应
高三化学选择题中等难度题查看答案及解析
-
[选做题——物质结构与性质]
金属钛(Ti)是一种具有许多优良性能的的金属,钛和钛合金被认为是21世纪的重要金属材料。
(l) Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
① Ti2+基态的电子排布式可表示为_____________________。
② BH4-的空间构型是______________________(用文字描述)。
③ 与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有__________种。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。
①纳米TiO2催化的一个实例如下图所示。
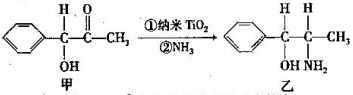
化合物甲的分子中采取
杂化方式的碳原子个数为______________, 化合物乙中采取
杂化的原子的第一电离能由小到大的顺序为________________。
②在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子、离子化学式分别为_________________、_______________(各写一种)。
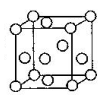
(3)金属钛内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图。若该晶胞的密度为
,阿伏加德罗常数为
,则该晶胞的边长为______________cm。
高三化学填空题简单题查看答案及解析
-
金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____。
②与BH4-互为等电子体的阳离子的化学式为_____。
③H、B、Ti原子的第一电离能由小到大的顺序为_____。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
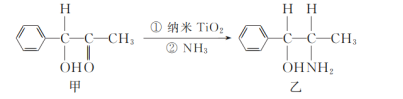
化合物乙的分子中采取sp3杂化方式的原子个数为_____。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____。
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____。

高三化学综合题中等难度题查看答案及解析
-
钛和钛的合金被誉为“21世纪最有发展前景的金属材料”,它们具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工、耐腐蚀等,尤其是钛合金与人体器官具有很好的“生物相容性”。根据它们的主要性能,下列用途不切合实际的是( )
A.用来作保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于家庭装修,作钛合金装饰门
高三化学单选题简单题查看答案及解析
-
铝、铁、铜及其合金具有广泛的应用,某学校化学兴趣小组为探究金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的AlCl3溶液和胆矾晶体(CuSO4·5H2O),其实验方案如下:
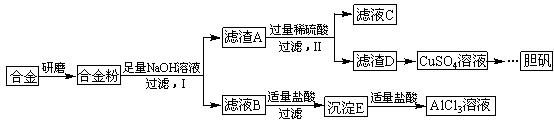
请回答下列问题:
(1)将合金研磨成合金粉的目的是 。
(2)写出步骤I中发生反应的化学方程式: 。
(3)硫酸铜溶液经过“一系列步骤”制得胆矾,此“一系列步骤”依次为 、 和过滤。
(4)在滤液B转化为沉淀E的过程中盐酸的用量不易控制,可将加入适量的盐酸改为通入一种气体,该气体的电子式为 ,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式: 。
(5)该小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣D中加入稀硫酸和H2O2可制得CuSO4,写出该反应的离子方程式: 。
(6)下面两种方法也可以制备硫酸铜:
方法一:2Cu+O2
2CuO,CuO+H2SO4=CuSO4+H2O
方法二:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
假如某工厂欲生产CuSO4,请选择一种方法,并说明理由: 。
高三化学填空题困难题查看答案及解析
-
合金具有很多优良性能,合金的制备常用到许多过渡金属。请问答下列问题:
(1)基态锌原子的电子排布式为________________;金属锌可溶于浓的烧碱溶液生成可溶性的四羟基合锌酸钠Na2[Zn(OH)4]与氢气,该反应的离子方程式为_________;已知四羟基合锌酸离子是对称的立体空间构型,则Zn2+的杂化方式为____________。
(2)铜与类卤素(SCN)2反应可生成Cu(SCN)2,Cu2+与SCN-之间以__________键结合。类卤素(SCN)2对应的酸有两种:A.硫氰酸(H-S-C≡N)和B.异硫氰酸(H-N=C=S),两者互为______________;其中熔点较高的是__________(填代号),原因是______________;组成酸的元素中第一电离能最大的是_________(填元素符号)。
(3)已知硫化锌晶胞如图1所示,则每个晶胞中含_______个硫化锌, Zn2+的配位数是________;
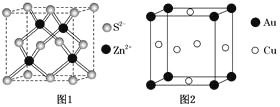
(4)铜与金形成的合金结构如图2所示,其立方晶胞的棱长为a纳米(nm),该合金的密度为____________g/cm3(用含a,NA的代数式表示)。
高三化学综合题中等难度题查看答案及解析