-
加0.1 mol MnO2粉末于50 mL过氧化氢溶液(H2O2,ρ= 1.1 g • mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。
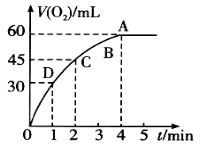
(1) 实验时放出气体的总体积是___________。
(2) 放出一半气体所需时间为____________。
(3) 反应放出 体积的气体所需时间约为___________。
体积的气体所需时间约为___________。
(4) A、B、C、D各点反应速率快慢的顺序为___________。
(5) 解释反应速率变化的原因∶________________________。
(6) 计算H2O2溶液的初始物质的量浓度为__________________。
(7) 计算2min时,用H2O2表示的化学反应速率为__________________。
-
加0.1 mol MnO2粉末于50 mL过氧化氢(H2O2,ρ=1.1 g· mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。
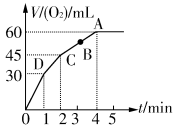
(1)实验时放出气体的总体积是_____________________________。
(2)放出一半气体所需时间为_______________________________。
(3)反应放出气体总体积的 所需的时间约为__________________
所需的时间约为__________________
(4)A、B、C、D各点反应速率快慢的顺序为____________________
(5)解释反应速率变化的原因___________________________________________________
(6)计算H2O2的初始物质的量浓度____________________
(7)求反应到2 min时,H2O2的质量分数_________________________
-
在50 mL过氧化氢溶液中加入1 g MnO2粉末,标准状况下放出气体的体积和时间的关系如图所示,下列说法不正确的是( )
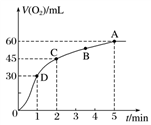
A. 标准状况下,实验放出一半气体所需的时间为1 min
B. A、B、C、 D各点反应速率中A点最慢,D点快
C. 0~2 min内产生O2的平均反应速率为22.5 mL·min-1
D. 本实验中影响反应速率的因素只有催化剂和H2O2的浓度
-
镁铝合金5.1g溶于300mL 2mol/L盐酸中,标准状况下放出气体体积为5.6L,向反应后的溶液中加入500mLNaOH溶液充分反应,最终产生白色沉淀.下列有关说法不正确的是
A.5.1g镁铝合金中含有镁、铝的质量分别为2.4g、2.7g
B.溶解5.1g镁铝合金时,剩余盐酸的物质的量为0.1mol
C.生成白色沉淀的最大质量为13.6g
D.若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2mol/L
-
镁铝合金5.1 g溶于300 mL 2 mol·L-1的盐酸中,在标准状况下放出气体的体积为5.6 L。向反应后的溶液中加入足量氨水,产生沉淀的质量为( )
A.5.1 g B.10.2 g C.13.6 g D.15.3 g
-
镁铝合金5.1 g溶于300mL2mol/L的HCl,在标准状况下放出气体的体积为5.6L。向反应后的溶液中加入足量氨水,产生沉淀的质量为
A.5.1g B.10.2g C.13.6g D.15.3g
-
下列反应中产生气泡速率最快的是
温度 浓度 催化剂
A 25℃ 2mL5%H2O2 0.1mol/LFeCl32滴
B 35℃ 2mL8%H2O2 MnO2粉末
C 25℃ 2mL5%H2O2 MnO2粉末
D 25℃ 2mL8%H2O2 0.1mol/LCuCl22滴
-
NA代表阿伏加德罗常数。下列有关叙述正确的是
A.标准状况下,2.24 L H2O含有的分子数等于0.1 NA
B.常温下,100 mL 1 mol/L Na2CO3溶液中阴离子总数大于0.1 NA
C.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.3.4 g NH3中含N-H键数目为0.2 NA
-
设NA为阿伏加德罗常数的数值。下列说法正确的是( )
A. 标准状况下,4.48LCO2和足量的过氧化钠反应,转移的电子数为0.4NA
B. 在200ml 0.1mol•L-1HCl溶液中加入2.3gNa,最多产生H2分子数为0.01NA
C. 4.6gNa在氧气中完全反应生成Na2O和Na2O2,转移电子数为0.2NA
D. 25℃时,1L pH=14的Ba(OH)2溶液中,Ba2+数目为NA
-
NA代表阿伏加德罗常数,下列有关叙述正确的是
A.标准状况下,2.24 L H2O含有的电子数等于NA
B.常温下,100 mL 1 mol·L-1Na2CO3溶液中阴离子总数大于0.1NA
C.分子数为NA的N2、C2H4混合气体体积约为22.4 L,质量为28 g
D.3.4 g NH3中含N—H键数目为0.2NA

体积的气体所需时间约为___________。

