-
氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如图1所示:
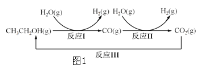

已知:反应I和反应Ⅱ的平衡常数随温度变化曲线如图2所示:
(1)①写出反应I中的化学方程式是________________。
②若反应I在恒温恒压条件下,向体系中充入N2,乙醇的平衡转化率___(填“增大”、“减小”或“不变”),理由是___________。
(2)反应Ⅱ在进气比[n(CO):n(H2O)]不同,测得相应的CO的平衡转化率见下图3(各点对应的反应温度可能相同,也可能不同)。
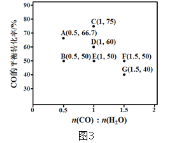
①图中D、E两点对应的反应温度分别为TD和TE。判断:TD______________TE(填“<”“=”或“>”);
②当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是___(用简要的文字叙述)。
(3)已知:
a、2CH3OH(g) + CO2(g)  CO(OCH3)2(g) + H2O(g) △H = -15.5 kJ/mol,该反应在0 ℃时K≈10-4.5;
CO(OCH3)2(g) + H2O(g) △H = -15.5 kJ/mol,该反应在0 ℃时K≈10-4.5;
b、2CH3OH(g) + CO2(g) +  (g)
(g)  CO(OCH3)2(g) +
CO(OCH3)2(g) +  (g)△H = -110.7 kJ/mol。依据以上数据,文献认为反应a没有工业价值,你认为其理由是______________________;但反应b引入环氧丙烷(
(g)△H = -110.7 kJ/mol。依据以上数据,文献认为反应a没有工业价值,你认为其理由是______________________;但反应b引入环氧丙烷( )可有效促进CO2与CH3OH反应生成CO(OCH3)2,其原因是_________________________________。
)可有效促进CO2与CH3OH反应生成CO(OCH3)2,其原因是_________________________________。
-
乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气具有良好的应用前景。已知通过乙醇制取氢气有如下两条路线:
a.水蒸气催化重整:CH3CH2OH(g) +H2O(g)®4H2(g) +2CO(g) DH =+255.58 kJ·mol-1
b.部分催化氧化:CH3CH2OH(g)+ O2(g)®3H2(g)+2CO(g) DH =+13.76kJ·mol-1
O2(g)®3H2(g)+2CO(g) DH =+13.76kJ·mol-1
则下列说法错误的是( )
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.按b路线进行,体系的能量会降低
-
(5分)氢能是高效、清洁能源,制氢技术的研究开发是氢能利用的必由之路。燃料水蒸气重整法是一种有效、经济、广泛采用的制氢方法,它是通过水蒸气与燃料间的反应来制取氢气的。
(1)在催化剂作用下,天然气和水蒸气反应可制得一氧化碳和氢气,已知该反应每制得1kg氢气需要吸收3.44×104 kJ热量。写出该反应的热化学方程式 ;
(2)CO可继续与水蒸气反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.0kJ·mol-1。若将1mol甲烷与足量水蒸气充分反应得到1molCO2,该反应的焓变ΔH= ;
(3)欲制得较纯净的氢气,可将(2)中充分反应后的气体通过足量的烧碱溶液,写出该反应的离子方程式 ;
-
甲醇水蒸气重整制氢(SRM)是用于驱动电动汽车的质子交换膜燃料电池的理想氢源,当前研究主要集中在提高催化剂活性和降低尾气中CO含量,以免使燃料电池Pt电极中毒。重整过程发生的反应如下:
反应I CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH1
CO2(g)+3H2(g) ΔH1
反应Ⅱ CH3OH(g) CO(g)+2H2(g) ΔH2
CO(g)+2H2(g) ΔH2
反应Ⅲ CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
其对应的平衡常数分别为K1、K2、K3,其中K2、K3随温度变化如下表所示:
| 125℃ | 225℃ | 325℃ |
| K2 | 05535 | 1858 | 9939.5 |
| K3 | 1577 | 137.5 | 28.14 |
请回答:
(1)反应Ⅱ能够自发进行的条件_______(填“低温”、“高温”或“任何温度”),ΔH1____ΔH3(填“>”、“<”或“=”)。
(2)相同条件下,甲醇水蒸气重整制氢较甲醇直接分解制氢(反应Ⅱ)的先进之处在于___________________________________________________________________。
(3)在常压、Cat.1催化下,CH3OH和H2O混和气体(体积比1∶1.2,总物质的量2.2mol)进行反应,tl时刻测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。
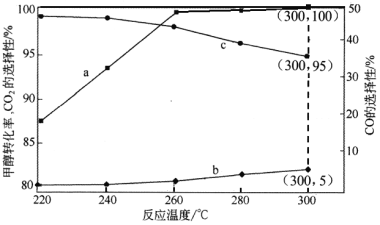
注:曲线a表示CH3OH的转化率,曲线b表示CO的选择性,曲线c表示CO2的选择性
① 下列说法不正确的是__________。
A.反应适宜温度为300℃
B.工业生产通常在负压条件下进行甲醇水蒸气重整
C.己知Cat.2催化剂具有更高催化活性,可提高甲醇平衡转化率
D.添加CaO的复合催化剂可提高氢气产率
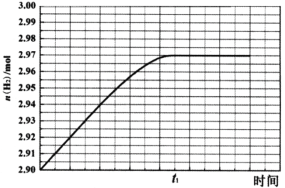
② 260℃时H2物质的量随时间的变化曲线如图所示。画出300℃时至t1时刻H2物质的量随时间的变化曲线。________________
(4)副产物CO2可以在酸性水溶液中电解生成甲酸,生成甲酸的电极反应式是:___________。
-
以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命。
(1)以甲醇为原料制取高纯H2是重要研究方向。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应:CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49 kJ•mol-1
CO2(g)+3H2(g) △H=+49 kJ•mol-1
副反应:H2(g)+CO2(g) CO(g)+H2O(g) △H=+41 kJ•mol-1
CO(g)+H2O(g) △H=+41 kJ•mol-1
①甲醇在催化剂作用下裂解可得到H2和CO,则该反应的化学方程式为_________________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________。
②分析适当增大水醇比(nH2O∶nCH3OH)对甲醇水蒸气重整制氢的好处_________________________。
③某温度下,将nH2O∶nCH3OH =1∶1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为_________________________。(忽略副反应)
(2)工业常用CH4 与水蒸气在一定条件下来制取H2,其原理为:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+203kJ·mol-1
①该反应的逆反应速率表达式为; V逆=k·c(CO)·c3(H2),k为速率常数,在某温度下,测得实验数据如表:
| CO浓度(mol·L-1) | H2浓度(mol·L-1) | 逆反应速率(mol·L-1·min-1) |
| 0.05 | C1 | 4.8 |
| c2 | C1 | 19.2 |
| c2 | 0.15 | 8.1 |
由上述数据可得该温度下,上述反应的逆反应速率常数k 为__________L3·mol-3·min-1。
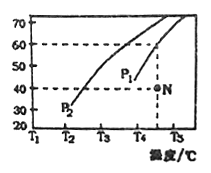
②在体积为3L的密闭容器中通入物质的量均为3mol 的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示,则压强Pl_____P2(填“大于”或“小于”)温度T3_______T4(填“大于”或“小于”);压强为P1时,在N点; v正_______v逆(填“大于”或“小于”或“等于”)。求N点对应温度下该反应的平衡常数 K=_____________________。
-
“可持续再生的绿色能源”是科学家目前正在研究的新能源之一。利用高粱、玉米等绿色植物的种子[主要成分是淀粉(C6H10O5)n],经发酵、蒸馏就可以得到该能源物质,它是( )
A.氢气(H2) B.酒精 (C2H5OH) C.甲烷(CH4) D.可燃冰
-
“可持续再生的绿色能源”是科学家目前正在研究的新能源之一。利用高粱、玉米等绿色植物的种子[主要成分是淀粉(C6H10O5)n],经发酵、蒸馏就可以得到该能源物质,它是( )
A.氢气 B.酒精 C.甲烷 D.可燃冰
-
“可持续再生的绿色能源”是科学家目前正在研究的新能源之一。利用高粱、玉米等绿色植物的种子[主要成分是淀粉(C6H10O5)n],经发酵、蒸馏就可以得到该能源物质,它是( )
A.氢气 B.酒精 C.甲烷 D.可燃冰
-
“可持续再生的绿色能源”是科学家目前正在研究的新能源之一.利用高粱、玉米等绿色植物的种子[主要成分是淀粉(C6H10O5)n],经发酵、蒸馏就可以得到该能源物质,它是( )
A.氢气
B.酒精
C.甲烷
D.可燃冰
-
氢能是一种应用前景非常广阔的新能源,但目前仍处于研究、试验阶段,还未能进入实用阶段,其主要原因是
①氢气燃烧对环境影响的评价尚无定论②氢气的制取耗能巨大,廉价制氢技术尚未成熟③氢气贮存、运输等安全技术尚未完全解决④氢气燃烧的放热量低于相同质量的矿物燃料,经济效益欠佳
A.①②
B.②③
C.③④
D.①④


CO(OCH3)2(g) + H2O(g) △H = -15.5 kJ/mol,该反应在0 ℃时K≈10-4.5;
(g)
CO(OCH3)2(g) +
(g)△H = -110.7 kJ/mol。依据以上数据,文献认为反应a没有工业价值,你认为其理由是______________________;但反应b引入环氧丙烷(
)可有效促进CO2与CH3OH反应生成CO(OCH3)2,其原因是_________________________________。


