下列反应中,可用离子方程式H++OH-===H2O表示的是
A. NH4Cl+NaOHNaCl+NH3↑+H2O
B. Mg(OH)2+2HCl===MgCl2+2H2O
C. NaOH+NaHCO3===Na2CO3+H2O
D. NaOH+HNO3===NaNO3+H2O
高三化学单选题中等难度题
下列反应中,可用离子方程式H++OH-===H2O表示的是
A. NH4Cl+NaOHNaCl+NH3↑+H2O
B. Mg(OH)2+2HCl===MgCl2+2H2O
C. NaOH+NaHCO3===Na2CO3+H2O
D. NaOH+HNO3===NaNO3+H2O
高三化学单选题中等难度题
下列反应中,可用离子方程式H++OH-===H2O表示的是
A. NH4Cl+NaOHNaCl+NH3↑+H2O
B. Mg(OH)2+2HCl===MgCl2+2H2O
C. NaOH+NaHCO3===Na2CO3+H2O
D. NaOH+HNO3===NaNO3+H2O
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
下列反应中,可用离子方程式H++OH-=H2O表示的是
A.NH4Cl+NaOHNaCl+NH3↑+H2O B. NaOH+HNO3=NaNO3+H2O
C.Mg(OH)2+2HCl=MgCl2+2H2O D. NaOH +NaHCO2=NaHCO3+H2O
高三化学选择题简单题查看答案及解析
能正确表示下列反应的离子方程式是
A.碳酸钠溶液和醋酸反应:2H+ + CO ═CO2↑+H2O
B.Na2S水【解析】
S2-+2H2O═H2S+2OH—
C.镁粉撒入NH4Cl溶液:Mg+2H+═Mg2++H2↑
D.Mg(HCO3)2溶液和足量NaOH溶液反应
Mg2++4OH—+2HCO═Mg(OH)2↓+ 2CO
+2H2O
高三化学选择题简单题查看答案及解析
(14分)我国制碱工业的先驱——侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
NH3+CO2+NaCl+H2O===NH4Cl+NaHCO3(晶体),
依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
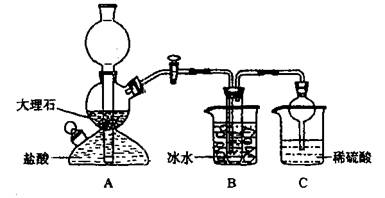
(1)A装置中所发生反应的离子方程式为________。
C装置中稀硫酸的作用为________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水的目的是________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指寻教师指出应在________装置之间(填写字母)连接一个盛有________的洗气装置,其作用是。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为________。
高三化学实验题中等难度题查看答案及解析
下列反应的离子方程式不正确的是
A. 向Ba(OH)2溶液中逐滴加入NH4HS04溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+=BaSO4↓+NH3·H2O+H2O
B. 向Mg(HC03)2溶液中加入足量澄清石灰水:Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+Mg(OH)2↓+2H2O
C. 氢氧化铁胶体的制备:Fe3++3H2OFe(OH)3(胶体)+3H+
D. 标准状况下将112mL氯气通入l0mL 1mol·L-l的溴化亚铁溶液中:2Fe3++4Br-+3Cl2=2Fe2++2Br2+6Cl-
高三化学单选题中等难度题查看答案及解析
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
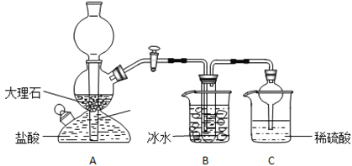
(1)A装置中所发生反应的离子方程式为:_________________。C装置中稀硫酸的作用为:________________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为________________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 ______装置____之间(填写字母)连接一个盛有_________ 的洗气装置,其作用是___________。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结论:______________。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为__________。
高三化学实验题中等难度题查看答案及解析
(14分)我国制碱工业的先驱侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓(晶体)依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
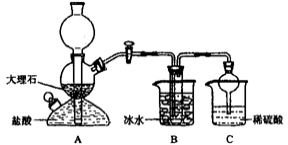
(1)A装置中所发生反应的离子方程式为________。C装置中稀硫酸的作用为_________。
(2)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在装置 之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(3)过滤NaHCO3 时除烧杯、漏斗外,还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的晶体的质量为5.04g,则NaHCO3的产率为 。
高三化学实验题困难题查看答案及解析
[2012·北京石景山一模](10分)我国制碱工业的先驱侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3(晶体)
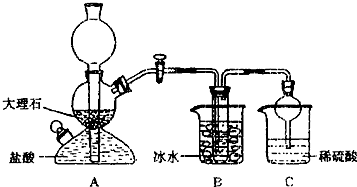
依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
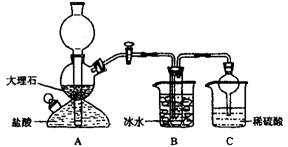
(1)A装置中所发生反应的离子方程式为________。
C装置中稀硫酸的作用为________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
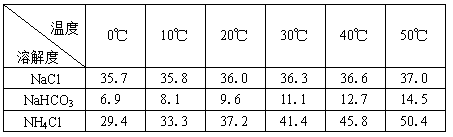
参照表中数据,请分析B装置中使用冰水的目的是________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在________装置之间(填写字母)连接一个盛有________的洗气装置,其作用是________。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为________。
高三化学实验题中等难度题查看答案及解析
| 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
高三化学解答题中等难度题查看答案及解析