-
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
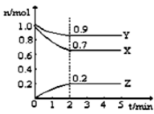
(1)由图中所给数据进行分析,该反应的化学方程式为 。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)= 。
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变),混合气体密度比起始时 (填增大、减小或不变)。
(4)下列措施能加快反应速率的是 。
A.恒容时充入X B.及时分离出Z C.降低温度 D.选择高效的催化剂
(5)下列说法正确的是 。
A.升高温度可以改变化学反应的平衡状态
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.达到化学反应的平衡状态与时间长短无关
D.化学反应的平衡状态是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
-
某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。

(1)由图中所给数据进行分析,该反应的化学方程式为 ;
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)= ;
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变);混合气体密度比起始时 (填增大、减小或不变)。
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) = n (Z),则原混合气体中a : b = 。
(5)下列措施能加快反应速率的是 。
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢
-
某温度时,在2L的密闭容器中,X、Y、Z(均为气体) 三种物质的量随时 间的变化曲线如图所示。
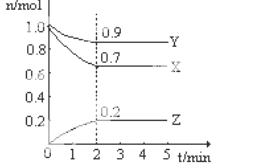
(1)由图中所给数据进行分析,该反应的化学方程式为_____________;
(2)反应从开始至2 分钟,用Z的浓度变化表示的平均反应速率为v(Z)=___________;
(3) 2min反应达平衡容器内混合气体的平均相对分子质量比起始时________(填增大、减小或无变化,下同);混合气体密度比起始时____________。
(4)下列措施能加快反应速率的是_______________。
A. 恒压时充入He B.恒容时充入He C.恒容时充入X
D.及时分离出Z E.升高温度 F.选择高效的催化剂
(5)下列说法正确的是___________。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反 应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y 的浓度,正反应速率加快,逆反应速率减慢
-
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。

(1)X的转化率是_______;
(2)由图中所给数据进行分析,该反应的化学方程式为_______________;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________;
(4)当反应进行到第___min,该反应达到平衡。若三种物质都是气体,平衡时Y所占体积的百分比为______。
-
(6分)某温度时,在2 L的密闭容器中,M、N两种物质的量随时间的变化曲线如下图所示。
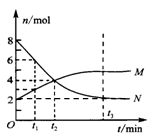
(1)达到平衡时N的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为 ;
(3)若t2=2,则反应从开始至2分钟末,用M的浓度变化表示的平均反应速率为 v(M)= ;
-
某温度时,在容积为2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:

(1)计算反应开始2 min内的平均反应速率:vY=__,vX=__。
(2)容器内的反应物是_______。
(3) 起始与2min时的压强之比_________。
(4)写出该反应的化学方程式________________________________。
-
某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:
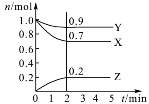
(1)该反应的化学方程式为 。
(2)反应开始至2 min,用Y表示的平均反应速率为 ,X的转化率为 。
(3)在密闭容器里,通入a mol A(g)和b mol B(g),发生反应A(g)+ B(g)= 2C(g),当改变下列条件时,会加快反应速率的是 (填序号)。
①降低温度 ②保持容器的体积不变,充入氦气
③加入催化剂 ④保持容器的体积不变,增加A(g)的物质的量
-
某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
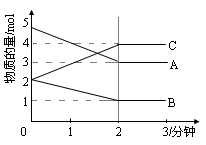
(1)该反应的化学方程式: ;
(2)反应开始至2min末,A的反应速率为 ;
(3)该反应是由 开始进行的。填序号
①正反应 ②逆反应 ③正逆反应同时
-
(Ⅰ)(6分)配平下列氧化还原反应方程式:

(Ⅱ)(10分)某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:

(1)计算反应开始2min内的 =________,
=________,  =________,
=________, =,
=,
(2)容器内的反应物是________。
(3)写出该反应的化学方程式________。
-
某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:

(1)该反应的化学方程式: ;
(2)反应开始至2min末,X的反应速率为 ;
(3)平衡时Z的转化率为 .
(4)3min后图中曲线所表示的含义是 .










