-
工业上通过电解MnSO4和ZnSO4制取Zn和MnO2,原料为软锰矿和闪锌矿。软锰矿主要含有MnO2(约70%)、SiO2、Al2O3,闪锌矿主要含有ZnS(约80%)、FeS、CuS、SiO2。
I.(1)为了测量软锰矿中MnO2含量的测定,现将14.5g软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取25.00ml该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用0.1000mol·L﹣1的标准Na2S2O3溶液滴定,消耗标准液50.00ml,则软锰矿中MnO2含量____。(已知:2KI+2H2SO4+MnO2=I2+2H2O+MnSO4+K2SO4 ;I2+2S2O32﹣=2I﹣+S4O62﹣)
Ⅱ.研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图所示。请回答下列问题:
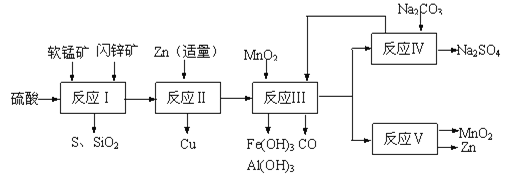
(2)反应Ⅰ后过滤所得滤液中含有有Mn2+、Zn2+、Cu2+、Fe3+、Al3+等金属阳离子。试写出反应Ⅰ中生成CuSO4的化学方程式____________。
(3)若反成Ⅱ加入的锌过量,还会进一步发生反应的离子方程式为_________。
(4)反应Ⅲ中加入MnO2的作用是(离子方程式表示)______________________。
(5)反应Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为__________。
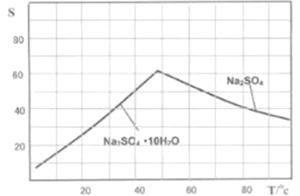
(6)图是Na2SO4和Na2SO4·10H2O的溶解度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶→___→用乙醇洗涤→干燥.用乙醇洗涤而不用水洗的原因是___________。
-
MnO2和Zn是制造普通干电池的重要原料,工业上用软锰矿(主要成分MnO2)和闪锌矿(主要成分ZnS)来制取:
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
 MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4
下列说法错误的是
A.干电池是一种将化学能转变为电能的装置
B.步骤③电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O=MnO2+4H+
C.步骤①每析出12.8g S沉淀,共转移0.8mol电子
D.步骤③的反应也可以设计成原电池
-
某工厂用软锰矿(含MnO2约70%及Al2 O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2,和Zn(干电池原料)。流程如下:
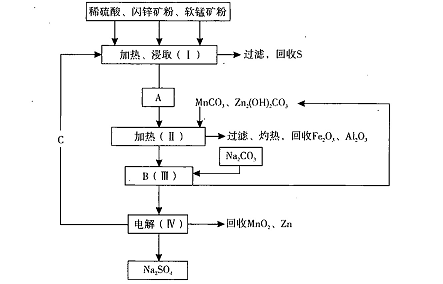
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3,Al2(SO4)3的混合液。
②IV中的电解反应式为MnSO4+ZnSO4+2H2O MnO2+Zn +2H2SO4。
MnO2+Zn +2H2SO4。
(1)A中属于还原产物的是________。
(2)加入MnCO3、Zn2(OH)2CO3的作用是________:C的化学式是________。
(3)该生产中除得到Na2SO4、S等副产品外,还可得到的副产品是________。
(4)副产品S可用于制硫酸,转化过程是:S→SO2→SO3→H2SO4。写出第二步转化的化学方程式________。
(5)要从Na2SO4溶液中得到芒硝( Na2SO4.10H2O),需进行的操作有蒸发浓缩、________、
过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿投料的质量比大约是________。
-
某工厂用软锰矿(含MnO2约70%及少量Al2O3)和闪锌矿(古ZnS约80%及少量FeS)共同生产MnO2和Zn(干电池原料)生产工艺如下:
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.
②IV中的电解反应式为:MnSO4+ZnSO4+2H2O═MnO2+Zn+2H2SO4
(1)A中属于还原产物的是________.
(2)Ⅱ中加入MnCO3、Zn2(OH)2CO3的作用是________;
Ⅱ需要加热的原因是________;C的化学式是________.
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是________.
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是________.
(5)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是________.

-
某工厂用软锰矿(含MnO2约70% 及A12O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料):
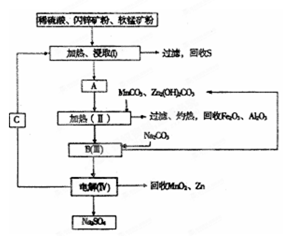
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②IV中的电解方程式为
(1)A中属于还原产物的是_____。
(2)加人MnCO3、Zn2(OH)2CO3的作用是_________________;II需要加热的原因是:______ ;C的化学式是_________。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是_____。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工 原料是_______。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进 行的操作有蒸发浓缩、 、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是____。
-
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS),共同生产MnO2和Zn(干电池原料)。
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②IV中的电解反应式为MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。

(1)A中属于还原产物的是 。
(2)MnCO3、Zn2(OH)2CO3的作用是 ;Ⅱ需要加热的原因是 ;C的化学式是 。
(3)Ⅲ中发生的离子方程式为 , ;
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是 。
-
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS),共同生产MnO2和Zn(干电池原料)。
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②IV中的电解反应式为MnSO4+ZnSO4+2H2O  MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。
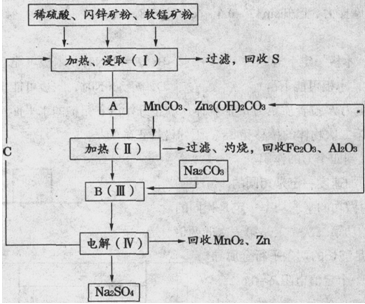
(1)A中属于还原产物的是________。
(2)MnCO3、Zn2(OH)2CO3的作用是________;Ⅱ需要加热的原因是________;C的化学式是________。
(3)Ⅲ中发生的离子方程式为________,________;
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是________。
-
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料):
已知①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.②IV中的电解反应式为MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4.
MnO2+Zn+2H2SO4.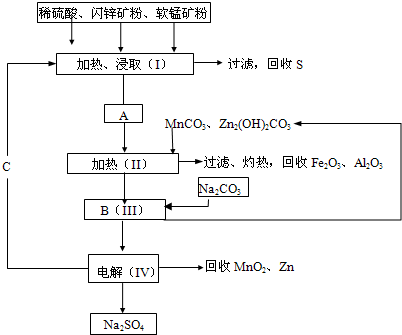
(1)A中属于还原产物的是______.
(2)MnCO3、Zn2(OH)2CO3的作用是______;II需要加热的原因是______;C的化学式是______.
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是______.
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是______.
(5)要从Na2SO4溶液中得到芒硝,需进行的操作有蒸发浓缩、______、过滤、洗涤、干燥等.
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是______.
-
MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
⑴ 软锰矿、闪锌矿与硫酸共热: MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O
⑵ 除去反应混合物中的不溶物
 ⑶ 电解混合液MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
⑶ 电解混合液MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4
下列说法不正确的是
A.步骤⑴中MnO2和H2SO4都是氧化剂
B.步骤⑴中每析出12.8g S沉淀共转移0.8mol电子
C.步骤(3)中电解时MnO2在阳极处产生
D.硫酸在生产中可循环使用
-
软锰矿主要含有MnO2(约70%)、SiO2、Al2O3,闪锌矿主要含有ZnS(约80%)、FeS、CuS、SiO2。为了高效利用这两种矿石,科研人员开发了综合利用这两种资源的同槽酸浸工艺,主要流程如下图所示,回答下列问题:

(1)反应Ⅰ所得滤液中含有Mn2+、Zn2+、Cu2+、Fe3+、Al3+等金属阴离子,所得滤液中含有S和______。为了提高硫酸“酸浸”时的浸出速率,可进行的操作是(至少两条):_________。
(2)若反成Ⅱ加入的锌过量,还会进一步发生反应的离子方程式方为_________。
(3)反应Ⅲ中加入MnO2的作用是(离子方程式表示)________;反应Ⅲ中加入MnCO3、ZnCO3的作用是________________。
(4)反应Ⅴ的电解总反应为:MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4,写出阳极的电极反应式________________。
MnO2+Zn+2H2SO4,写出阳极的电极反应式________________。
(5)MnO2和Zn可按等物质的量之比生产锌-锰干电池,则从生产MnO2和Zn的角度计算,所用软锰矿和闪铲矿的质量比大约是______。(保留小数点后两位)








