-
ClO2遇浓盐酸会生成Cl2 ,反应方程式为2ClO2 + 8HCl = 5Cl2+ 4H2O ,该反应中若转移电子的数目为9.632×1023,则产生的Cl2在标况下的体积为
A. 11.2L B. 33.6L C. 22.4L D. 44.8L
高三化学单选题中等难度题查看答案及解析
-
ClO2遇浓盐酸会生成Cl2,反应方程式为2ClO2+8HCl====5Cl2+4H2O,该反应中若转移电子的数目为9.632×1023,则产生的Cl2在标准状况下的体积为 ( )
A.11.2 L B.33.6 L C.22.4 L D.44.8 L
高三化学选择题中等难度题查看答案及解析
-
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯.其变化可表述为:□KClO3+□HCl(浓)-□KCl+□Cl2↑+□ClO2↑+□______
(1)配平化学方程式并标出电子转移的方向和数目(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是______(填写编号,多选倒扣).
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1mol Cl2,则转移的电子的物质的量为______.
(4)ClO2具有很强的氧化性.因此,常被用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是Cl2的______倍.高三化学解答题中等难度题查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:2NaClO3+4HCl═2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是( )
A. 浓盐酸在反应中仅体现还原性 B. 每生成0.1mol ClO2转移0.5mol电子
C. 氧化性:NaClO3<ClO2 D. 被氧化和被还原的物质的物质的量之比为1:1
高三化学单选题中等难度题查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是
A.浓盐酸在反应中仅体现还原性
B.氧化性:NaClO3 <ClO2
C.每生成0.lmol ClO2转移0.5mol电子
D.被氧化和被还原的物质的物质的量之比为1:1
高三化学选择题中等难度题查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:
2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是
A.浓盐酸在反应中仅体现还原性
B.每生成0.lmol ClO2转移0.5mol电子
C.氧化性:NaClO3 <ClO2
D.被氧化和被还原的物质的物质的量之比为1:1
高三化学选择题中等难度题查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:
2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是( )
A.浓盐酸在反应中仅体现还原性
B.每生成0.lmol ClO2转移0.5mol电子
C.氧化性:NaClO3 <ClO2
D.被氧化和被还原的物质的物质的量之比为1:1
高三化学选择题中等难度题查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:
2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是
A. 浓盐酸在反应中仅体现还原性
B. 氧化性:NaClO3 <ClO2
C. 每生成0.lmol ClO2转移0.5mol电子
D. 被氧化和被还原的物质的物质的量之比为1:1
高三化学选择题中等难度题查看答案及解析
-
(10分)按要求完成下列各题。
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为: 。
(2)ClO2常用子水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式: 。
(3)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4,反应的化学方程式为: 。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 。
(4)(CN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为
。
高三化学填空题中等难度题查看答案及解析
-
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.请回答下列问题:
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl═2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是 (填序号).
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为 mol.
(2)目前已开发出用电解法制取ClO2的新工艺.
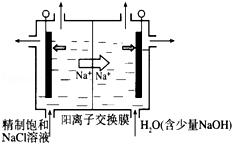
①上述生产示意图用石墨做电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式: .
②电解一段时间后,当阴极产生的气体体积为112mL(标准状况)时,停止电解.则通过阳离子交换膜的阳离子的物质的量为 mol;
③用平衡移动原理解释阴极区pH增大的原因 .
高三化学填空题困难题查看答案及解析