-
已知
表示阿伏加德罗常数的值,下列有关说法正确的是( )
A.1 mol CnH2n(n≥2)中所含的共用电子对数为(3n+1)NA
B.在12.0 g NaHSO4 和MgSO4混合物中,所含离子数目为0.2NA
C.1 L 1 mol·L-1饱和FeCl3溶液滴入沸水中完全水解生成Fe(OH)3胶粒数为NA
D.标准状况下8.96 L D2含有中子数0.4NA
高三化学单选题中等难度题查看答案及解析
-
纵观古今,化学与生活皆有着密切联系。下列说法正确的是( )
A.《本草图经》在绿矾项记载:“盖此矾色绿,味酸,烧之则赤……”。因为绿矾能电离出H+,所以“味酸”
B.“司南之杓(勺),投之于地,其柢(勺柄)指南”,司南中“杓”的材质为Fe2O3
C.用盐酸能鉴别纯碱和食盐,只用蒸馏水不能。
D.东汉魏伯阳在《周易参同契》中对汞的描述:“……得火则飞,不见埃尘,将欲制之,黄芽为根。”这里的“黄芽”是指硫黄
高三化学单选题中等难度题查看答案及解析
-
水的电离平衡曲线如图所示,下列说法中,正确的是
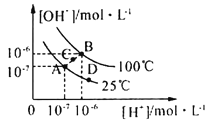
A.图中A、B、D三点处Kw的大小关系:B>A>D
B.25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3·H2O)的值逐渐减小
C.在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、SO42—
高三化学单选题中等难度题查看答案及解析
-
短周期主族元素W、X、Y、Z的原子序数依次增大。W的某种核素不含中子;X、Y原子核外L层的电子数之比为3︰4;X与Z同主族,且X、Y、Z原子的最外层电子数之和为16。下列说法不正确的是( )
A.W、X、Z三种元素形成的化合物一定为强电解质
B.简单氢化物的稳定性:X>Z>Y
C.X分别可与W、Z各形成两种常见化合物
D.原子半径:Y>Z>X>W
高三化学单选题中等难度题查看答案及解析
-
下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是
选项
离子组
试剂X
离子方程式
A
Fe3+、Al3+、
、
过量的盐酸
+2H+═H2O+SO2↑
B
透明溶液中:Fe3+、
、
、Cl-
过量的铜粉
2Fe3++Cu═2Fe2++Cu2+
C
Na+、Ba2+、
、Cl-
NaHSO4溶液
H++
═CO2↑+H2O
D
pH=1的溶液中:Mg2+、Fe2+、
、
双氧水
2Fe2++H2O2+2H+═2Fe3++2H2O
A.A B.B C.C D.D
高三化学单选题中等难度题查看答案及解析
-
探究补铁剂[主要成分:氯化血红素(含+2 价铁)、富锌蛋白粉、维生素 C、乳酸、葡萄糖浆] 中铁元素是否变质。先取少量补铁剂,用酸性丙酮溶解后制成溶液。
实验Ⅰ
实验Ⅱ
实验Ⅲ
取待测液,加入少量 KSCN 溶液,无明显现象;再加入少量H2O2,溶液不变红
取实验Ⅰ所得溶液,再加入少量KSCN 溶液,无明显现象;再加入H2O2溶液,溶液变为红褐色
取实验Ⅰ所得溶液,加入少量盐酸溶液,无明显现象,继续加入H2O2 至过量,溶液先变红后褪色
下列说法不正确的是
A.实验Ⅰ中加入KSCN 溶液无明显现象,与 KSCN 溶液的用量无关
B.实验Ⅰ中加入H2O2溶液后不变红,可能是H2O2被维生素 C 还原了
C.实验Ⅲ中溶液红色褪去,可能是H2O2将SCN-氧化了
D.实验说明,该补铁剂中+2 价铁在酸性条件下才能被H2O2氧化
高三化学单选题中等难度题查看答案及解析
-
25℃时,向 10mL 0.01 mol/L NaCN 溶液中逐滴滴加 10mL0.01 mol/L 的盐酸,其 pH 变化曲线如图所示。下列溶液中的关系一定正确的是(忽略体积微小变化)
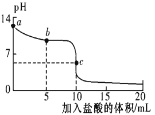
A.a 点溶液的 pH ≥12
B.b 点的溶液:c(CN-)> c(Cl-)>c(HCN )
C.pH =7 的溶液:c(Na+)+ c(H+) =c(Cl-)+ c(CN-)
D.c 点的溶液:c(CN-)+c(HCN ) +c(Cl-)=0.01 mol/L
高三化学单选题中等难度题查看答案及解析
-
从海水中制备纯碱和金属镁的流程如下图所示:
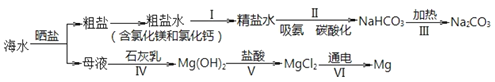
下列说法不正确的是
A.流程 I 依次向粗盐水中加入过量 Ca(OH)2 溶液、Na2CO3 溶液并过滤
B.流程 II 吸氨是使溶液呈碱性,有利于吸收二氧化碳
C.海水提镁流程中涉及到三种基本反应类型
D.流程 IV、V 是通过化学方法富集镁元素
高三化学单选题中等难度题查看答案及解析
-
已知 443℃时: 2HI(g)⇌H2(g) +I2(g) ΔH = +12.5 kJ·mol-1 ,443℃时,向 1L 密闭容器中充入 1 mol HI,体系中 c(HI)与反应时间 t 的关系如下图所示。下列说法中,正确的是

A.反应进行 40 min 时,体系吸收的热量约为 0.9375 kJ
B.升高温度,再次平衡时,c(HI) > 0.78 mol·L-1
C.0~20 min 内的平均反应速率可表示为υ(H2) = 0.0045 mol·L-1·min-1
D.该反应的化学平衡常数计算式为
高三化学单选题中等难度题查看答案及解析
-
下列实验现象预测正确的是
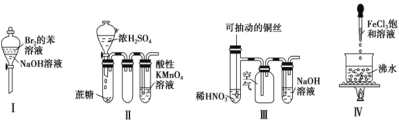
① 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
② 实验Ⅱ:酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
③ 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
④ 实验Ⅳ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
A.①② B.③④ C.①③ D.②④
高三化学单选题中等难度题查看答案及解析