-
为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取10g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图(见图)。
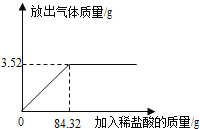
(1)碳酸钙完全反应用去稀盐酸的质量为__________g。
(2)该石灰石样品中碳酸钙的质量分数为_________。
(3)当盐酸和石灰石恰好完全反应,所得溶液中溶质质量分数是_____________
高三化学计算题中等难度题查看答案及解析
-
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1) 若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。样品中铝的质量是_____________g。
(2) 若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:________,氧化铁与铝的质量比是________。
(3) 待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=______________。
高三化学计算题中等难度题查看答案及解析
-
在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
实验序号
甲
乙
丙
合金质量/g
0.255
0.385
0.459
生成气体/ml
280
336
336
(1)该盐酸的物质的量浓度____________;
(2)合金中Mg、Al的物质的量之比为___________;
(3)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为AlO2-,并使Mg2+刚好沉淀完全,则溶液中AlO2-的物质的量为__________mol;溶液中Na+的物质的量为_________mol;所加NaOH溶液的体积为_________mL。
高三化学计算题中等难度题查看答案及解析
-
将金属M的样品2.5g放入50g 19.6%的硫酸溶液中,恰好完全反应(样品中的杂质既不溶于硫酸,也不与其发生反应),生成硫酸盐。实验测知,此硫酸盐中硫、氧元素的质量分数之和为80 %。试求:
(1)原金属样品中,金属M的质量分数_____
(2)M的相对原子质量__________
(3)反应所得的硫酸盐溶液中溶质的质量分数___________
高三化学计算题中等难度题查看答案及解析
-
已知Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,现在向0.001 mol·L-1K2CrO4和0.01 mol·L-1KCl混合液中滴加0.01 mol·L-1AgNO3溶液,通过计算回答:
(1)Cl-、CrO42-谁先沉淀________?
(2)刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是________?(设混合溶液在反应中体积不变)
高三化学计算题中等难度题查看答案及解析
-
(1)已知Ksp(AgCl)=1.8×10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag+)是________?
(2)已知Ksp[Mg(OH)2]=1.8×10-11,则将Mg(OH)2放入蒸馏水中形成饱和溶液,溶液的pH为________?
(3)在0.01 mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的pH是________?当Mg2+完全沉淀时,溶液的pH为________?
高三化学计算题中等难度题查看答案及解析
-
求下列溶液的pH(常温条件下)(已知lg2=0.3)
(1)0.005 mol·L-1的H2SO4溶液________
(2)已知CH3COOH的电离常数Ka=1.8×10-5,0.1 mol·L-1的CH3COOH溶液________
(3)0.1 mol·L-1NH3·H2O溶液(NH3·H2O的电离度为α=1%,电离度=
 ×100%)________
×100%)________(4)将pH=8的NaOH与pH=10的NaOH溶液等体积混合________
(5)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11∶9混合________
(6)将pH=3的HCl与pH=3的H2SO4等体积混合________
(7)0.001 mol·L-1的NaOH溶液________
(8)pH=2的盐酸与等体积的水混合________
(9)pH=2的盐酸加水稀释到1 000倍________
高三化学计算题中等难度题查看答案及解析
-
一瓶久置的Na2SO3(杂质只有Na2SO4),为了测定其纯度,取样品5.0 g配成100 mL溶液,取其中25.00 mL于锥形瓶中,用0.10 mol•L-1酸性KMnO4溶液进行滴定,到终点时消耗KMnO4溶液20.00 mL,求此样品的纯度。_______________
高三化学计算题中等难度题查看答案及解析
-
t℃时,向足量饱和Na2CO3(aq)中,加入1.06 g无水Na2CO3,搅拌后静置,并冷却至t℃,最终所得晶体质量为5.83 g,求该温度下Na2CO3的溶解度。_____________
高三化学计算题中等难度题查看答案及解析
-
求下列溶液的pH(常温条件下)(已知lg2=0.3)
(1)0.005 mol·L-1的H2SO4溶液________
(2)已知CH3COOH的电离常数Ka=1.8×10-5,0.1 mol·L-1的CH3COOH溶液________
(3)0.1 mol·L-1NH3·H2O溶液(NH3·H2O的电离度为α=1%,电离度=
 ×100%)________
×100%)________(4)将pH=8的NaOH与pH=10的NaOH溶液等体积混合________
(5)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11∶9混合________
(6)将pH=3的HCl与pH=3的H2SO4等体积混合________
(7)0.001 mol·L-1的NaOH溶液________
(8)pH=2的盐酸与等体积的水混合________
(9)pH=2的盐酸加水稀释到1 000倍________
高三化学计算题中等难度题查看答案及解析