-
丁苯酞(J)是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下:

(1)H中含氧官能团的名称为_____、_____。
(2)D的系统命名是___________;J的结构简式为_____________。
(3)由A生成B的化学方程式为_______________________,反应类型__________。
(4)C与银氨溶液反应的化学方程式为_______________________________________。
(5)H在一定条件下生成高分子化合物的结构简式为_______________。
(6)G的同分异构体中核磁共振氢谱有4组峰,且能与FeCl3溶液发生显色反应,写出其中两种符合上述条件的同分异构体的结构简式_________________________。
(7)写出由物质A、甲醛、液溴为原料合成“2一苯基乙醇”的路线图:_______________________。
高三化学简答题中等难度题查看答案及解析
-
元素及其化合物在生活及生产中有很多重要用途。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)基态碳原子价电子的电子轨道表达式为____,第一电离能Ga____As(填“>”、 “<”、“=”)。
(2)BN和GaAs都是原子晶体,它们的硬度和熔点BN>GaAs,原因是________________。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。 (CN)2分子中氮原子的轨道杂化类型为_____,σ 键与 π 键数目之比为_______; (SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H—N=C=S),其原因是_________。
(4)①卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为_____________;②一定条件下(SCN)2可氧化为CO32—和SO32—等离子,其中SO32—的立体构型为_________。
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图1 所示),CaC2 晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。写出与C22﹣互为等电子体的微粒符号________、_______;此晶体中 1 个 C22﹣周围距离最近的Ca2+为______个;若该晶胞的边长为a、a、b(nm),则该晶体的密度为______ g·cm-3(写出表达式)。

高三化学简答题中等难度题查看答案及解析
-
充分利用黄铁矿(主要成份为FeS2)对资源和环境具有重要的意义。
(1)一种酸性条件下催化氧化黄铁矿的物质转化关系如下面图Ⅰ所示。
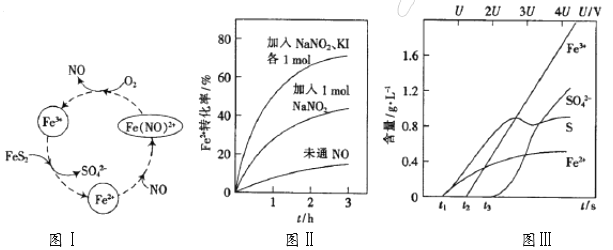
①图Ⅰ中,NO起的是_____作用;O2氧化FeS2生成Fe3+的离子方程式为____________;
②硝酸也可以将FeS2氧化为Fe3+和SO42-,但使用稀硝酸比浓硝酸的反应速率快很多,其原因是:_________。
(2)控制Fe3+的浓度、溶液体积和通入O2的速率一定,图Ⅱ表示当改变其它条件时Fe2+被氧化的转化率随时间的变化。
①加入NaNO2发生反应:3NO2-+2H+==NO3-+2NO↑+H2O。若3molNaNO2完全反应,则转移的电子数为____________________mol。
②在酸性溶液中,加入NaNO2、KI发生反应生成NO和I2,该离子反应方程式为______ ;图Ⅱ中曲线从下至上, Fe2+转化速率依次增大的原因是________。
(3)为研究FeS2作电极时的放电规律,以FeS2作阳极进行电解,由FeS2放电产生的粒子的含量与时间(t)、电压(U)之间的关系如图Ⅲ所示。
①t1至t2间FeS2发生的电极反应式为_________________。
②当电压值介于3.5U~4.4U之间时,FeS2放电所得的主要粒子为_______________。
③黄铁矿含有杂质钴和镍。若电解一段时间,c(Fe3+)=1×10-2mol·L-1时,通过计算判断:pH控制为_______不会产生Fe(OH)3沉淀;当使Co2+沉淀完全时,Fe3+_____(填:“已经”或“没有”)开始沉淀。{已知:离子浓度≤1×10–5mol·L–1认为沉淀完全;Ksp[Fe(OH)3]=3.8×10–38、Ksp[Co(OH)2]=2×10–15,
= – 0.16}
高三化学简答题中等难度题查看答案及解析
-
(1)用硫酸分解磷尾矿[主要成份为Ca5(PO4)3F]可制得中强酸磷酸H3PO4。请回答:
①Na2HPO4溶液呈碱性,则在该溶液中c(H2PO4-)_____c(PO43-)(填“>”、“<”、“=”),
向Na2HPO4溶液中加入足量的CaCl2溶液,溶液显酸性,溶液显酸性的原因是(从电离平衡移动角度分析):_____________________________。
②已知:25℃时,H3PO4的电离平衡常数:K1=7.52×10-3;K2=6.23×10-8;K3=6.23×10-13则:H3PO4(aq)+OH-(aq)
H2PO4-(aq)+H2O (l)的平衡常数K=______。
③Ca5(PO4)3F(s) +OH-(aq)
Ca5(PO4)3(OH) (s)+F-,该温度下,溶液中c(F-)随溶液的pH和温度(T)的变化曲线如右图所示。则:pH1___pH2(填“>”、“<”、“=”);A、B两点的溶液中F-的速率v(A)____v(B)(填“>”、 “<”、“=”)。

(2)处理含镍酸性废水可用电解法实现铁上镀镍,其装置如右图所示。
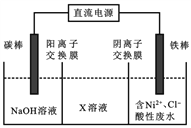
①电流方向是_____(填:a.碳棒→铁棒;b.铁棒→碳棒);
②中间隔室的可以得到的物质X是_______(填化学式);
③阳极的电极反应式为_______________;电解总反应的离子方程式为_______________。
高三化学简答题中等难度题查看答案及解析
-
A、B、C、D、E、R为原子序数依次增大的六种元素,位于元素周期表的前四周期。B元素原子含有3个能级,且毎个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子。请回答下列问题:
(1)写出C基态原子的价层电子排布____________,F基态原子的外围电子排布式_____________。
(2)下列说法正确的是____________ (填序号)。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2 > CO2
B.笫一电离能由小到大的顺序:B <C < D
C.N2与CO为等电子体,结构相似
D.稳定性:H2O> H2S,水分子更稳定的原因是水分子间存在氢键
(3) F元素位于周期表中_________区,其离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向F的硫酸盐溶液中通人过量的C与A形成的气体X可生成[F(X)4]2+,该离子的结构式为__________(用元素符号表示)。
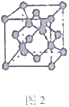
(4)某化合物与F(I)(I表示化合价为+ 1)结合形成下图1所示的离子,该离子中碳原子的杂化方式为____________________。
(5)B单质的一种同素异形体的晶胞如下图2所示,则一个晶胞中所含B原子的个数为____________。
(6)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为apm, F离子的半径bpm,则该晶胞的空间利用率为_______________。

高三化学简答题中等难度题查看答案及解析
-
CO2的转换在生产、生活中具有重要的应用。
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”。
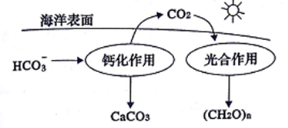
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为_________、___________________。
②在海洋碳循环中,可通过上图所示的途径固碳。写出钙化作用的离子方程式:____________。
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2
2Na2CO3+C。放电时,在正极得电子的物质为___________;充电时,阳极的反应式为___________。
(3) 目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5molCO2和1.5 mol H2转化率达80%时的能量变化示意图。能判断该反应达到化学平衡状态的依据_______(填字母)。
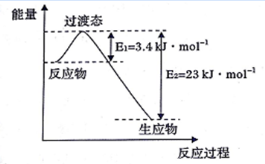
a.容器中压强不变 b.H2的体积分数不变
c.c(H2 =3c(CH3OH) d.容器中密度不变
e. 2个C = O断裂的同时有6个H - H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
CO2(g) +H2(g),得到如下三组数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达到平衡所
需时间/min
CO
H2O
H2
CO
1
650
4
2
1.6
2.4
6
2
900
2
1
0.4
1.6
3
3
900
a
b
c
d
t
①实验2条件下平衡常数K=____________。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值_________ (填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正____v(逆)(填“ <”、“ >”或“=")。
(5)已知在常温常压下:
①2CH3OH(I) +3O2(g)=2CO2(g) +4H2O(g) △H= -1275.6 kJ • mol-1
②2CO(g) +O2(g)=2CO2(g) △H = -566.0 kJ·mol-1
③H2O(g)=H2O(I) △H =-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_____________。
高三化学简答题中等难度题查看答案及解析
-
用硝酸氧化淀粉水解的产物(C6H12O6)可以制备草酸,装置如下图所示(加热、搅拌和仪器固定装置均己略去)。
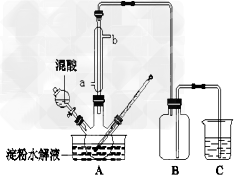
实验过程如下:
①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,得到淀粉水解液,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后得草酸晶体粗品,再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入少许98%硫酸的目的是:_____________________。
(2)冷凝水的进口是________(填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是______________________。
(3)装置B的作用是___________,为使尾气被充分吸收,C中的试剂是___________。
(4)重结晶时,将草酸晶体粗品经I加热溶解、Ⅱ趁热过滤、Ⅲ冷却结晶、Ⅳ过滤洗涤、Ⅴ干燥等实验步骤,得到较纯净的草酸晶体。该过程中可将粗品中溶解度较大的杂质在_________(填上述实验步骤序号)时除去;而粗品中溶解度较小的杂质最后留在_______(填“滤纸上”或“滤液中”)。
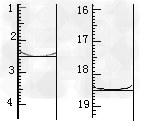
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。称取一定量该样品加适量水完全溶解,用KMnO4标准液滴定,反应的离子方程式为_________________。 滴定前后滴定管中的液面读数如图所示,则消耗KMnO4溶液的体积为_________。
(6)已知草酸是一种二元弱酸,草酸氢钠溶液(NaHC2O4)显酸性。常温下,向10 mL0.01 mol • L -1IH2C2O4溶液中加入10mL0.01mol·L-1NaOH溶液时,溶液中各种离子的浓度由大到小的顺序为________________。
高三化学简答题中等难度题查看答案及解析
-
三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。

已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。
请回答下列问题:
(1)步骤①转化的目的是____________,滤液1中的溶质为Na2CO3和______(填化学式)。
(2) 步骤③酸溶时,为提高酸溶速率,可采取的措施是____________________。
(任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为_____________。
(3)滤液2中可循环利用的溶质为__________(填化学式)。若步骤④沉铅后的滤液中c(Pb2+)=1.82×l0-5mol ·L-1,则此时 c(SO42-)________mol·L-1。
(4)步骤⑥合成三盐的化学方程式为_________ 。若得到纯净干燥的三盐49.5t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为__________。
简述步骤⑦洗涤沉淀的方法_______________________。
高三化学简答题中等难度题查看答案及解析
-
二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
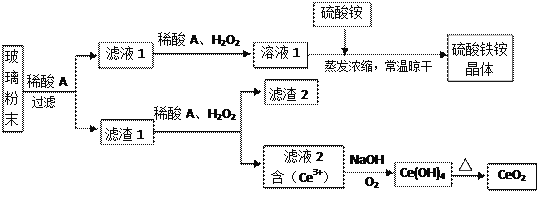
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是___________________。
(2)滤液1中加入H2O2溶液的目的是_________________________________________________。
(3)某同学设计实验证明滤液1中含有Fe2+,他所用的试剂为___________________。
(4)已知溶液中的Fe2+可以和难溶于水的FeO(OH)反应生成Fe3O4,请书写该反应的离子方程式_____________________________________________________________________________。
(5)由滤液2生成Ce(OH)4的离子方程式______________________________________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理。相对于去除中性废水,其在去除酸性废水中的悬浮物时效率_________(填“增强”或“降低”)。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。
该产品中Ce(OH)4的纯度为__________________。(保留两位有效数字)
高三化学简答题中等难度题查看答案及解析
-
某小组模拟工业合成氨,并制备NaHCO3,设计实验如下(夹持装置略去)。
回答下列问题:
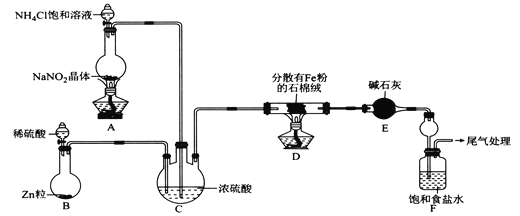
(1)装置E中盛放碱石灰的仪器名称为_____________________________。
(2)装置A中发生反应的离子方程式为___________________________________________________。
(3)装置C的作用为使N2和H2混合均匀______________________、_________________________。
(4)实验时,应先打开装置B中分液漏斗活塞,反应一段时间,在装置末端导管处收集H2并验纯后,再点燃D处酒精灯,原因为___________________________________________________________。
(5)当F中的氨气饱和后,取下装置F,再向其中通入足量CO2,现象为______________________;发生反应的离子方程式为______________________________________________________________。
高三化学简答题中等难度题查看答案及解析