-
下列几种物质:①H2O2 ②Na2O2 ③CO2 ④Ne ⑤MgCl2 ⑥NaOH ⑦O2。回答下列问题:
(1)含有共价键的离子化合物有__________。(填物质的序号)
(2)不含有任何化学键的物质有__________。(填物质的序号)
(3)与Na2O中阴阳离子个数比相等的物质有________。(填物质的序号)
(4)含有两种类型共价键的物质有________。(填物质的序号)
高一化学填空题中等难度题查看答案及解析
-
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1-36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
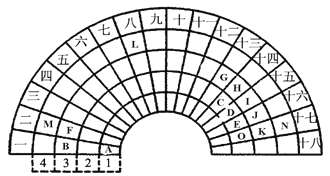
(1) D代表的元素处于常见元素周期表的位置是第 _____ 周期________ 族。
(2)元素F、G、I、K、M的原子半径由大到小的顺序是___________________(用元素符号表示)。
(3)B、F、G三种元素三种元素最高价氧化物对应水化物碱性最强的碱是_________(填化学式)。
高一化学填空题中等难度题查看答案及解析
-
A、B、C三种元素的原子序数依次为a、b、c ,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n > m,则a、b、c由大到小的排列顺序是____________。离子半径由大到小的排列顺序是_________(用离子符号表示)。
高一化学填空题中等难度题查看答案及解析
-
下表列出了A-R9种元素在周期表中的位置
周期\族
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
O
2
E
F
3
A
C
D
G
R
4
B
H
(1)这9种元素中化学性质最不活泼的是_______(填元素符号)
(2)D元素的最高价氧化物对应水化物与氢氧化钠反应的离子方程式是____________
(3)A、B、C三种元素按原子半径由大到小的顺序排列为______(填元素符号)
(4)F元素氢化物的化学式是_____,该氢化物在常温下跟B发生反应的化学方程式是_______,所得溶液的pH____7。
(5)H元素跟A元素形成化合物的化学式___,高温灼烧该化合物时,火焰呈____色。
(6)G元素和H元素两者核电荷数之差是______。
高一化学填空题中等难度题查看答案及解析
-
(1)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.4 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·2H2O(s)+8H2O(g) ΔH2=+373.6 kJ·mol-1
H2O(g)= H2O(l) ΔH3=-44kJ·mol-1
写出Na2CO3·2H2O脱水分解后生成碳酸钠固体和液态水的热化学方程式 。
(2)已知1g乙醇(C2H5OH)完全燃烧生成CO2气体和液态水时,放出29.7 kJ的热量,
写出乙醇燃烧热的热化学方程式为 。
高一化学填空题中等难度题查看答案及解析
-
(1)请写出以下物质的电子式:Na2O2__________H2S___________
(2)用“>”或“<”回答下列问题:
酸性:H2SiO3____H3PO4;稳定性:HCl____CH4;氧化性:Cu2+_____Fe3+
高一化学填空题中等难度题查看答案及解析
-
Ⅰ. CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+1/2O2(g)
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______(填字母)。
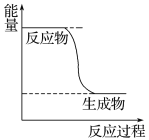
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=________________,则CH3OH的转化率为___________。
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)______________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________。
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为________,负极的电极反应式为_______________________________。当反应中收集到标准状况下224 mL气体时,消耗的a电极质量为________g。
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
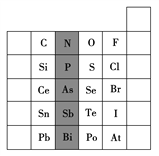
(1)阴影部分元素N在元素周期表中的位置为____周期第____族。根据元素周期律,预测酸性强弱:H3AsO4____H3PO4(填“>”或“<”)。
(2)S的最高化合价和最低化合价的代数和为____,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度____(填“更大”“更小”或“相同”)。
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是____。
(4)下列说法错误的是____(填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
高一化学填空题中等难度题查看答案及解析
-
在浓硝酸中放入铜片:
(1)开始反应的化学方程式为_______,实验现象为_______。
(2)若铜有剩余,则反应将要结束时的离子方程式为___________。
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况下)。则所消耗硝酸的物质的量是________________________。
高一化学填空题中等难度题查看答案及解析
-
以下六种物质是一个氧化还原反应的反应物和生成物:NO、FeSO4、H2O、Fe(NO3)3、HNO3和Fe2(SO4)3. 写出该反应方程式并配平,用单线桥标出电子转移方向与数目。____________________ ,该反应中,氧化剂是___________,被氧化的元素是___________,若产生标准状况下11.2L气体,转移电子数为____________。
高一化学填空题中等难度题查看答案及解析