-
电解原理在化学工业上有广泛应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
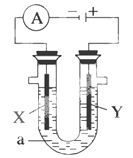
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,①电解池中X极上的电极反应式为 _____,在X极附近观察到的现象为__。
②Y电极上的电极反应式______,检验该电极反应产物的方法是__。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液(说明:杂质发生的电极反应不必写出)
①X电极的材料是_________,电极反应式为______________。
②Y电极的材料是__________,电极反应式为_____________。
高一化学填空题中等难度题查看答案及解析
-
普通锌锰干电池的结构如图所示。回答下列问题。
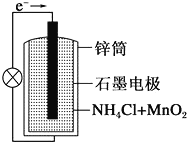
(1) ①电池中电解质溶液为________。
②正极反应式为_______________。
③放电时,NH 4 +向______(填“正极”或“负极”)移动。
(2)废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是____,原因是____。若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是_____(填序号)。
A.微热 B.加入适量氧化铜
C.加入少量硫酸铜溶液 D.加水
E.加入少量氢氧化钡溶液
高一化学填空题中等难度题查看答案及解析
-
(1)某温度时,在2 L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。由此分析,该反应的化学方程_____;从反应开始至2 min,Z的反应速率为______ mol·L-1·min-1。
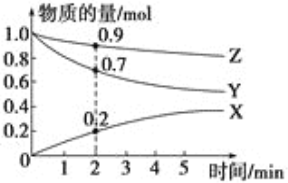
(2)若上述反应的△H<0,下列有关该反应速率的叙述,正确的是_____。
A.升高温度和增大压强均可以增大活化分子百分数,加快反应速率
B.使用催化剂可以使反应的活化能降低,加快反应速率
C.活化分子间所发生的碰撞为有效碰撞
D.降低温度,v正、v逆均减小且v正减小的倍数小于v逆减小的倍数
(3)在一密闭容器中发生反应N2(g)+3H2(g)
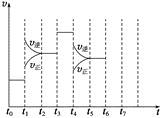
2NH3(g) △H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。t1、t3、t4时刻分别改变的一个条件是:
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氦气
t1时刻_____;t3时刻______;t4时刻______(填字母)。
高一化学填空题中等难度题查看答案及解析
-
一定温度下,冰醋酸加水稀释过程中溶液的导电能力有如图所示曲线,请回答。
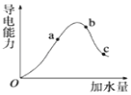
①a、b、c三点的氢离子浓度由小到大的顺序为______。
②a、b、c三点中,醋酸的电离程度最大的一点是______。
③测得某醋酸溶液中氢离子浓度为0.004mol•L﹣1,则醋酸的电离度为_____,该温度下醋酸的电离平衡常数K=_____。
高一化学填空题中等难度题查看答案及解析
-
一定条件下反应A(g)+B(g)⇌C(g)△H<0达到平衡后,据下列图象判断:
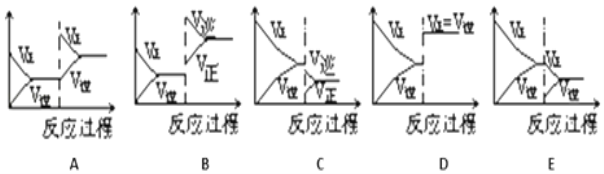
达到新的平衡对应的图象
(填写字母)
平衡移动方向
(正反应、逆反应,不移动)
(i)使用催化剂
_________
________
(ii)升温
_________
_________
(iii)降压
_________
_________
(iv)增加A的量
__________
_________
(v)减少C的量
__________
________
高一化学填空题中等难度题查看答案及解析
-
取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:

(1)原NaOH溶液的物质的量浓度为_______________。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是___,其物质的量之比为___。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况下)的最大值为____mL。
高一化学填空题中等难度题查看答案及解析
-
阅读下面科普信息,回答问题:
一个体重50 Kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有________性,下列不能实现上述转化的物质是________。
A.Cl2 B.O2
C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________性。
(4)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________性和________性,则1 mol Fe参加反应时,被还原的HNO3为__________mol,转移电子数________mol。
高一化学填空题中等难度题查看答案及解析
-
对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。比如:
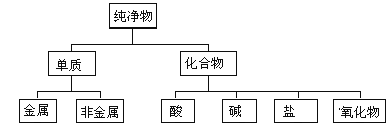
(1)上图所示的物质分类方法名称是 ;
(2)按上述分类法,下列物质中Fe、O2、H2SO4、Ba(OH)2、Ca(HCO3)2、SO2属于酸的是__________,这些物质间有的可发生化学反应,请写出一个属于置换反应的离子方程式:___________________;
人们利用分类法对化学物质和化学反应进行分类学习,例如CO2属于二元弱酸的酸性氧化物,Ca(OH)2属于强碱,已知将过量CO2缓缓通入澄清石灰水中,溶液先变浑浊,后又变澄清;NaOH也属于强碱,请写出:
少量CO2与NaOH溶液反应的离子方程式:____________________________;
过量CO2与NaOH溶液反应的离子方程式:____________________________。
高一化学填空题中等难度题查看答案及解析
-
人们应用原电池原理制作了多种电池以满足不同的需要。电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2 +2Ag+2NaCl=Na2Mn5O10 +2AgCl。
①该电池的负极反应式是______________;
②在电池中,Na + 不断移动到“水”电池的_______极(填“正“或“负”);
③外电路每通过4mol电子时,生成Na2 Mn5 O10 的物质的量是_______。
(2)中国科学院应用化学研究所在甲烷(CH4是一种可燃物)燃料电池技术方面获得新突破。甲烷燃料电池的工作原理如下图所示:

①该电池工作时,b口通入的物质为____________。
②该电池负极的电极反应式_________________________。
③工作一段时间后,当3.2 g甲烷完全反应生成CO2时,有__________NA个电子转移。
(3)Ag2O是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液时,电池放电时正极的Ag2O转化为Ag,负极的Zn转化为Zn(OH)2,写出该电池反应方程式:__________________________。
高一化学填空题中等难度题查看答案及解析
-
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
周期
IA
0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
⑧
(1)④、⑤、⑥的原子半径由大到小的顺序为_____________________(填化学式)。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:_______。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,写出其化学方程式____。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
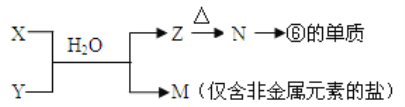
X溶液与Y溶液反应的离子方程式为_____________,N→⑥的单质的化学方程式为_____________。
高一化学填空题中等难度题查看答案及解析