-
甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________→E,确定还原产物中有二氧化氮的现象是______________________________________,实验中要多次使用装置F,第二次使用F的目的是______________________________________________。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________。
-
甲同学通过查询资料知道,一定浓度的硝酸与Mg反应时,可同时得到NO2、NO、N2三种气体。该同学欲用下列仪器组装装置来直接验证有NO2、NO生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①NO2沸点为21.1 ℃、熔点为-11 ℃,NO沸点为-151 ℃、熔点为-164 ℃;
②镁也能与CO2反应;
③氮化镁遇水剧烈水解生成Mg(OH)2和氨气。
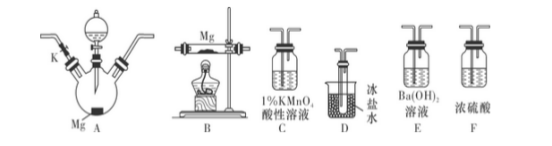
(1)实验中先打开开关K,通过导管向装置内通入CO2气体以排出装置内的空气,停止通入CO2的标志是 。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是:A→ →E,确定还原产物中有NO2的现象是 ,实验中要多次使用装置F,第二次使用F的目的是 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是 。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成 。
-
下列说法不正确的是( )
A.潮湿的氯气遇二氧化硫其漂白性减弱
B.NO中有少量的NO2,用水洗涤后再干燥
C.一氧化氮可以由氮气和氧气在放电条件下直接化合得到
D.二氧化氮能与水反应生成硝酸,所以二氧化氮是硝酸的酸酐
-
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,直至-3价。某同学取一定量铝、铁混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
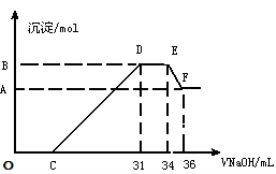
试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为________________________。
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为______________;上述CD段说明溶液中_______结合OH-的能力比_____强(填离子符号)。
(3)B与A的差值为___________mol。
(4)B点对应的沉淀的物质的量为______mol,C点对应的氢氧化钠溶液的体积为_____mL。
-
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量的铝铁合金与100mL很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4 mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
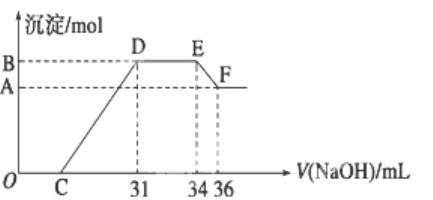
(1)结合OH-的能力最弱的是________(填离子符号)
(2)B与A的差值为________mol.
(3)原混合物中铝粉与铁粉的物质的量之比为______.
(4)B点对应的沉淀量为________mol,C点对应的溶液体积为________mL.
(5)硝酸溶液的物质的量浓度为_________mol·L-1
(6)写出铝与该浓度硝酸反应的离子方程式_____________________。
-
Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
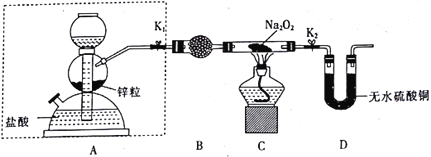
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________。
(2)B装置中所盛放的试剂是_____,其作用是_______。
(3)步骤3中的必要操作为打开K1、K2,_______(请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____(填“偏大”“偏小”或“不变”)
-
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
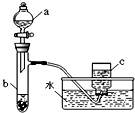
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2 g铜。
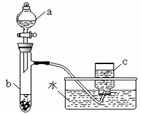
①请写出铜与稀硝酸反应的离子反应方程式________。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有________。
③仪器c中收集的气体主要是________。(填分子式)
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是________g。
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+。则
①反应结束后的溶液中NO3-的物质的量的取值范围是________。(用含a的代数式等表示)
②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+)∶n(Fe2+) 为3∶1,则b/a的值为________。
-
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。甲组同学采用如右图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4 g铜。
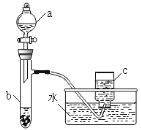
(1)仪器a的名称是_______。
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质主要有_______。
(3)仪器c中收集的气体主要是_______。(填分子式)
-
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
(1)甲组同学采用如右图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2g铜。
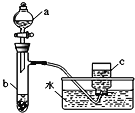
①请写出铜与稀硝酸反应的离子反应方程式_________________________________________。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有__________________________。
③仪器c中收集的气体主要是_______________________。(填分子式)
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是______g。
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+。
①反应结束后的溶液中NO3-的物质的量的取值范围是___________(用含a的代数式等表示)
②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+)∶n(Fe2+)为3∶1,则b∶a的值为______。
-
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.
(1)甲组同学采用如右图所示装置验证铜与硝酸的反应.已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2g铜.
①请写出铜与稀硝酸反应的离子反应方程式________.
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有________.
③仪器c中收集的气体主要是________.(填分子式)
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是________g.
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+.则
①反应结束后的溶液中NO3-的物质的量的取值范围是________.(用含a的代数式等表示)
②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+) 为3:1,则b:a的值为________.