-
造纸、炼焦、医药、塑料等行业的废水中常含有苯酚(C6H5OH),会对人类的生产和生活造成极大的危害。含酚废水的处理是环境科学领域的热点问题,下面介绍三项新技术。
电渗析
苯酚具有微弱的酸性,可利用电场促使C6H5O-定向移动、脱离废水,并富集回收。其电离方程式、电渗析装置示意图如下:
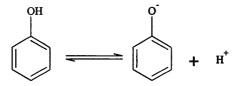
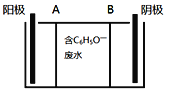
(1)为促进苯酚电离并增强溶液导电能力,可向废水中加入__________。
(2)A、B分别为离子交换膜,其中A应该是______(填“阳”或“阴”)离子交换膜。
催化重整制氢
在固定床反应器中,用含Rh催化剂使苯酚与水蒸气反应转化为氢气和二氧化碳。已知:2H2(g)+ O2(g)== 2H2O(g) ΔH1=-483.6 kJ·mol-1
C6H5OH(g)+ 7O2(g)== 6CO2(g)+ 3H2O(g) ΔH2=-2742.4 kJ·mol-1
(3)那么,反应C6H5OH(g)+ 11H2O(g)== 6CO2(g)+ 14H2(g) ΔH=_________kJ·mol-1。
活性炭纤维(ACF)物理吸附
ACF是一种活性炭纤维,不溶于水,具有多孔结构,可吸附苯酚等多种有机物质。下表是实验室里在不同温度下用0.50 g ACF吸附处理1 L苯酚溶液的相关数据。
| T / ℃ | 25 | 35 | 45 | 55 | 65 |
| 起始苯酚浓度 / mol·L-1 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 |
| 平衡苯酚浓度 / mol·L-1 | 5.00×10-4 | 6.43×10-4 | 7.85×10-4 | 9.12×10-4 | 1.13×10-3 |
(4)由表格数据可知,C6H5OH(aq) + ACF(s)  C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
(5)已知:吸附平衡常数KF= ,(其中,平衡时单位质量吸附剂对苯酚的吸附量
,(其中,平衡时单位质量吸附剂对苯酚的吸附量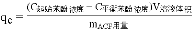 ;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
-
造纸、炼焦、医药、塑料等行业的废水中常含有苯酚(C6H5OH),会对人类的生产和生活造成极大的危害。含酚废水的处理是环境科学领域的热点问题,下面介绍三项新技术。
电渗析
苯酚具有微弱的酸性,可利用电场促使C6H5O-定向移动、脱离废水,并富集回收。其电离方程式、电渗析装置示意图如下:
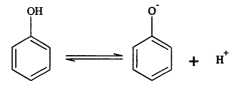
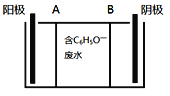
(1)为促进苯酚电离并增强溶液导电能力,可向废水中加入__________。
(2)A、B分别为离子交换膜,其中A应该是______(填“阳”或“阴”)离子交换膜。
催化重整制氢
在固定床反应器中,用含Rh催化剂使苯酚与水蒸气反应转化为氢气和二氧化碳。已知:2H2(g)+ O2(g)== 2H2O(g) ΔH1=-483.6 kJ·mol-1
C6H5OH(g)+ 7O2(g)== 6CO2(g)+ 3H2O(g) ΔH2=-2742.4 kJ·mol-1
(3)那么,反应C6H5OH(g)+ 11H2O(g)== 6CO2(g)+ 14H2(g) ΔH=_________kJ·mol-1。
活性炭纤维(ACF)物理吸附
ACF是一种活性炭纤维,不溶于水,具有多孔结构,可吸附苯酚等多种有机物质。下表是实验室里在不同温度下用0.50 g ACF吸附处理1 L苯酚溶液的相关数据。
| T / ℃ | 25 | 35 | 45 | 55 | 65 |
| 起始苯酚浓度 / mol·L-1 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 | 1.50×10-3 |
| 平衡苯酚浓度 / mol·L-1 | 5.00×10-4 | 6.43×10-4 | 7.85×10-4 | 9.12×10-4 | 1.13×10-3 |
(4)由表格数据可知,C6H5OH(aq) + ACF(s)  C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
(5)已知:吸附平衡常数KF= ,(其中,平衡时单位质量吸附剂对苯酚的吸附量
,(其中,平衡时单位质量吸附剂对苯酚的吸附量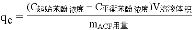 ;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
-
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大危害,必须进行处理.常用的处理方法有两种.方法1:还原沉淀法.
该法的工艺流程为: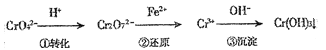
其中第①步存在平衡2CrO42−(黄色)+2H+⇌Cr2O32−(橙色)+H2O
(1)若平衡体系的 pH=2,该溶液显______色.
(2)能说明第①步反应达平衡状态的是_____(填序号)
A.Cr2O72−和CrO42−的浓度相同
B.2v(Cr2O72−)=v(CrO42−)
C.溶液的颜色不变
(3)第②步中,还原1molCr2O72−离子,需要______mol的FeSO4•7H2O.
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至______.
方法2:电解法.
该法用Fe做电极电解含Cr2O72−的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生
Cr(OH)3沉淀.
(5)用Fe做电极的原因为______(用电极反应式解释).
(6)在阴极附近溶液 pH 升高,溶液中同时生成的沉淀还有______.
-
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________(填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______(填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
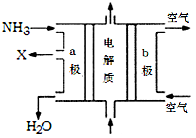
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________极(填“正”“负”“阴”或“阳”),其电极反应式为___________。
-
地球是我们赖以生存的美丽家园,人类在生产和生活中的下列活动能对环境造成污染的是 ( )。
①工业“三废”未经处理直接排放 ②植树造林,加大绿化面积 ③随意丢
弃废旧电池和塑料制品垃圾 ④生活污水的任意排放 ⑤减少空气中硫氧化
物和氮氧化物的排放,防止生成酸雨
A.①④⑤ B.②④⑤ C.①②⑤ D.①③④
-
(10分)(1)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36。请用离子方程式说明上述除杂的原理____________。
(2)工业上为了处理含有Cr2O72-的酸性工业废水, 用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原 成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为_________________________________。
②常温下,Cr(OH)3的溶度积Ksp =1×10—32 ,溶液的pH至少为 ,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78mg•L—1的废水,需用绿矾的质量为 kg。(写出计算过程,保留到小数点后一位)
-
水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重。目前,世界各国已高度重视这个问题,并采取积极措施进行治理。
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法都正确的是________(填字母编号,可多选)。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含纯碱的废水 | 加石灰水反应 | 化学法 |
(2)下图是某市污水处理的工艺流程示意图:
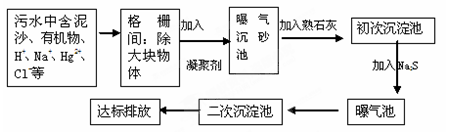
① 下列物质中不可以作为混凝剂(沉降剂)使用的是________(填字母编号,可多选)。
A.偏铝酸钠 B.氧化铝 C.碱式氯化铝 D.氯化铁
② 混凝剂除去悬浮物质的过程是________(填字母编号)。
A.只是物理过程 B. 只是化学过程 C. 是物理和化学过程
(3)在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
某厂废水中含KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应:
KCN + 2KOH + Cl2 = KOCN + 2KCl + H2O 再投入过量液氯,可将氰酸盐进一步氯化为氮气。请配平下列化学方程式:口KOCN + 口KOH + 口Cl2→口CO2 + 口N2 + 口KCl + 口H2O若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯________g。
-
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。某工厂使用还原沉淀法处理,该法的工艺流程为:

其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=12,则溶液显________色。
(2)能说明第①步反应达平衡状态的是________ 。
a.Cr2O72-的浓度不变 b.Cr2O72-和CrO42-的浓度相同
c.2v(Cr2O72-)=v(CrO42-) d.溶液的颜色不变
(3)第②步反应中,还原剂为________,该还原剂反应后生成________。
(4)电镀废液中Cr2O72-还可通过下列反应转化:
Cr2O72-(aq)+2Pb2+(aq)+H2O(l) 2 PbCrO4(s)+2H+(aq) ΔH< 0
2 PbCrO4(s)+2H+(aq) ΔH< 0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是________
-
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.某工厂使用还原沉淀法处理,该法的工艺流程为:

其中第①步存在平衡:2CrO42-(黄色)+2H+═Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=12,则溶液显________色.
(2)能说明第①步反应达平衡状态的是________.
a.Cr2O72-的浓度不变 b.Cr2O72-和CrO42-的浓度相同
c.2v(Cr2O72-)=v(CrO42-) d.溶液的颜色不变
(3)第②步反应中,还原剂为________,该还原剂反应后生成________.
(4)电镀废液中Cr2O72-还可通过下列反应转化:
Cr2O72-(aq)+2Pb2+(aq)+H2O(l)═2PbCrO4(s)+2H+(aq)△H<0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是________

-
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法是还原沉淀法。该法的工艺流程为: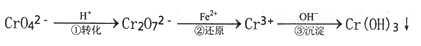
其中第①步存在平衡:2 CrO42-(黄色)+2H+ Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO4•7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s) Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。


C6H5OH·ACF(s,吸附态) ΔH_____0(填“>”或“<”)。
,(其中,平衡时单位质量吸附剂对苯酚的吸附量
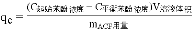 ;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。

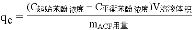 ;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。
;n为与ACF吸附能力相关的系数,25℃时n为0.5),计算25℃时KF(苯酚)=_____________________。






