-
煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g) =CO2(g)+2H2(g);△H1= 90.1kJ•mol-1
②催化液化I:CO2(g)+3H2(g)= CH3OH(g)+H2O(g) ;△H2= -49.0kJ•mol-1
③催化液化II:CO2(g)+2H2(g)=H3OH(g)+  O2(g) ;△H3= akJ•mol-1
O2(g) ;△H3= akJ•mol-1
A. 催化液化I中使用催化剂,反应的活化能Ea、△H2都减小
B. 反应C(s)+H2O(g) +H2(g)=CH3OH(g) △H= 41.1 kJ•mol-1
C. △H2>△H3
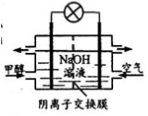
D. 右图为甲醇燃料电池的工作原理,负极的电极反应为: CH3OH-6e-+6OH-= CO2+5H2O
-
煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH1=+90.1kJ·mol—1
②催化液化I:CO2(g)+3H2(g)===CH3OH(g)+H2O(g)△H2=-49.0kJ·mol—1
③催化液化Ⅱ:CO2(g)+2H2(g)===CH3OH(g)+ O2(g)△H3=akJ·mol
O2(g)△H3=akJ·mol
A. 催化液化I的反应在高温下更容易自发进行
B. C(s)+H2O(g)+H2(g)==CH3OH(g)△H=+41.1kJ·mol—1
C. △H2>△H3
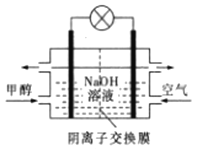
D. 如图所示为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e—+6OH—=CO2↑+5H2O
-
煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH1=+90.1kJ·mol—1
②催化液化I:CO2(g)+3H2(g)===CH3OH(g)+H2O(g)△H2=-49.0kJ·mol—1
③催化液化Ⅱ:CO2(g)+2H2(g)===CH3OH(g)+ O2(g)△H3=akJ·mol
O2(g)△H3=akJ·mol
A. 催化液化I的反应在高温下更容易自发进行
B. C(s)+H2O(g)+H2(g)==CH3OH(g)△H=+41.1kJ·mol—1
C. △H2>△H3
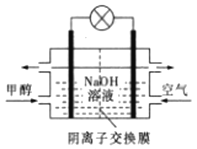
D. 如图所示为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e—+6OH—=CO2↑+5H2O
-
煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH1=+90.1kJ·mol—1
②催化液化I:CO2(g)+3H2(g)===CH3OH(g)+H2O(g)△H2=-49.0kJ·mol—1
③催化液化Ⅱ:CO2(g)+2H2(g)===CH3OH(g)+ O2(g)△H3=akJ·mol
O2(g)△H3=akJ·mol
A. 催化液化I的反应在高温下更容易自发进行
B. C(s)+H2O(g)+H2(g)==CH3OH(g)△H=+41.1kJ·mol—1
C. △H2>△H3
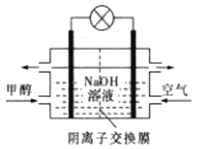
D. 如图所示为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e—+6OH—=CO2↑+5H2O
-
(14分)煤可以通过气化和液化转变为清洁能源并提高燃烧效率。
煤气化的主要反应是:C(g)+ H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
气化得到的CO和H2可以进一步液化合成甲醇,反应方程式为:
CO(g)+2H2(g) CH3OH(g) ∆H
CH3OH(g) ∆H
(1)若相同温度下CO、H2、CH3OH(g)的燃烧热(∆H)分别为a、b、c,则上述反应的∆H= 。

(2)图1表示CO的转化率与温度、压强之间的关系,图2表示CO的转化率与起始投料比n(H2)/n(CO)、温度的变化关系,曲线I、Ⅱ、Ⅲ对应的温度分别为T1、T2、T3,则T1、T2、T3的大小关系为 ,理由 。测得B(X,60)点氢气的转化率为40%,则X= 。
(3)一定条件下,将2 mol CO和4 mol H2置于容积为2 L固定的密闭容器中发生上述反应,反应达到平衡时H2的物质的量为2 mol,则此时CH3OH(g)的物质的量浓度为 ,平衡常数K= 。下列说法中能说明反应已达到平衡状态的是 (填选项前的字母)。
A.混合气体的平均摩尔质量不变
B.一氧化碳的消耗速率等于甲醇的生成速率
C.CO和H2的物质的量之比保持不变
D.混合气体的密度不变
-
“液态阳光”是指由阳光、二氧化碳和水通过人工光合得到的绿色液态燃料。下列有关“液态阳光”的说法错误的是
A. CO2和H2O转化为“液态阳光”过程中同时释放能量
B. 煤气化得到的水煤气合成的甲醇不属于“液态阳光”
C. “液态阳光”行动有利于可持续发展并应对气候变化
D. “液态阳光”有望解决全球化石燃料不断枯竭的难题
-
化学与材料、生活和环境密切相关。下列有关说法中错误的是
A. 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料
B. 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用
C. 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
D. 神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅
-
化学与材料、生活和环境密切相关。下列有关说法中错误的是
A. 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料
B. 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用
C. 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
D. 神舟10 号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅
-
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。已知制备甲醇的有关化学反应及平衡常数如下:
①CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH1=-90.8 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-90.8 kJ·mol-1
②CO(g)+H2O(g)  CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH2=-41.2 kJ·mol-1
③CO(g)+2H2(g)  CH3OH(g) ΔH3
CH3OH(g) ΔH3
850 ℃平衡常数分别为K1=160、K2=243、K3=160,甲醇可以与乙酸反应制香料C H3OH(l)+CH3COOH(l)
H3OH(l)+CH3COOH(l)  CH3COOCH3(l)+H2O(l)。
CH3COOCH3(l)+H2O(l)。
(1)则反应ΔH3=____________,制香料反应的K的表达式________________。
(2)由CO合成甲醇时,以下有关该反应的说法正确的是________(填字母)。
A.恒温、恒容条件下,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2 的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH 的产率
D.某温度下,将2 mol CO和6 mol H2 充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)850 ℃时,在密闭容器中进行反应①,开始时只加入CO2、H2,反应10 min后测得各组分的浓度如下表。比较正、逆反应的速率的大小:v正________(填“>”“<”或“=”)v逆,该时间段内反应速率v(H2)=____________________________________________________。
| 物质 | H2 | CO2 | CH3OH | H2O |
| 浓度/mol·L-1 | 0.2 | 0.2 | 0.4 | 0.4 |
(4)在一定条件下3 L恒容密闭 容器中,充入一定量的H2和CO2仅发生反应①,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线,如图1所示。
容器中,充入一定量的H2和CO2仅发生反应①,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线,如图1所示。
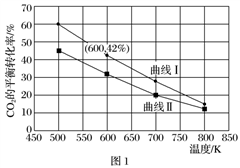
①H2和CO2的起始的投入量以A和B两种方式投入
A:n(H2)=3 mol,n(CO2)=1.5 mol,
B:n(H2)=3 mol,n(CO2)=2 mol,曲线Ⅰ代表哪种投入方式________(用A、B表示)。
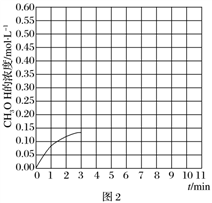
②在温度为500 K的条件下,按照A方式充入3 mol H2和1.5 mol CO2,该反应10 min时达到平衡,在此条件下,系统中CH3OH的浓度随反应时间的变化趋势如图2所示,当反应时间达到3 min时,迅速将体系温度升至600 K,请在图2中画出3~10 min内容器中CH3OH浓度的变化趋势曲线。_____________________
-
化学与材料、生活和环境密切相关。下列有关说法中错误的是
A.煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料
B.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用
C.日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
D.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅
O2(g)△H3=akJ·mol






