-
室温下向20mL含0.10mol·L-1Cr2+和0.10mol·L-1Fe2+的混合溶液中滴加0.10 mol·L -1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如图所示。若溶液中金属离子浓度小于10-5mol·L-1视为完全沉淀,则下列说法错误的是
[Cr(OH)2的ksp为2×10-16,Fe(OH)2的ksp为8×10-16]
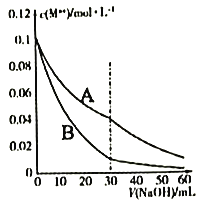
A. 曲线A表示c(Fe2+)
B. 当V(NaOH)=30mL时,Fe2+开始沉淀
C. 当pH=7时溶液中Fe2+、Cr2+均完全沉淀
D. V(NaOH)>30mL时,溶液中c(Fe2+)︰c(Cr2+) =4.0
-
室温下,用0.10 mol/L NaOH溶液分别滴定20.00 mL浓度均为0.10 mol/L的CH3COOH 溶液和HCN溶液所得滴定曲线如图所示。下列说法正确的是
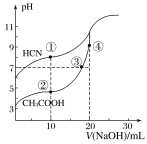
A. 室温下,电离平衡常数:K(HCN)>K(CH3COOH)
B. 点①和点②所示溶液中:c(CH3COO-)>c(CN-)
C. 点③所示的溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D. 点④所示的溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
-
室温下,用0.10 mol·L-1盐酸分别滴定20.00 mL 0.10 mol·L-1氢氧化钾溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。下列说法正确的是( )
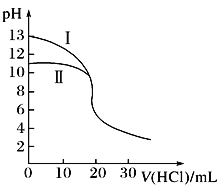
A. Ⅰ表示的是滴定氨水的曲线
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且此时溶液中c(NH4+)=c(Cl-)
C. 滴定氢氧化钾溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(H+)>c(K+)>c(OH-)
D. 当滴定氨水消耗V(HCl)=10 mL时,c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)>c(H+)
-
室温下,用0.10mol·L-1盐酸分别滴定20.00mL 0.10 mol·L-1氢氧化钾溶液和氨水,滴定过程中溶液pH随加入盐酸体积V(HCl)的变化关系如图。下列说法不正确的是( )
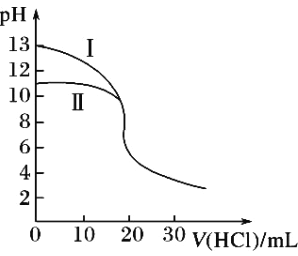
A. Ⅱ表示的是滴定氨水的曲线
B. 当pH=7时,滴定氨水消耗的V(HCl)<20mL,且此时溶液中c(NH4+)=c(Cl-)
C. 滴定氢氧化钾溶液时,若V(HCl)>20mL,则可能c(Cl-)>c(H+)>c(K+) >c(OH-)
D. 当滴定氨水消耗V(HCl)=10mL时,c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-)>c(H+)
-
室温时,将0.10 mol/L的NaOH溶液滴入20.0 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积变化曲线如图。下列有关说法不正确的是
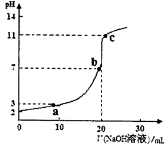
A.该一元酸溶液浓度为0.10mol/L
B.a、b、c点的水溶液导电性依次增强
C.室温时,HA的电离常数Ka l×10-5
l×10-5
D.a点和c点所示溶液中H2O的电离程度相同
-
室温下,用0.10mol/L的盐酸滴定20.00mL 0.10mol/L的某碱BOH溶液得到的滴定曲线如下,下列判断不正确的是( )

A.a点时,溶液呈碱性,溶液中c(B+)>c(Cl-)
B.b点时溶液的pH=7
C.当c(Cl-)=c(B+)时,V(HCl)<20mL
D.C点时溶液中c(H+)约为0.03mol/L
-
室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=—lgc(OH−),下列正确的是
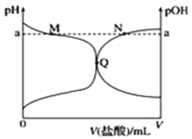
A.M 点所示溶液中可能存在:c(Cl−)>c(NH4+)
B.M 点到Q点所示溶液中水的电离程度先变大后减小
C.Q 点盐酸与氨水恰好中和
D.N 点所示溶液中可能存在:c(NH4+)+c(NH3·H2O)=c(Cl−)
-
室温下,向20.00 mL 0.10 mol·L−1一元弱碱MOH溶液中滴入0.10 mol·L−1的盐酸,溶液的AG与所加盐酸的体积关系如图所示,已知AG = lg  。
。
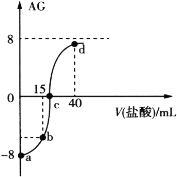
下列有关叙述不正确的是( )
A.50℃下,AG=0,此时溶液显中性
B.a点对应溶液中H2O电离出的c(H+)=1.0×10−11 mol·L−1
C.b点对应溶液中 4c(M+)+4c(MOH)=3c(Cl−)
D.d点对应溶液中c(Cl−)>c(H+)> c(M+)>c(MOH)
-
室温下,用0.10 mol·L-1盐酸分别滴定20.00 mL 0.10 mol·L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。下列说法不正确的是
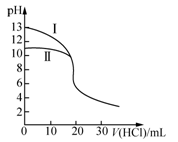
A.Ⅱ表示的是滴定氨水的曲线,当V(HCI)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-)
C.滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-)
D.当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
-
室温下,用0.10 mol·L-1盐酸分别滴定20.00 mL 0.10 mol·L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。下列说法不正确的是
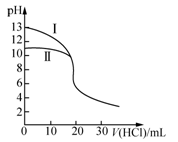
A.Ⅱ表示的是滴定氨水的曲线,当V(HCI)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-)
C.滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-)
D.当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)









