化学沉淀法可除去粗盐中的杂质离子(Ca2+、SO42-、Mg2+),下列操作不合理的是
A. 溶解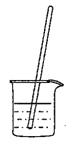 B. 沉淀反应
B. 沉淀反应
C. 过滤 D. 蒸发结晶
D. 蒸发结晶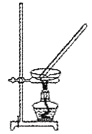
高三化学单选题中等难度题
化学沉淀法可除去粗盐中的杂质离子(Ca2+、SO42-、Mg2+),下列操作不合理的是
A. 溶解 B. 沉淀反应
B. 沉淀反应
C. 过滤 D. 蒸发结晶
D. 蒸发结晶
高三化学单选题中等难度题
化学沉淀法可除去粗盐中的杂质离子(Ca2+、SO42-、Mg2+),下列操作不合理的是
A. 溶解 B. 沉淀反应
B. 沉淀反应
C. 过滤 D. 蒸发结晶
D. 蒸发结晶
高三化学单选题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
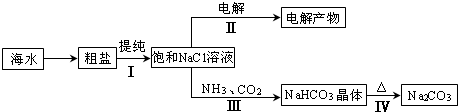
利用海水资源进行化工生产的部分工艺流程如图:

(1)流程I中,欲除去粗盐中含有的Ca2+、Mg2+、SO42-等离子,需将粗盐溶解后,按序加入药品进行沉淀、过滤等。加入药品和操作的顺序可以是________。
a.Na2CO3、NaOH、BaCl2、过滤、盐酸 b.NaOH、BaCl2、Na2CO3、过滤、盐酸
c.NaOH、Na2CO3、BaCl2、过滤、盐酸 d.BaCl2、Na2CO3、NaOH、过滤、盐酸
(2)流程II中,电解饱和NaCl溶液的离子方程式为________。通电开始后,阳极区产生的气体是________,阴极附近溶液pH会________(填“增大”、“减小”或“不变”)。
(3)流程III中,通过反应得到NaHCO3晶体。下图为NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲线,其中能表示NaHCO3溶解度曲线的是________,化学反应方程式是________。

(4)流程IV中,所得纯碱常含有少量可溶性杂质,提纯它的过程如下:将碳酸钠样品加适量水溶解、 ________、 ________、过滤、洗涤2-3次,得到纯净Na2CO3•10H2O,Na2CO3•10H2O脱水得到无水碳酸钠,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
把该过程产生的气态水完全液化释放的热能全部用于生产Na2CO3所需的能耗(不考虑能量损失),若生产1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = ________。
高三化学填空题极难题查看答案及解析
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程。下列有关说法正确的是
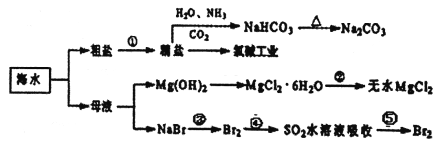
A. 制取NaHCO3的反应是利用其溶解度比较小
B. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
C. 在第③、④、⑤步骤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
高三化学null困难题查看答案及解析
(5分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获得氯化钠。将海水进行可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是_________________。(用序号填一种合理组合)。
 上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为__________,
由无水MgCl2制取Mg的化学方程式为_____________________________________。海
水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:___________________________________________________________。
高三化学填空题中等难度题查看答案及解析
氯碱工业是最基本的化学工业之一,它的产品应用广泛。请回答下列问题:
(1)氯碱工业是利用电解食盐水生产 为基础的工业体系。
(2)电解前,为除去食盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入下列试剂的顺序合理的是 (填下列各项中序号)。
a、碳酸钠、氢氧化钠、氯化钡 b、碳酸钠、氯化钡、氢氧化钠
c、氢氧化钠、碳酸钠、氯化钡 d、氯化钡、氢氧化钠、碳酸钠
(3)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
利用盐泥生产MgSO4·7H2O晶体的工艺流程如下图所示。

回答下列问题:
①酸洗过程中加入的酸为 ,加入的酸应适当过量,控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,在此过程中同时生成CaSO4。其中碳酸钙可以转化为硫酸钙的原因是 。
②过滤所得滤渣的主要成分为 。
③根据图分析,蒸发结晶过滤所得晶体A主要成分为 。

④真空干燥MgSO4·7H2O晶体的原因是 。
高三化学填空题极难题查看答案及解析
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程,下列说法正确的是
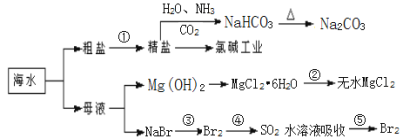
A. ①粗盐提纯中除去杂质离子Mg2+、Ca2+、SO42-时,必须先除SO42-后除Ca2+
B. 过程中②是将MgCl2·6H2O在空气中受热脱水得到无水MgCl2
C. 在③、④、⑤中,溴元素均被氧化
D. 可用澄清石灰水检验Na2CO3和NaHCO3
高三化学单选题中等难度题查看答案及解析
以下是以空气、海水中的物质为原料制取纯碱的工业流程:
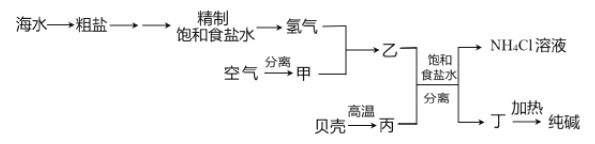
已知粗盐中含有Ca2+、Mg2+、SO42-等杂质离子。下列有关说法不正确的是
A. 除去粗盐中的杂质离子可依次加入NaOH 溶液、BaCl2 溶液、Na2CO3 溶液
B. 甲、丙分别为N2、CO2
C. 分离得到丁和NH4Cl 溶液的操作是过滤
D. 上述流程中物质转化有涉及置换反应
高三化学单选题中等难度题查看答案及解析
海水中蕴含丰富的资源,对海水进行综合利用,可制备一系列物质(见下图),下列说法正确的是
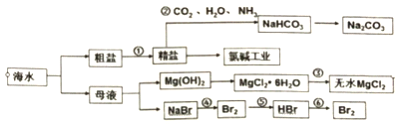
A. 步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→盐酸→过滤
B. 步骤②中反应利用的原理是:相同条件下NaHCO3的溶解度比NaCl小
C. 步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥溴元素均被氧化
高三化学选择题困难题查看答案及解析
海水是重要的资源,可以制备一系列物质。
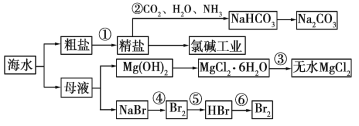
下列说法正确的是
A. 除去粗盐中 SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH 溶液→BaCl2 溶液→Na2CO3 溶液→过滤→盐酸
B. 步骤②中,应先通 CO2,再通 NH3
C. 步骤③中可将 MgCl2·6H2O 晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥反应中,溴元素均被氧化
高三化学单选题中等难度题查看答案及解析