-
非金属元素及其化合物在物质制备、生产生活中发挥着重要作用。
I.CO2与NH3合成尿素的反应如下:CO2(g)+2NH3(g) [CO(NH2)2](s)+H2O(g) △H=akJ/mol
[CO(NH2)2](s)+H2O(g) △H=akJ/mol
曲线表示不同温度、不同压强下,CO2的平衡转化率与温度的关系,请回答下列问题:
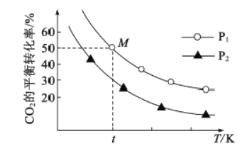
(1)a__________0,P1__________P2(填“>”、“<”或“=”)。
(2)t℃时,向容积为2L的密闭容器中充入3molNH3和1molCO2,实现M点的平衡,则
①平衡时容器内压强为开始时的____________倍,t℃时的化学平衡常数为__________。
②若保持条件不变,再向该容器中充入1molNH3和1molCO2,NH3的转化率将________(填“增大”、“减小”或“不变”)。
II.硫及其化合物在生产生活中应用广泛,回答下列问题。
(1)铁铵矾是一种化学物质,分子式为NH4Fe(SO4)2·12H2O,其溶于水后,溶液中离子浓度大小关系为________________________________。
(2)已知某溶液中含有CO32-、SO42-等离子,取一定量的该溶液向其中加入 BaCl2溶液,当CO32-开始沉淀时,溶液中 为____________。(已知:Ksp(BaSO4)=1.0×10-10,Ksp(BaSO4)=2.5×10-9)
为____________。(已知:Ksp(BaSO4)=1.0×10-10,Ksp(BaSO4)=2.5×10-9)
(3)恒温恒容密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g) △H=-197kJ/mol。下列能说明反应达到平衡状态的是___________。
2SO3(g) △H=-197kJ/mol。下列能说明反应达到平衡状态的是___________。
a.体系压强保持不变 b.混合气体的密度保持不变
c.SO3和O2的体积比保持不变 d.每消耗1molSO3的同时生成0.5molO2
-
碳和氮的许多化合物在工农业生产和生活中有着重要的作用.
(1)以CO2和NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159kJ•mol-1
②NH2CO2NH4(S)═CO(NH2)2(s)+H2O(g)△H=1165kJ•mol-1
③H2O(l)═H2O(g)△H=44.0kJ•mol-1
则反应2NH3(g)═CO(NH2)2(s)+H2O(l)的△H=______kJ•mol-1.
(2)用活性炭原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:
C(s)+2NO(g)⇌N2(g)+CO2(g)△H=QkJ•mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min)
浓度(mol/L) | | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min内,NO的平均反应速率v(NO)=______,T1℃时,该反应的平衡常数K=______;
②30min后,只改变某一条件,反应重新达到的平衡,根据上表中的数据判断改变的条件可能是______(填字母代号);
a.加入一定量的活性炭
b.通入一定量的NO
c.适当缩小容器的体积
d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中,NO、N3、CO2的浓度之比为5:3:3,则Q______0(填“>”或“<”).
-
碳和氮的许多化合物在工农业生产和生活中有重要的作用。
(1)工业上生产硝酸所需要的一氧化氮常用氨气来制备,该反应的化学方程式为 。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2 NH4(s) △H=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5 kJ·mol-1
③H2O(1)=H2O(g) △H=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(3)以氨气代替氢气研发氨燃料电池是当前科研的一个热点,已知氨燃料电池使用的电解质溶液是2mol·L-1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4g NH3转移的电子数为 (阿伏加德罗常数的值用NA表示)。
(4)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ·mol-1。
N2(g)+CO2(g) △H=Q kJ·mol-1。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(Min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号)。
a.加入一定量的活性炭 b.通人一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q 0(填“>”或“<”)。
-
氨气在生产、生活和科研中应用十分广泛 。
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47kJ/mol
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+72.49kJ/mol
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH=_____________kJmol。
②液氨可以发生电离:2NH3(l) NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式______________。
NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式______________。
(2)氨气易液化,便于储运,可利用NH3作储氢材料已知:2NH3(g) N2(g)+3H2(g) ΔH=+92.4 kJ/mol 。
N2(g)+3H2(g) ΔH=+92.4 kJ/mol 。
①氨气自发分解的反应条件是________________(填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度 的变化如图所示。
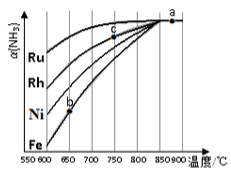
在600℃时催化效果最好的是________________(填催化剂的化学式)。c点氨气的转化率高于b点, 原因是________________。
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
①写出电解时A极的电极反应式:________________。
②写出第二步反应的化学方程式:__________________。
-
氨气在生产、生活和科研中应用十分广泛
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+ 72.49 kJ·mol-1
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH= kJ·mol-1。
②液氨可以发生电离:2NH3(l) NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
(2)氨气易液化,便于储运,可利用NH3作储氢材料
已知:2NH3(g) N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
① 氨气自发分解的反应条件是 (填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如右图所示。
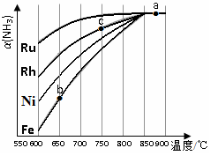
在600℃时催化效果最好的是 (填催化剂的化学式)。c点氨气的转化率高于b点,原因是 。
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
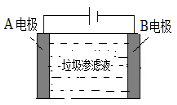
①写出电解时A极的电极反应式: 。
②写出第二步反应的化学方程式: 。
-
氨气在生产、生活和科研中应用十分广泛。
(1)以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+72kJ·mol-1
H2O(l)=H2O(g) △H=+44kJ·mol-1
则反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=______kJ·mol-1
(2)某温度下,向容积为100 ml的密闭容器中通入4molNH3和2molCO2发生反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g),物质X的浓度变化曲线如下图所示。
CO(NH2)2(s)+H2O(g),物质X的浓度变化曲线如下图所示。

①前5s内,v(H2O)=__________。
②该条件下的平衡常数K=_______。
(3)T℃时,将等物质的量的NO和CO充入体积为2L的密闭容器中,保持温度和体积不变,反应过程(0——15min)中NO的物质的量随时间的变化如图所示。
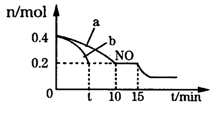
①平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将____(填“向左”“向右”或“不”)移动。
②图中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是______(填“a”或“b”)。
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是____。
(4)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入如图所示的电解池(电极为惰性材料)中进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
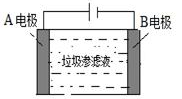
①写出第二步反应的化学方程式_________。
②若垃圾渗滤液中氨氮物质的含量为1.7%,则理论上电解1t该污水,电路中转移的电子数为________。
-
氮及其化合物与人类生产、生活息息相关。其中尿素(H2NCONH2) 是人类最早合成的有机物,工业上生产尿素的反应为: N2+3H2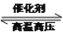 2NH3,2NH3+CO2
2NH3,2NH3+CO2 H2NCONH2+H2O。回答下列问题:
H2NCONH2+H2O。回答下列问题:
(1)纳米氧化铜、纳米氧化锌均可作合成氨的催化剂,Cu2+价层电子的轨道表达式为______,Zn位于元素周期表的_______区。
(2)C、N、O三种元素第一电离能从大到小的顺序是___________。
(3)上述化学方程式中的无机化合物,沸点由高到低的顺序是____________,原因: ___________。
(4)尿素分子中,原子杂化轨道类型有____________,σ键与π键数目之比为_______。
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1) 和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。
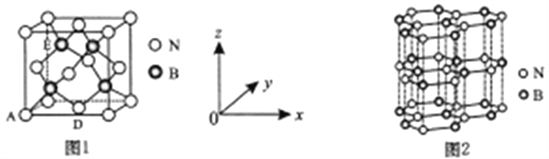
①晶胞中的原子坐标参数可表亓晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为( ),则E原子的坐标参数为_____。X-射线衍射实验测得立方氮化硼晶胞参数为361.5pm,则立方氮化硼晶体N 与B的原子半径之和为______pm。(
),则E原子的坐标参数为_____。X-射线衍射实验测得立方氮化硼晶胞参数为361.5pm,则立方氮化硼晶体N 与B的原子半径之和为______pm。( )
)
②已知六方氮化硼同层中B-N距离为acm,密度为dg/cm3,则层与层之间距离的计算表达式为_______pm。
-
尿素(H2NCONH2)是一种非常重要的高氮化肥,在工农业生产中有着非常重要的地位.
(1)工业上合成尿素的反应如下:2NH3(l)+CO2(g)⇌H2O(l)+H2NCONH2(l)△H=-103.7kJ•mol-1
下列措施中有利于提高尿素的生成速率的是______
A.采用高温 B.采用高压
C.寻找更高效的催化剂 D.减小体系内CO2浓度
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)⇌H2NCOONH4(氨基甲酸铵)(l)△H1
第二步:H2NCOONH4(l)⇌H2O(l)+H2NCONH2(l)△H2.
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和l mol二氧化碳,实验测得反应中各组分随时间的变化如下图I所示:
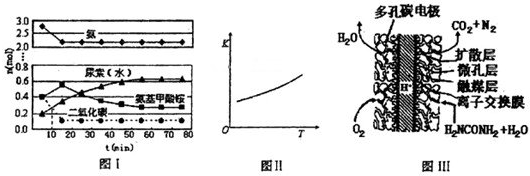
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第______步反应决定,总反应进行到______min时到达平衡.
②第二步反应的平衡常数K随温度的变化如上图II所示,则△H2______0(填“>”“<”或“=”)
(3)在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2
①尿素与NO、NO2三者等物质的量反应,化学方程式为______.
②已知:N2(g)+O2(g)═2NO(g).△H=180.6kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=______kJ•mol-1
(4)尿素燃料电池结构如上图III所示.其工作时负极电极反应式可表示为______.
-
尿素(H2NCONH2)是一种非常重要的高氮化肥,在工农业生产中有着非常重要的地位。
(1)工业上合成尿素的反应如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2(l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2(l) △H=-103.7 kJ·mol-1
下列措施中有利于提高尿素的生成速率的是________
A.采用高温
B.采用高压
C.寻找更高效的催化剂
D.减小体系内CO2浓度
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)  H2NCOONH4(氨基甲酸铵)(l) △H1
H2NCOONH4(氨基甲酸铵)(l) △H1
第二步:H2NCOONH4(l)  H2O(l)+H2NCONH2(l) △H2.
H2O(l)+H2NCONH2(l) △H2.
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和l mol二氧化碳,实验测得反应中各组分随时间的变化如下图I所示:
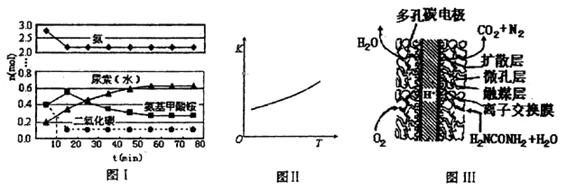
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第________步反应决定,总反应进行到________min时到达平衡。
②第二步反应的平衡常数K随温度的变化如上图II所示,则△H2 ________0(填“>” “<” 或 “=”)
(3)在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2
①尿素与NO、NO2三者等物质的量反应,化学方程式为
________
②已知:N2(g)+O2(g)=2NO(g).△H=180.6 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1
则4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g) △H=________kJ·mol-1
(4)尿素燃料电池结构如上图III所示。其工作时负极电极反应式
可表示为________ 。
-
氨气是一种重要的化工原料,在工农业中都有广泛的应用。
(1)NH3和CO2在120℃和催化剂的作用下可以合成尿素,反应方程式如下:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g)。某实验小组向一个容积不变的真空密闭容器中充入 与
与 合成尿素。在恒定温度下,混合气体中
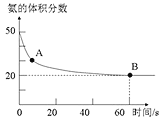
合成尿素。在恒定温度下,混合气体中 的含量随时间的变化关系如图所示
的含量随时间的变化关系如图所示 该条件下尿素为固体
该条件下尿素为固体 。A点的正反应速率
。A点的正反应速率 ______ B点的逆反应速率
______ B点的逆反应速率 填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” ,
, 的平衡转化率为______。
的平衡转化率为______。
(2)氨基甲酸铵 是合成尿素过程中的中间产物。现将体积比为2:1的
是合成尿素过程中的中间产物。现将体积比为2:1的 和
和 混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:
混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡: 。实验测得在不同温度下的平衡数据如表:
。实验测得在不同温度下的平衡数据如表:
①上述反应的焓变: ______
______ 填“
填“ ”、“
”、“ ”或“
”或“ ”,下同
”,下同 ,熵变
,熵变 ______
______ 根据表中数据,列出
根据表中数据,列出 时该反应的化学平衡常数的计算式
时该反应的化学平衡常数的计算式 ______
______ 不要求计算结果
不要求计算结果 。
。
②若从已达平衡状态的上述容器中分离出少量的氨基甲酸铵晶体,反应物的转化率将______ 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
(3)向含 的溶液中滴加bL氨水后溶液恰好呈中性,则滴加氨水的过程中水的电离平衡将______
的溶液中滴加bL氨水后溶液恰好呈中性,则滴加氨水的过程中水的电离平衡将______ 填“正向”、“不”或“逆向”
填“正向”、“不”或“逆向” 移动,所滴加氨水的浓度为______
移动,所滴加氨水的浓度为______  时,
时, 的电离平衡常数
的电离平衡常数 
[CO(NH2)2](s)+H2O(g) △H=akJ/mol

为____________。(已知:Ksp(BaSO4)=1.0×10-10,Ksp(BaSO4)=2.5×10-9)
2SO3(g) △H=-197kJ/mol。下列能说明反应达到平衡状态的是___________。






 2NH3,2NH3+CO2
2NH3,2NH3+CO2


