-
常温下,下列所述有关离子浓度之间的关系错误的是
A. 将0.2mol/L NaHCO3溶液与0.1mol/L KOH溶液等体积混合:3c(K+)+c(H+)=c(OH-) +c(HCO3-)+2c(CO32-)
B. 浓度均为0.1mol/L 的CH3COOH 与CH3COONa溶液等体积混合后pH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9) mol/L
C. 将CO2通入0.1 mol/L Na2CO3溶液至中性,溶液中2c (CO32-) +c (HCO3-)=0.1mol/L
D. 0.1 mol/L Na2CO3溶液中存在:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
高二化学单选题中等难度题查看答案及解析
-
常温下的下列溶液中,微粒浓度关系正确的是
A. 0.2 mol/L NaHCO3溶液与0.1 mol/L KOH溶液等体积混合:3c(K+) + c(H+) = c(OH-) + c(HCO3-) + 2(CO32-)
B. 只含有NH4+、Cl-、H+、OH-的溶液中,其离子浓度可能是:c(Cl-) > c(NH4+) > c(OH-) > c(H+)
C. 0.1 mol/L的NaHA溶液,其pH=4,则其中离子浓度最大与最小的差值为(0.1-10-4) mol/L
D. c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则c[(NH4)2SO4] > c[(NH4)2CO3] > c[(NH4)2Fe(SO4)2]
高二化学单选题中等难度题查看答案及解析
-
常温下,下列有关离子浓度之间的关系不正确的是( )
A.将CO2通入0.1mol/LNa2CO3溶液至中性(忽略溶液体积变化),溶液中:2c(CO32-)+c(HCO3-)=0.2mol/L
B.在0.1mol/LNaHCO3溶液中:c(H2CO3)+c(H+)=c(OH-)+c(CO42-)
C.浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后pH=5,则混合溶液中:c(Na+)>c(CH3COO-)
D.已知Ka(CH3COOH)=Kb(NH3·H2O),则常温下0.1mol/LCH3COONH4中:c(CH3COO-)=c(NH4+)
高二化学单选题中等难度题查看答案及解析
-
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是
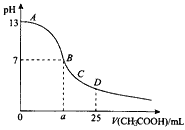
A. A、B之间任意一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C. C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
高二化学单选题中等难度题查看答案及解析
-
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是
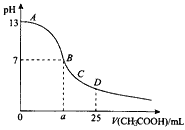
A.A、B之间任意一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
高二化学单选题中等难度题查看答案及解析
-
下列所述有关离子浓度之间的关系错误的是
A. 将CO2通入0.1mol·L-1Na2CO3溶液至中性,溶液中:2c(CO32-)+c(HCO3-)=0.1mol·L-1
B. 浓度均为0.lmol/L的CH3COOH与CH3COONa溶液等体积混合后,pH=5, 则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9) mol/L
C. 将0.2mol • L-lNaHCO3溶液与0.lmol • L-1KOH溶液等体积混合:3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. 已知常温下,Ka(CH3COOH)=Kb(NH3•H2O)=1.8×10-5,则常温下0.1 mol·L-1CH3COONH4 中:c(NH4+)=c(CH3COO-)
高二化学单选题困难题查看答案及解析
-
下列有关粒子浓度关系正确的是( )
A. 0.2mol/L的NaHCO3溶液:c(HCO3-)>c(CO32-)>0.1mol/L>c(H2CO3)
B. pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C. 0.2mol/L CH3COOH溶液和0.2mol/L CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
D. 浓度均为0.1mol/L的①NH4Cl ②NH4Al(SO4)2 ③NH4HCO3三种溶液,其中c(NH4+):③>①>②
高二化学单选题中等难度题查看答案及解析
-
常温下,下列溶液的离子浓度关系式正确的是
A.浓度相同的Na2CO3和NaHCO3混合溶液中,c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
B.0.1mol/L①醋酸②氯化铵③硫酸溶液中,水电离产生的氢离子浓度大小顺序是②>①>③
C.0.1mol/L的NaHCO3溶液中C(Na+)+c(H+)=c(OH-)+c(HCO3-)
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):③>②>①
高二化学选择题困难题查看答案及解析
-
在15mL 0.1mol•L-1KOH溶液中逐滴加入0.2mol•L-1醋酸溶液,溶液pH和加入的醋酸的体积关系曲线如图所示,有关粒子浓度大小关系正确的是 ( )
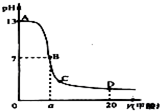
A.在A、B间任意一点:c(K+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点:c(K+)=c(CH3COO-)>c(OH-)=c(H+),且a=7.5
C.在C点:c(CH3COO-)>c(K+)>c(OH-)>c(H+)
D.在D点:c(CH3COO-)+c(CH3COOH)>2c(K+)高二化学选择题中等难度题查看答案及解析
-
常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错误的是( )
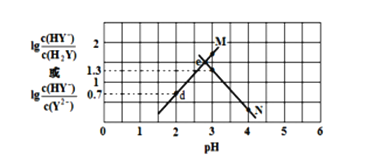
A. 曲线 M 表示 pH与lg
的变化关系
B. Ka2(H2Y)=10-4.3
C. d 点溶液中: c(H+)-c(OH -)=2c(Y2-)+ c(HY-)-c(K+)
D. 交点 e 的溶液中: c(H2Y) = c(Y2-) > c(HY-)> c(H+)> c(OH -)
高二化学单选题困难题查看答案及解析