-
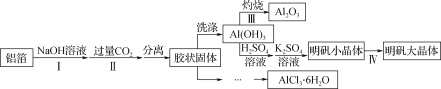
某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下:

已知:AlCl3·6H2O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
请回答:
(1)步骤Ⅰ中的化学方程式______________________________________。步骤Ⅱ中生成Al(OH)3的离子方程式________________________________________。
(2)步骤Ⅲ,下列操作合理的是______________________。
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序_______________。
①迅速降至室温 ②用玻璃棒摩擦器壁③配制90℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央⑥配制高于室温10~20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如图:
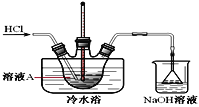
①通入HCl的作用是抑制AlCl3水解和________________。
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是____________________________;
洗涤时,合适的洗涤剂是______________________。
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是___________________。
-
某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下
已知:(1) AlCl3·6H2O易溶于水、乙醇及乙醚;
(2) 明矾在水中的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅱ中生成Al(OH)3的离子方程式为____________________________________________。
(2)步骤Ⅲ灼烧Al(OH)3所用实验室常用仪器为________,为了提高Al2O3纯度,需________(填操作步骤)。
(3)制备AlCl3·6H2O的工业生产中,胶状固体用酸浸取后,还需要通入HCl气体。通入HCl的作用主要有两点:____________和____________。
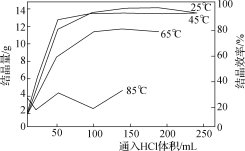
(4)已知:在不同温度条件下向一定量的氯化铝溶液中通入HCl气体,通入量对AlCl3·6H2O结晶量和结晶效率的影响如图,请补充完整由胶状固体制备AlCl3·6H2O晶体的实验方案:向胶状固体滴加一定浓度盐酸,直至恰好完全溶解,__________________________。
-
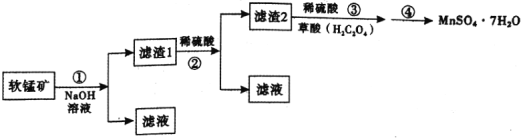
硫酸锰晶体( )是重要的微量元素肥料之一。某兴趣小组在实验室中探究用软锰矿(主要成分为
)是重要的微量元素肥料之一。某兴趣小组在实验室中探究用软锰矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 等杂质制取硫酸锰晶体,其具体流程如下:
等杂质制取硫酸锰晶体,其具体流程如下:
已知:①反应原理为: ;
;
② 难溶于水。
难溶于水。
(1)滤渣2主要成分是 ,步骤②中的稀硫酸的作用是________。
,步骤②中的稀硫酸的作用是________。
(2)步骤③中采用 硫酸和草酸晶体溶解
硫酸和草酸晶体溶解 ,草酸晶体的作用是________;配制
,草酸晶体的作用是________;配制 硫酸时,需要的仪器除量筒、烧杯、玻璃棒外,还需要________。将滤渣2置于烧杯中,先加入稀硫酸,将溶液稍加热后,在搅拌下缓慢分批加入草酸晶体,直至烧杯中的固体全部溶解。在搅拌下缓慢分批加入草酸晶体的理由是________。
硫酸时,需要的仪器除量筒、烧杯、玻璃棒外,还需要________。将滤渣2置于烧杯中,先加入稀硫酸,将溶液稍加热后,在搅拌下缓慢分批加入草酸晶体,直至烧杯中的固体全部溶解。在搅拌下缓慢分批加入草酸晶体的理由是________。
(3)步骤④的具体实验操作有________,经洗涤后干燥得到 晶体。
晶体。
(4)兴趣小组同学拟继续研究硫酸锰的高温分解的固体产物,经查资料可知:硫酸锰晶体高温下分解产物为 、
、 、
、 ,及水蒸气。为了确定
,及水蒸气。为了确定 的化学式,采用下面装置进行测定(已知:
的化学式,采用下面装置进行测定(已知: 的熔点为16.8℃,沸点为44.8℃)。
的熔点为16.8℃,沸点为44.8℃)。
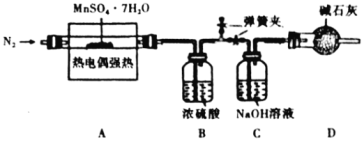
① 装置中吸收的气体为________。
装置中吸收的气体为________。
②实验自始至终均需通入 ,其目的是________。
,其目的是________。
③若起始时,在装置A中加入 ,充分反应后,测得装置C增重6.4g,则
,充分反应后,测得装置C增重6.4g,则 的化学式为________。
的化学式为________。
-
某兴趣小组用锡粒制备氯化锡 和氯化亚锡
和氯化亚锡 ,流程如下:
,流程如下:
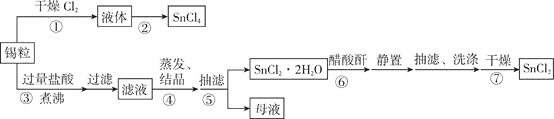
制备 的装置如图:
的装置如图:
已知: 为无色液体,熔点
为无色液体,熔点 ,沸点
,沸点 ,遇水强烈水解,可溶于乙醇、四氯化碳等。
,遇水强烈水解,可溶于乙醇、四氯化碳等。 为白色晶体,在空气中加热会发生水解及氧化。
为白色晶体,在空气中加热会发生水解及氧化。 为白色晶体,熔点
为白色晶体,熔点 ,沸点
,沸点 ,易溶于水、乙醇、冰醋酸,极易溶于盐酸。
,易溶于水、乙醇、冰醋酸,极易溶于盐酸。
请回答:
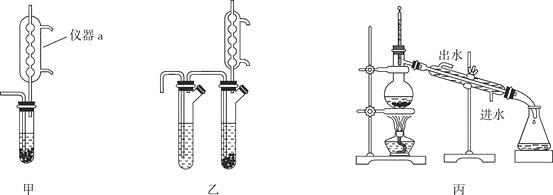
 步骤
步骤 的反应装置如图甲,其中仪器a的作用为________。若用图乙代替图甲作为反应装置,优点是在不拆除装置的情况下,向支管不断填装锡粒大量制备
的反应装置如图甲,其中仪器a的作用为________。若用图乙代替图甲作为反应装置,优点是在不拆除装置的情况下,向支管不断填装锡粒大量制备 ,则制备过程中将生成的
,则制备过程中将生成的 转移至蒸馏烧瓶中的简易操作为________。
转移至蒸馏烧瓶中的简易操作为________。
 步骤
步骤 的装置如图丙,此装置存在一处明显的缺陷为________。
的装置如图丙,此装置存在一处明显的缺陷为________。
 步骤
步骤 选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,其理由为________。
选择的实验仪器为铂皿,比用玻璃仪器或陶瓷仪器更好,其理由为________。
 步骤
步骤 中的反应需在搅拌下进行,该反应的化学方程式为________。
中的反应需在搅拌下进行,该反应的化学方程式为________。
 关于
关于 的制备,下列说法不正确的是________。
的制备,下列说法不正确的是________。
A.步骤 蒸发及步骤
蒸发及步骤 干燥时均需在真空环境下进行
干燥时均需在真空环境下进行
B.步骤 抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,应用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,以提高产率
抽滤操作中,将晶体转移至布氏漏斗时,若有晶体附着在烧杯内壁,应用蒸馏水将烧杯内壁的晶体淋洗至布氏漏斗中,以提高产率
C.为提高产品纯度,可在含醋酸酐的冰醋酸中重结晶
D. 在干燥
在干燥 或干燥HCl气流中加热也可得到无水
或干燥HCl气流中加热也可得到无水
E.若步骤 产生的母液较多,可进一步浓缩母液以提高产品纯度
产生的母液较多,可进一步浓缩母液以提高产品纯度
-
煤矸石(主要成份是SiO2和Al2O3还含有少量的Fe2O3、K2O、TiO2)活化后,可以制备六水三氯化铝(AlCl3·6H2O),工艺流程如下图所示。
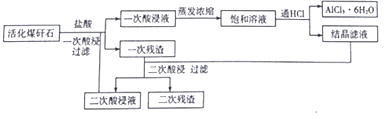
回答下列问题:
(1)焙烧至700℃左右可使煤矸石活化,活化过程中会发生一系列反应,写出SiO2与K2O反应的化学方程式______________,焙烧后的矸石颗粒有微孔,不需研磨成粉即可进行酸溶,原因是_____________。
(2)本工艺的突出特点是通过向饱和溶液中通HCl 来得到产品和对一次残渣进行二次酸浸,HCl的作用是_________________和抑制Al3+水解,二次酸浸的目的是___________________。
(3)四轮循环后所得结晶滤液中,含有较多杂质离子,必须在常温下进行如下图所示的处理
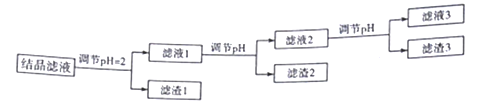
已知:Ksp(Fe(OH)3]=1.0×10-38,Ksp(Al(OH)3]=1.0×10-33,当离子浓度等于1.0×10-5mol·L-1时,可认为其已沉淀完全。
滤渣1中所含金属元素为___________,获得滤渣2时,应调节溶液的pH至少为_________,在该流程中,滤渣3 可循环使用,则生成滤渣2的离子方程式为_________________。
-
(本题共12分)六水合高氯酸铜 [Cu(C1O4)2 ·6H2O]是一种蓝色晶体,易溶于水,120℃时开始分解。实验室用硫酸铜的粗产品制备少量高氯酸铜晶体的流程如下:
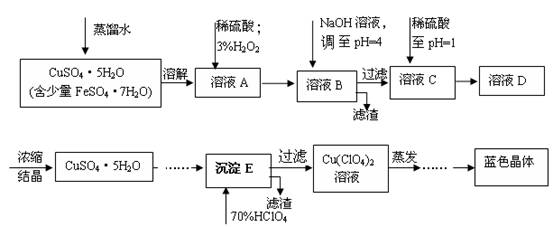
已知:
| 离子 | 溶液pH值 |
| 开始沉淀 | 沉淀完全 |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
(1).写出A→B过程中发生反应的离子方程式为________。
(2).溶液C中加入稀硫酸调至pH=1的目的是________________________________________。
(3).如欲检验溶液C中的杂质是否除净,其操作是________。
(4).蒸发至__________(填写现象),然后经过冷却结晶、过滤、洗涤、________(填写操作),得到纯净的蓝色晶体。
(5).为了测定硫酸铜的粗产品的纯度,某同学称量硫酸铜的粗产品2.000g、________、________、(填写实验步骤)过滤、洗涤沉淀、在空气中灼烧,至质量不再改变时,称得质量为0.58816 g。
(6).该样品的纯度为___________。如果样品的实际纯度为93.2%,则测定的相对误差为__________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。 某兴趣小组制备 KH2PO4,流程如下:
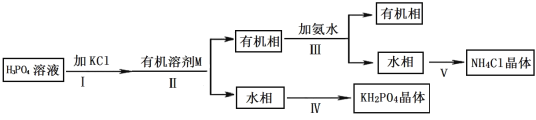
已知:
a.KH2PO4 有潮解性,溶于水,不溶于乙醇和醚等有机溶剂。
b.HCl 易溶于乙醇和醚等有机溶剂。
请回答:
(1)步骤Ⅱ的实验操作是_____。
(2)有关步骤Ⅲ,下列说法正确的是_____。
A.有机溶剂 M 可用乙醇
B.步骤Ⅲ与步骤Ⅱ的实验操作基本相同
C.NH4Cl 在水中溶解度明显大于在有机溶剂 M 中
D.有机溶剂 M 可循环使用
(3)试从平衡角度分析,由步骤Ⅰ、Ⅱ得到 KH2PO4 溶液的原理:_____。
(4)在下列仪器中,使用前需进行“检漏”操作的是_____。
A.吸滤瓶 B.球型分液漏斗 C.蒸馏烧瓶 D.碱式滴定管
(5)步骤Ⅳ,包括蒸发浓缩、冷却结晶、过滤、干燥等多步操作。在冷却结晶操作中,为了得到 磷酸二氢钾大晶体,常采取的措施有____________________。某同学发现使用加热浓缩、冷却结晶得到的磷酸二氢钾晶体欠佳,请提出针对性的改进实验方案:_____________,然后经过滤、干燥得到晶体。
-
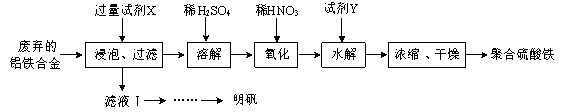
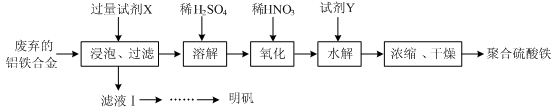
(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
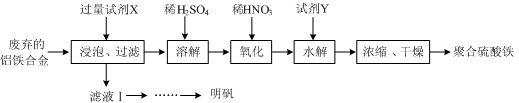
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;
浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
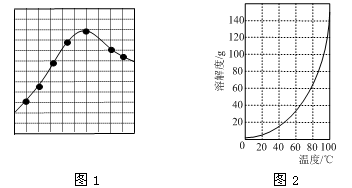
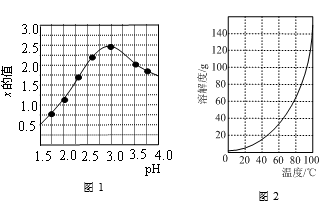
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料,试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH) x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
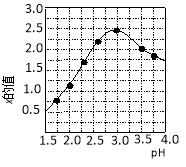
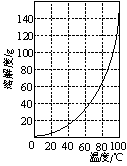
图1 图2
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
-
(15分)铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:
(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH)x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。


















