-
某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题

(1)利用上图装置研究铜与浓硫酸反应,A装置反应的化学方程式为_________________。B装置反应的化学方程式为__________________________,C装置的作用是_________________________。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是__________________。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为____________________。
验证该气体的实验方案如下:
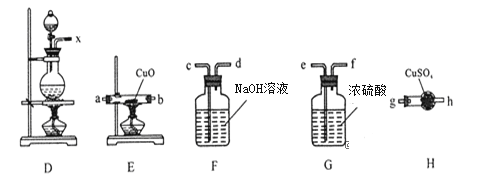
①装置连接顺序:X→ _________________________;
②能证明上述假设成立的实验现象是_____________________________________。
-
某化学小组欲进行如下实验探究金属与浓硫酸反应。试回答下列问题。
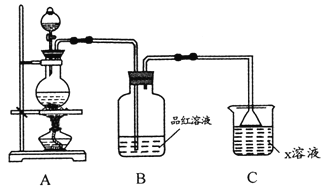
(1)利用上图装置研究铜与浓硫酸反应,反应化学方程式为_________; B装置的目的是______;x溶液为___________。
(2)将上述实验中的铜改为黄铜(铜锌合金),实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快。该气体可能为____,气体产生越来越快的原因可能是_____(答一点即可)。
验证该气体的实验方案如下:

①装置连接顺序:x→_________;
②能证明上述假设成立的实验现象是__________。
-
某化学小组欲进行如下实验探究金属与浓硫酸反应。试回答下列问题。
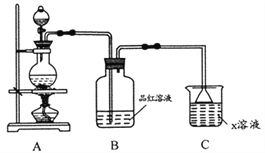
(1)利用上图装置研究铜与浓硫酸反应,反应化学方程式为_________;B装置的目的是______;x溶液为___________。
(2)将上述实验中的铜改为黄铜(铜锌合金),实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快。该气体可能为____,气体产生越来越快的原因可能是_____(至少两点)。验证该气体的实验方案如下:
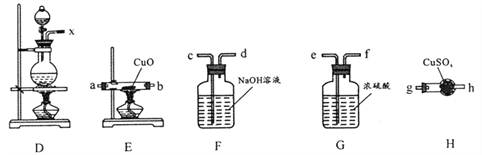
①装置连接顺序:x→_________;
②能证明上述假设成立的实验现象是__________。
(3)取少量镁粉加入盛浓硫酸的烧杯,在通风橱中实验。充分反应后溶液中有灰白色悬浮物,设计方案研究该悬浮物的组成,请帮助完善。(假设镁的化合物都溶于稀酸)
 _____
_____
写出产生该灰白色悬浮物主要反应的化学方程式_____。
-
(14分)某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
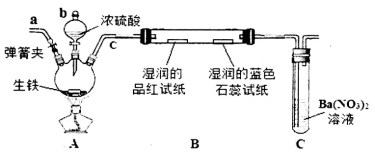
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为_____________:实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_____________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为__________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是________________________________。
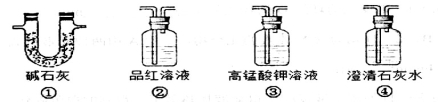
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是___________________(用离子方程式表示)。
-
(14分)某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
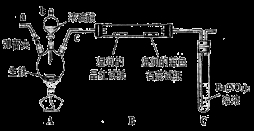
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为_____________:实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为_______________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是________________________________。

(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是_____________(用离子方程式表示)。
-
研究性学习小组利用下列有关装置进行探究实验,回答相关问题。
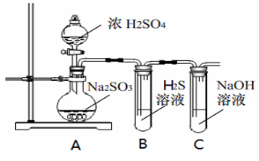
(1)写出A中的反应化学方程式
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是 。
(3)装置B中的溶液出现浑浊,该实验证明SO2具有 性 。
(4)实验后,测定装置C中溶液呈碱性。溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余。请设计实验方案证明哪种意见成立。选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
(5)另一小组利用装置D进行实验:用注射器向装置D共注入v mL实验室制备SO2的空气,当溶液刚好褪色,停止实验。
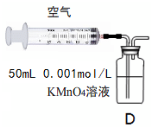
该小组的实验目的是 。
-
某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示。请回答下列问题:
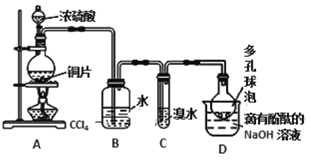
(1)装置B的作用是________________。
(2)装置C中发生反应的离子方程式是_____________________________。
SO2在装置D中完全转化为酸式酸根离子的过程中,溶液颜色变化是________。
(3)已知酸性:HCl>H2SO3>HClO。向Na2SO3溶液中加入盐酸酸化的NaClO溶液时,证明NaClO不足时的试剂是________。
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka大于其水解平衡常数Kh。______________。
-
某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如下图所示:
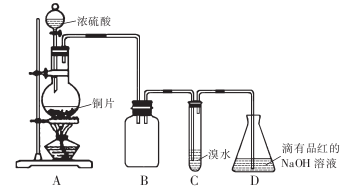
请回答下列问题:
(1)装置B的作用是________________
(2)设计装置C的目的是验证SO2的____________性,装置C中发生反应的离子方程式是____________。装置D中NaOH全部转化为NaHSO3的标志是________________。
(3)向NaHSO3溶液中加入NaCl0溶液时,反应有三种可能的情况:
I.HSO3-与ClO -恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HCl0)

(4)请设计简单实验证明:室温下HS03-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:________
-
某化学兴趣小组设计如下实验方案,将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
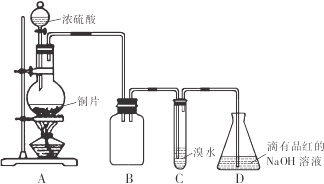
请回答下列问题:
(1)装置B的作用是______。
(2)设计装置C的目的是验证SO2的______性,装置C中发生反应的离子方程式是______装置D中NaOH全部转化为NaHSO3的标志是______。
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
| 序号 | 实验操作 | 现象 | 结论 |
| ① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
| ② | 滴加少量淀粉KI溶液,振荡 | _______ | Ⅲ |
| ③ | 滴加少量溴水,振荡 | _________ | Ⅱ |
| ④ | 滴加少量酸性KMnO4溶液、振荡 | 溶液为紫色 | ____ |
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:___。
-
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I:反应产物的定性探究
按下图装置(固定装置已略去)进行实验
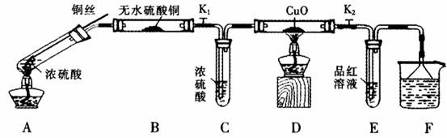
(1)A中反应的化学方程式为: 。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是_____________。
(3)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(4)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
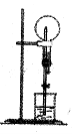
(5)某同学想用SO2气体进行喷泉实验(装置如图所示),烧杯中的溶液可以为 (填序号)
a.NaOH溶液 b.饱和NaHSO3溶液 c.氯水 d. KMnO4溶液
实验Ⅱ:反应产物的定量探究
(6)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol·L-1Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为ag,则硫酸铜的产率为 (已知:2Cu2++4I-=2CuI+I2,2S2O32-+I2=S4O62-+2I-)。






 _____
_____










