-
一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2 + 3H2  2NH3,2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是
2NH3,2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是
A.v(N2) = 0.25mol/(L·min) B.v(H2) = 0.75mol/(L·min)
C.v(NH3) = 1mol/(L·min) D.v(NH3) = 0.5mol/(L·min)
-
一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应3H2(g)+N2(g)⇌2NH3(g) ΔH=-92.4 kJ·mol-1,测得反应的相关数据如下:
| 容器1 | 容器2 | 容器3 |
| 反应温度T/K | 500 | 500 | 300 |
| 反应物投入量 | 3 mol H2、1 mol N2 | 4 mol NH3 | 2 mol NH3 |
| 平衡v正(N2)/mol·L-1·s-1 | v1 | v2 | v3 |
| 平衡c(NH3)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 达到平衡时能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 达到平衡时体积分数 | φ1(NH3) | φ2(NH3) | φ3(NH3) |
| 物质的平衡转化率α | α1(H2) | α2(NH3) | α3(NH3) |
| 平衡常数K | K1 | K2 | K3 |
下列说法正确的是( )
A. v1<v2,c2>2c1 B. K1=K2,p2>2p1
C. φ1(NH3)<φ3(NH3),a+0.5b<92.4 D. c2>2c3,α1(H2)+α3(NH3)>1
-
氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g)  2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
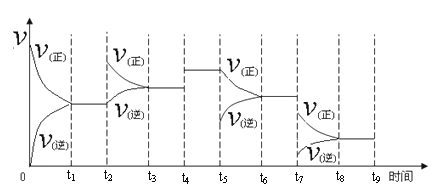
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻所对应的实验条件改变分别是
t4 ________t5 ________ t7________。
②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为________。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g)  H2(g) + CO(g) △H = +131.3 kJ/mol
H2(g) + CO(g) △H = +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是________。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度 ( )
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol碘化氢(a>b)待反应:2HI(g) H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A________c(I2)B ;平衡时HI的分解率αA________αB ;平衡时H2在混合气体中的体积分数A________B (填写“>”“<”“=”)
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A________c(I2)B ;平衡时HI的分解率αA________αB ;平衡时H2在混合气体中的体积分数A________B (填写“>”“<”“=”)
-
在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g) 2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | P1 | P2 | P3 |
| 反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A.2 c1>c3 B.a + b=92.4 C.2P1<P3 D.α1 +α3=1
-
不同温度下,三个体积均为1 L的密闭容器中发生反应3H2(g)+N2(g) 2NH3(g)ΔH =-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表。下列说法正确的是
2NH3(g)ΔH =-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表。下列说法正确的是
| 容器编号 | 温度(K) | 起始物质的量/mol | 平衡物质的量/mol |
| H2 | N2 | NH3 | H2 |
| Ⅰ | T1 | 3 | 1 | 0 | 2.4 |
| Ⅱ | T2 | 1.2 | 0.4 | 0.2 | 1.2 |
| Ⅲ | T1 | 2 | 0.2 | 0.2 | |
A. T1>T2
B. 平衡时,容器Ⅰ中反应放出的热量为92.6 kJ
C. 容器Ⅰ和容器Ⅱ中反应的化学平衡常数相同
D. 容器Ⅲ中的反应起始时向逆反应方向进行
-
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+ 3H2(g)=2NH3(g) △H=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:( )
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系 能量的变化 |
| N2 | H2 | NH3 |
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| | | | |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积变为0.5L,则平衡时放出的热量小于23.15kJ
-
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+ 3H2(g)=2NH3(g) △H=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:( )
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系 能量的变化 |
| N2 | H2 | NH3 |
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| | | | |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积变为0.5L,则平衡时放出的热量小于23.15kJ
-
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 |
| N2 | H2 | NH3 |
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是 ( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
-
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 |
| N2 | H2 | NH3 |
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
-
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应: N2(g) + 3H2(g)  2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 |
| N2 | H2 | NH3 |
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是 ( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.达平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
2NH3(g) ΔH<0,NH3的物质的量与时间的关系如表所示,下列说法错误的是( )
2NH3(g)的活化能小于2NH3(g)
N2(g)+3H2(g)的活化能
