-
一定温度下,在三个容积相同的恒容密闭容器中按不同的方式投入反应物,发生反应 N2(g)+3H2(g)
2NH3(g) △H=-92.4kJ/mol,测得反应的相关数据如下表:
容器甲
容器乙
容器丙
反应温度/℃
400
400
500
反应物投入量
1molN2,3molH2
4molNH3
1molN2,3molH2
平衡时v(正)(H2)/mol/(L·s)
v1
v2
v3
平衡时c(NH3)/(mol/L)
c1
c2
c3
平衡时总压强P/Pa
P1
P2
P3
物质的平衡转化率a
a1(N2)
a2(NH3)
a3(N2)
平衡常数K
K1
K2
K3
下列关系正确的是
A. v1<v2,c1<2c2 B. c2>2c3,a2(NH3)+a3(N2)<1
C. K1>K3, P2>2P3 D. v1<v3,a1(N2)<a3(N2)
高三化学单选题困难题查看答案及解析
-
一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应3H2(g)+N2(g)⇌2NH3(g) ΔH=-92.4 kJ·mol-1,测得反应的相关数据如下:
容器1
容器2
容器3
反应温度T/K
500
500
300
反应物投入量
3 mol H2、1 mol N2
4 mol NH3
2 mol NH3
平衡v正(N2)/mol·L-1·s-1
v1
v2
v3
平衡c(NH3)/mol·L-1
c1
c2
c3
平衡体系总压强p/Pa
p1
p2
p3
达到平衡时能量变化
放出a kJ
吸收b kJ
吸收c kJ
达到平衡时体积分数
φ1(NH3)
φ2(NH3)
φ3(NH3)
物质的平衡转化率α
α1(H2)
α2(NH3)
α3(NH3)
平衡常数K
K1
K2
K3
下列说法正确的是( )
A. v1<v2,c2>2c1 B. K1=K2,p2>2p1
C. φ1(NH3)<φ3(NH3),a+0.5b<92.4 D. c2>2c3,α1(H2)+α3(NH3)>1
高三化学多选题困难题查看答案及解析
-
在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
甲
乙
丙
反应物投入量
1molN2、3molH2
2molNH3
4molNH3
NH3的浓度(mol/L)
c1
c2
c3
反应的能量变化
放出a kJ
吸收b kJ
吸收c kJ
体系压强
P1
P2
P3
反应物转化率
α1
α2
α3
下列说法正确的是
A.2 c1>c3 B.a + b=92.4 C.2P1<P3 D.α1 +α3=1
高三化学单选题困难题查看答案及解析
-
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2+3H2
NH3
kJ·mol
)
容器
甲
乙
丙
反应物投入量
1mol N2、3mol H2
2mol NH3
4mol NH3
NH3的浓度(mol·L
)
c1
c2
c3
反应的能量变化
放出akJ
吸收bkJ
吸收ckJ
体系压强(Pa)
p1
p2
p3
反应物转化率
下列说法正确的是
A.
B.
C.
D.
+
=1
高三化学单选题困难题查看答案及解析
-
已知:N2(g)+3H2(g)
2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
容器1
容器2
反应物投入量 始态
1mol N2、3mol H2
2mol NH3
NH3的平衡浓度/mol·L-1
cl
c2
反应的能量变化
放出a kJ
吸收b kJ
体系压强/Pa
p1
p 2
反应物转化率
α1
α2
下列说法不正确的是 ( )
A. cl 一定等于c2 B.a + b = 92.4
C. p1 一定等于p2 D.α1 一定等于α2
高三化学选择题中等难度题查看答案及解析
-
已知:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法不正确的是( )容器 容器1 容器2 反应物投入量 始态 1mol N2、3mol H2 2mol NH3 NH3的平衡浓度/mol•L-1 cl c2 反应的能量变化 放出a kJ 吸收b kJ 体系压强/Pa p1 p 2 反应物转化率 α1 α2
A.cl一定等于c2
B.a+b=92.4
C.p1一定等于p2
D.α1一定等于α2高三化学选择题中等难度题查看答案及解析
-
在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g)
2NH3(g) △H=-92.4 kJ·mol-1)
容器
甲
乙
反应物投入量
1 mol N2、3 mol H2
4 mol NH3
NH3的浓度(mol·L-1)
c1
c2
反应的能量变化
放出a kJ
吸收b kJ
气体密度
ρ1
ρ2
反应物转化率
α1
α2
下列说法正确的是
A.c1<c2<2 c1 B.a+b>92.4 C.α1 +α2=1 D.ρ2=2ρ1
高三化学选择题困难题查看答案及解析
-
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:(已知N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1)
容器
甲
乙
丙
反应物的投入量
1molN2、3molH2
2molNH3
4molNH3
NH3的浓度(mol•L-1)
c1
c2
c3
反应的能量变化
放出akJ
吸收bkJ
吸收ckJ
体系的压强(Pa)
p1
p2
p3
反应物的转化率
a1
a2
a3
下列说法正确的是
A.2c1>c3 B.a+b=92.4 C.2p2<p3 D.α1+α3=1
高三化学选择题困难题查看答案及解析
-
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始浓度和起始容积相同,一定条件下发生反应:N2(g)+3H2(g)
2NH3(g) △H
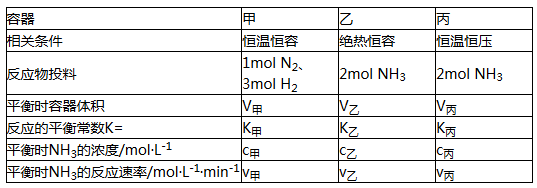
下列说法正确的是( )
A. V甲>V乙 B. K丙>K乙 C. V甲=V丙 D. c乙>c甲
高三化学选择题中等难度题查看答案及解析
-
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)
2NH3(g) ΔH=-92.4 kJ·mol-1]:
容器
甲
乙
丙
反应物投入量
1 mol N2、3 mol H2
2 mol NH3
4 mol NH3
NH3的浓度(mol·L-1)
c1
c2
c3
反应的能量变化
放出a kJ
吸收b kJ
吸收c kJ
体系压强(Pa)
p1
p2
p3
反应物转化率
α1
α2
α3
下列说法正确的是
A. 2c1>c3 B. a+b=92.4 C. 2p2<p3 D. α1+α3>1
高三化学选择题困难题查看答案及解析