以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是( )

A.石墨电极Ⅱ处的电极反应式为O2+4e-===2O2-
B.X是铁电极
C.电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D.若将电池两极所通气体互换,X、Y两极材料也互换,实验方案更合理。
高二化学单选题中等难度题
以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是( )

A.石墨电极Ⅱ处的电极反应式为O2+4e-===2O2-
B.X是铁电极
C.电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D.若将电池两极所通气体互换,X、Y两极材料也互换,实验方案更合理。
高二化学单选题中等难度题
以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是( )

A.石墨电极Ⅱ处的电极反应式为O2+4e-===2O2-
B.X是铁电极
C.电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D.若将电池两极所通气体互换,X、Y两极材料也互换,实验方案更合理。
高二化学单选题中等难度题查看答案及解析
以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2,通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是( )

A.X、Y两端都必须用铁作电极
B.不可以用NaOH溶液作为电解液
C.阴极发生的反应是:2H++2e-=H2↑
D.白色沉淀只能在阳极上产生
高二化学单选题中等难度题查看答案及解析
“以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2。通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是

A. X、Y两端都必须用铁作电极 B. 不可以用NaOH溶液作为电解液
C. 阴极发生的反应是2H2O+2e-===H2↑+2OH- D. X端为电解池的阳极
高二化学单选题困难题查看答案及解析
现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是( )
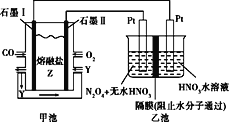
A.石墨Ⅰ是原电池的负极,发生氧化反应
B.乙池中,若使用质子交换膜,每生成1molN2O5,则有2mol H+通过交换膜进入右室
C.石墨II的电极反应式:O2+2CO2+4e-=2CO32-
D.若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol
高二化学单选题中等难度题查看答案及解析
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
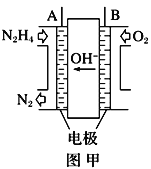
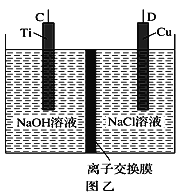
①上述装置中D电极应连接肼燃料电池的____极(填“A”或“B”),该电解池中离子交换膜为_____离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为____________
③当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(2)利用下图丙装置,可以模拟铁的电化学防护。
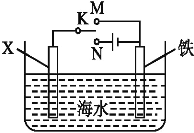
若X为碳棒,为减缓铁的腐蚀,开关K应置于_______处。若X为锌,开关K置于M处,该电化学防护法称为_________。
高二化学综合题中等难度题查看答案及解析
(1)如图1是一种新燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验。
①写出A极发生的电极反应式______________________;
②要用燃料电池为电源进行粗铜的精炼实验,则B极应该与____________极(填:“C”或“D”)相连;
③当消耗1.12L(标况下)CO时,粗铜电极理论上减少铜的质量不超过__________克。

(2)工业上,可用铁作阳极,电解KOH溶液制备K2FeO4。
①电解过程中,OH-向_________(填“阴”或“阳”)极移动,阳极的电极反应式为______________;
②若阳极有28gFe溶解,则阴极析出的气体在标准状况下的体积为___________L。
高二化学填空题困难题查看答案及解析
(16分)钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是 (用离子方程式表示)。
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:
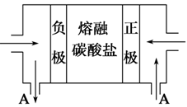
正极的电极反应式为 ,电池工作时物质A可循环使用,A物质的化学式为 。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
| 溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是 ,根据表中数据,浓度均为0.01 mol·L-1下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为 。
②已知几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”)。
高二化学填空题困难题查看答案及解析
下列用来表示物质变化的化学用语中,正确的是( )
A. 氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
B. 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe2+
C. 电解熔融NaCl,阴极的电极反应式为:2Cl﹣﹣2e﹣=Cl2↑
D. 电解饱和食盐水时,阳极的电极反应式为:2Cl﹣﹣2e﹣=Cl2↑
高二化学选择题中等难度题查看答案及解析
有一种新型的固体氧化物型燃料电池,装置如下图所示,在两极上分别通入甲烷和空气,电解质是掺杂了Y203的Zr03固体( 在高温熔融状态下能传导O2-)。下列说法正确的是( )

A. a处通入的甲烷
B. 工作时,在熔融电解质中,O2-离子移向d电极
C. c电极为正极,发生氧化反应
D. d电极的电极反应式:O2+4e-=2O2-
高二化学单选题中等难度题查看答案及解析
利用LiOH可制备锂离子电池正极材料。LiOH可由电解法制备,如右图,两极区电解质溶液分别为LiOH和LiCl溶液。下列说法错误的是
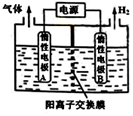
A.B极区电解质溶液为LiOH溶液
B.阳极电极反应式为2Cl--2e-=Cl2↑
C.电解过程中主要是H+通过阳离子交换膜向B电极迁移
D.电极A连接电源的正极
高二化学选择题简单题查看答案及解析