-
探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
| 实验 | 装置 | 试剂a | 现象 |
| ① | 
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4 CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4 NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2 +5
+5 +16H+
+16H+ 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
| 实验 | 装置 | 试剂a | 现象 |
| ① | 
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4 CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4 NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2 +5
+5 +16H+
+16H+ 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
| 实验 | 装置 | 试剂a | 现象 |
| ① | 
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4 CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4 NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2 +5
+5 +16H+
+16H+ 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
| 实验 | 装置 | 试剂a | 现象 |
| ① | 
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4 CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4 NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2 +5
+5 +16H+
+16H+ 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
| 实验 | 装置 | 试剂a | 现象 |
| ① | 
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
| ② | 少量NaHCO3溶液 | 产生气泡 |
| ③ | 酸性KMnO4溶液 | 紫色溶液褪色 |
| ④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4 CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4 NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2 +5
+5 +16H+
+16H+ 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
-
乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1) 室温下,测得 0.1 mol·L−1 H2C2O4溶液的pH = 1.3,写出草酸的电离方程式_______。
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如图所示:
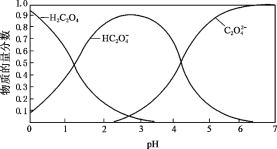
① 向草酸溶液中滴加KOH溶液至pH = 2.5时发生的主要反应的离子方程式是_______。
② 0.1 mol·L−1 KHC2O4溶液中,下列粒子浓度关系正确的是_______(填序号)。
a.c(K+) + c(H+) = c(HC2O4–) + c(C2O42–) + c(OH–)
b.c(K+) > c(HC2O4–) > c(C2O42–) > c(H2C2O4)
c.c(K+) = c(HC2O4–) + c(C2O42–) + c(H2C2O4)
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2+ + H2C2O4 + xH2O ⇌ FeC2O4·xH2O↓ + 2H+
① 制备时需添加氨水以提高FeC2O4·xH2O的产率,从化学平衡移动原理角度解释原因:_____。
② 测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定。到达滴定终点时,消耗0.1000 mol·L-1的KMnO4酸性溶液18.00 mL。已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+则FeC2O4·xH2O中x = _______(FeC2O4的摩尔质量是144 g·mol-1)。
-
乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图,下列说法正确的是
已知:①室温下,0.1 mol· L-1 H2C2O4的pH=1.3 ;0.1 mol· L-1NaHC2O4的pH=2.8
②草酸钙(Ca C2O4)难溶于水;
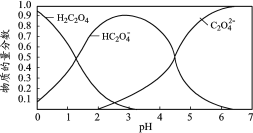
A.pH=4.5的草酸溶液中含有的大量微粒有:H2C2O4、HC2O4-、C2O42-
B.0.1 mol·L−1 NaHC2O4溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)
C.向H2C2O4溶液中加入酸性高锰酸钾溶液,紫色褪去:2MnO4-+5C2O42-+16H+=2Mn2+ +10CO2↑ +8H2O
D.向NaHC2O4溶液中加入足量澄清石灰水,产生白色沉淀:2HC2O4- +Ca2++2OH-=Ca C2O4↓ +2H2O+C2O42-
-
探究草酸(H2C2O4)的性质,室温下进行以下两组实验:(已知:室温下,H2C2O4的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5)
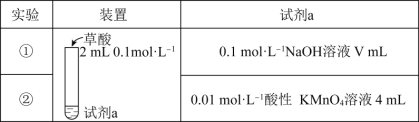
下列有关实验说法正确的是( )
A.若实验①中V=2,则混合后溶液中:c(C2O42-)>c(H2C2O4)
B.若实验①中V=4,则混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-)
C.实验②反应的离子方程式为5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O
D.若实验②测得KMnO4溶液的褪色时间为40s,则这段时间内的平均反应速率v(KMnO4)=2.5×10-4mol•L-1•s-1
-
对Na2C2O4溶液进行研究,下列说法不正确的是(室温下0.1mol· L—1H2C2O4的pH=1.3)
A.Na2C2O4溶液中离子关系:c(C2O42-)+ c(HC2O4-)+ c(H2C2O4) = c (Na+)
B.向Na2C2O4溶液中加入酚酞,溶液变红:C2O42-+H2O HC2O4-+OH-
HC2O4-+OH-
C.向Na2C2O4溶液中加入酸性高锰酸钾溶液,紫色褪去:2MnO4 -+ 5C2O42-+16 H += 2Mn 2+ +10CO2↑+8 H2O
D.向Na2C2O4溶液中加入足量稀硫酸制备草酸:C2O42-+2H+= H2 C2O4
-
室温下,向100 mL一定浓度的草酸(H2C2O4)溶液中加入0.1mol·L-1NaOH 溶液,溶液的pH随NaOH溶液体积的变化曲线如图所示。下列有关说法正确的是
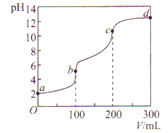
A. a点溶液的pH=2,草酸溶液的浓度为0.005 mol ·L-1
B. b点对应溶液中:c(Na+)>c(HC2O4-)>c(OH-)>c(C2O42-)
C. b→c段,反应的离子方程式为HC2O4- +OH-=C2O42-+H2O
D. c→d段,溶液中C2O42-的水解程度逐渐增强
CaC2O4↓+2H2O
NaHC2O4+CO2↑+H2O
+5
+16H+
2Mn2++10CO2↑+ 8H2O
C2H5OOCCOOC2H5+2H2O