-
(14分)二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛。
(1)①TiCl4水解生成TiO2·xH2O的化学方程式为 。
②检验TiO2·xH2O中Cl-是否被除净的方法是 。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
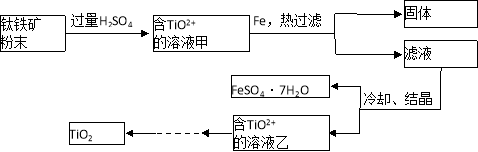
(2)Fe2O3与H2SO4反应的离子方程式是 。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有 。
(4)加Fe的作用是 。
Ⅱ、二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
TiO2 TiCl4
TiCl4 Ti
Ti
反应②的方程式是 ,该反应需要在Ar气氛中进
行,请解释原因: 。
-
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 ,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________;
② 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
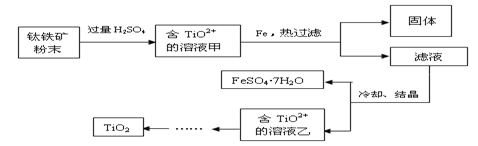
(2)Fe2O3与H2SO4反应的离子方程式是________。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有________。
(4)加Fe的作用是。
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:

反应②的方程式是________,该反应需要在Ar气氛中进行,请解释原因:_____________。
-
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。现在工业由以下两种方法制备二氧化钛:
方法1:可用含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要工艺流程如下:
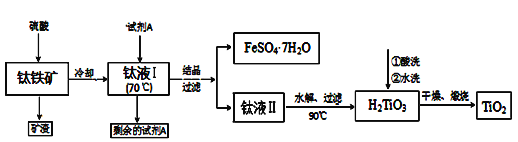
已知有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)→FeSO4(aq)+TiOSO4(aq)+2H2O(l)
水解TiOSO4(aq)+2H2O(l)→H2TiO3(s)+H2SO4(aq)
(1)试剂A为____,钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因____;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现红色,说明H2TiO3中存在的杂质离子是__________。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2会略发黄,发黄的杂质是_____________(填化学式)。
方法2:
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4;
II.将SiCl4分离,得到纯净的TiCl4;
III.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,洗涤和干燥;
IV.TiO2·xH2O高温分解得到TiO2。
(1)TiCl4水解生成TiO2•x H2O的化学方程式为____________________;
(2)检验TiO2•x H2O中Cl-是否被除净的方法是____________________;金属钛被称为“21世纪金属”,工业制备金属钛是在800~900℃及惰性气体的保护下,在密闭反应器中,将TiCl4以一定的流速通入熔化的镁即可。主要涉及以下反应:
①TiO2+2Cl2+C→TiCl4+CO2
②TiCl4+2Mg → 2MgCl2+Ti
(3)下列推断不合理的是________
A.钛在高温下可能易与氧气反应
B.镁的熔点比钛的熔点高
C.钛的金属活动性比镁的金属活动性强
D.反应②产生的MgCl2可作为电解法制取镁的原料
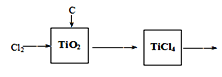
(4)请完成以TiO2、Cl2和焦炭为原料制取金属Ti和Mg的流程图,并用箭头标明物料循环。___________________
-
二氧化钛(TiO2)广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到胶体TiO2 ,此方法制备得到的是纳米二氧化钛。
(1)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________________;
②检验TiO2·x H2O中Cl-是否被除净的方法是______________________________________
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
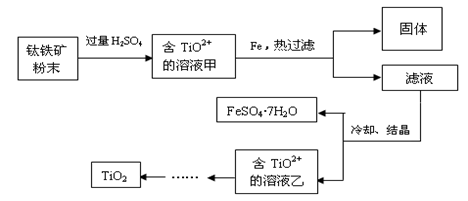
(2)钛铁矿粉末中加硫酸反应得TiO2+的离子方程式为________
(3)溶液甲中加入Fe的作用是________
(4)若要加热FeSO4.7H2O晶体得无水硫酸亚铁,除酒精灯、玻璃棒外,还要用到的两种硅酸盐质仪器是
Ⅱ二氧化钛可用于制取钛单质,涉及到的步骤如下图:
反应②的方程式是________,该反应需要在Ar气氛中进行,请解释原因:_________________
-
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(1)Fe2O3与H2SO4反应的离子方程式是_________________________________。
(2)甲溶液中除含TiO2+之外还含有的金属阳离子有__________________。
(3)加Fe的作用是_________________________________。
方法2:TiCl4水解生成TiO2·x H2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 ,此方法制备得到的是纳米二氧化钛。
(4)① TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________;
② 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:

反应②的方程式是________,该反应需要在Ar气氛中进行,请解释原因:_____________。
-
钛是继铁、铝后的第三金属,二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.用钛铁矿制取二氧化钛,(钛铁矿主要成分为FeTiO3,其中Ti元素化合价为+4价,含有Fe2O3杂质。)主要流程如下:
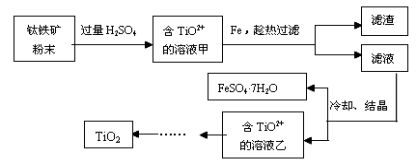
(1)Fe2O3与H2SO4反应的离子方程式_________________。
(2)加Fe的作用是______________________。
Ⅱ.由金红石(含TiO2大于96%)为原料生产钛的流程如下:
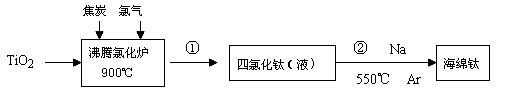
(3)反应②的方程式是 ,该反应需要在Ar气氛中进行的原因是 。
Ⅲ.科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。
(4)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氧化钙,原理如右图所示 该方法阴极获得钛的电极反应为 。
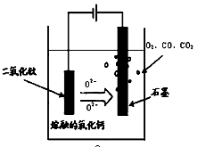
(5)阳极产生的CO2经常用氢氧化钠溶液来吸收,现有0.4mol CO2用200ml 3mol/L的NaOH溶液将其完全吸收,溶液中的离子浓度由大到小的顺序为 。
-
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·xH2O的化学方程式为_______________________________。
⑵检验TiO2·xH2O中Cl-是否被除净的方法是______________________________。
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。





a b c d e
⑸滴定终点的现象是___________________________________________________。
⑹滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
-
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用.制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.用氧化还原滴定法测定TiO2的质量分数操作如下:首先在一定条件下,把TiO2溶解并转化为Ti3+,再用NH4Fe(SO4)2标准溶液滴定Ti3+至全部转化成Ti4+.
请回答下列问题:
(1)TiCl4水解生成TiO2•xH2O的化学方程式为________.
(2)检验TiO2•xH2O中Cl-是否被除净的方法是________.
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是________;配制溶液使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要如图中的________(填字母代号).
(4)该滴定操作所用到的指示剂是________,滴定终点的现象是________
(5)滴定分析时,称取TiO2试样w g,消耗c mol•L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为________.

-
三氯化钌广泛应用于氯碱工业中金属阳极钌涂层及加氢催化剂。现以固体含Ru废料为原料制备RuCl3晶体,其工艺流程如下:
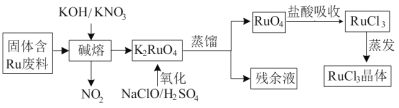
回答下列问题:
(1)K2RuO4中Ru的化合价为_____,“碱熔”中产生的气体可用于____(写一种工业用途)。
(2)“氧化”时欲使2mol K2RuO4氧化为RuO4,则需要氧化剂的物质的量为______mol。
(3)为了提高“碱熔”效率,可以采取的措施有______。
(4)RuO4气体有剧毒,“盐酸吸收”时的化学方程式为___________。
(5)可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2 = 2Ru+6HCl,所得实验数据记录如下:
| 实验序号 | 产品质量/g | 固体Ru质量/g |
| ① | 5.1875 | 2.0210 |
| ② | 5.1875 | 2.0190 |
| ③ | 5.1875 | 2.0200 |
| ④ | 5.1875 | 1.6200 |
则产品的纯度为________(用百分数表示)。
(6)钌及其化合物在合成工业上有广泛用途,根据图示写出合成反应的化学方程式________。
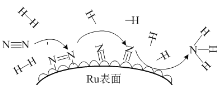
-
水合肼 是重要的化工原料,广泛地应用于医药、农药、染料等。其在工业上常利用尿素氧化法制备,反应原理为
是重要的化工原料,广泛地应用于医药、农药、染料等。其在工业上常利用尿素氧化法制备,反应原理为 。某同学在实验室模仿工业制备方法制备
。某同学在实验室模仿工业制备方法制备 。回答下列问题:
。回答下列问题:
(1) 溶液的制备,装置如图所示。
溶液的制备,装置如图所示。
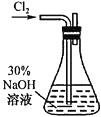
①实验室利用二氧化锰和浓盐酸制备氯气的离子方程式为_________________。
②实验需要用到 的NaOH溶液,配制该溶液所需玻璃仪器除量筒外还有_____。
的NaOH溶液,配制该溶液所需玻璃仪器除量筒外还有_____。
③锥形瓶中发生反应的化学方程式为___________________________。
④因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液中NaOH的浓度。利用所提供试剂,设计实验方案:____________________________所提供的试剂有: 溶液、
溶液、 溶液、
溶液、 的盐酸、酚酞试液。
的盐酸、酚酞试液。
(2)水合肼的制备,装置如图所示。
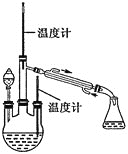
实验步骤:控制反应温度 加热装置已省略
加热装置已省略 ,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应后,持续加热蒸馏三颈烧瓶内的溶液,收集
,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应后,持续加热蒸馏三颈烧瓶内的溶液,收集 馏分于锥形瓶中。已知
馏分于锥形瓶中。已知 。分液漏斗中的溶液是_________
。分液漏斗中的溶液是_________ 填“
填“ 溶液”或“NaOH和NaClO混合溶液”
溶液”或“NaOH和NaClO混合溶液” ,选择的理由是___________。
,选择的理由是___________。
(3)馏分中水合肼含量的测定。
称取馏分 ,加入适量的
,加入适量的 固体
固体 滴定过程中,控制溶液的pH保持在
滴定过程中,控制溶液的pH保持在 左右
左右 ,加水配成
,加水配成 溶液,移出
溶液,移出 ,用
,用 的
的 溶液滴定。实验测得消耗
溶液滴定。实验测得消耗 溶液的平均值为
溶液的平均值为 ,馏分中水合肼
,馏分中水合肼 的质量分数为_____。
的质量分数为_____。 已知:
已知:

TiCl4
Ti












