-
以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O。已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离【解析】
SO2(l)+SO2(l) SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )
SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )
A.该滴定反应可以表示为:SO32-+ SO2+=2SO2
B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C.自离解的存在,说明SO2是离子化合物
D.可通过导电能力变化来判断是否到达滴定终点
-
以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O。已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离【解析】
SO2(l)+SO2(l)  SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是( )
SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是( )
A.该滴定反应可以表示为:SO32-+SO2+=2SO2
B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C.自离解的存在,说明SO2是离子化合物
D.可通过导电能力变化来判断是否到达滴定终点
-
以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O.已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离【解析】
SO2(l)+SO2(l)⇌SO32-+SO2+.若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是( )
A.该滴定反应可以表示为:SO32-+SO2+=2SO2
B.在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C.自离解的存在,说明SO2是离子化合物
D.可通过导电能力变化来判断是否到达滴定终点
-
实验表明,相同温度下,液态纯硫酸的导电性强于纯水。已知液态电解质都能像水那样自身电离而建立电离平衡(如H2O+H2O H3O++OH-),且在一定温度下都有各自的离子积常数。25 ℃时,纯硫酸的离子积常数K和水的离子积常数Kw关系为( )
H3O++OH-),且在一定温度下都有各自的离子积常数。25 ℃时,纯硫酸的离子积常数K和水的离子积常数Kw关系为( )
A. K>Kw B. K=Kw C. K<Kw D. 无法比较
-
下列实验操作或原理正确的是( )
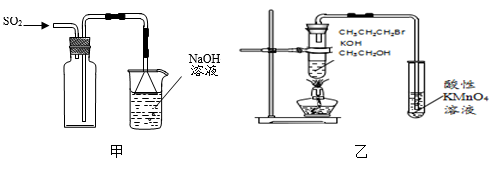
A.用装置甲收集SO2气体
B.用装置乙验证1-溴丙烷发生消去反应是否生成烯烃
C.酸碱中和滴定过程中,眼睛必须注视滴定管 刻度的变化
刻度的变化
D.配制溶液定容时,俯视容量瓶刻度会使所配溶液的浓度偏高
-
下列叙述中因果关系成立的是( )
A.因为氨水可以导电,所以NH3是电解质
B.因为SO2可以使溴水褪色,所以SO2具有漂白性
C.因为加热后纯水的pH<7,所以升温可使水呈酸性
D.因为电解质溶于水后发生电离,所以电解质在溶液中的反应实质是离子间的反应
-
下列叙述中因果关系成立的是
A.因为NH3的水溶液可以导电,所以NH3是电解质
B.因为SO2可以使溴水褪色,所以SO2具有漂白性
C.因为加热后纯水的pH<7,所以升温可使水呈酸性
D.因为电解质溶于水后发生电离,所以电解质在溶液中的反应实质是离子间的反应
-
下列叙述中因果关系成立的是
A.因为NH3的水溶液可以导电,所以NH3是电解质
B.因为SO2可以使溴水褪色,所以SO2具有漂白性
C.因为加热后纯水的pH<7,所以升温可使水呈酸性
D.因为电解质溶于水后发生电离,所以电解质在溶液中的反应实质是离子间的反应
-
下列有关实验原理或操作正确的是
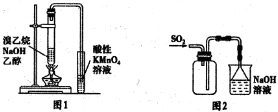
A.用图1所示装置检验有乙烯生成
B.用图2所示装置收集SO2
C.室温下,向苯和苯酚的混合溶液中加入浓溴水,充分反应后过滤,以除去苯中少量的苯酚
D.酸碱中和滴定前,滴定管用蒸馏水洗涤后用待装溶液润洗
-
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定中和滴定的终点。某化学小组同学利用该原理在常温时,分别测定NaOH溶液和氨水的物质的量浓度,并得到如图所示曲线。
①待测溶液:100 mL氨水、100 mL NaOH溶液 ②标准溶液:0.40 的盐酸。
的盐酸。
 下列说法错误的是( )
下列说法错误的是( )
A.滴定NaOH溶液时,所得的曲线是b
B.达到滴定终点时,N点溶液的pH<7,M点溶液的pH=7
C.氨水溶液的物质的量浓度为0.10
D. NaOH溶液的pH=13
SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )


 下列说法错误的是( )
下列说法错误的是( )