绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
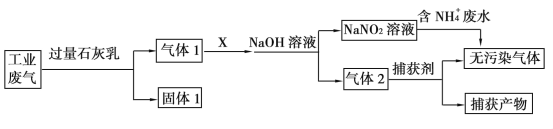
已知:NO+NO2+2OH-=2NO2-+H2O
下列说法正确的是
A.固体1中主要含有CaCO3、CaSO4
B.X可以是空气,且需过量
C.处理含NH4+废水时,发生的反应为:NH4++5NO2-+4H+=6NO+4H2O
D.捕获剂所捕获的气体主要是CO
高三化学单选题中等难度题
绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

已知:NO+NO2+2OH-=2NO2-+H2O
下列说法正确的是
A.固体1中主要含有CaCO3、CaSO4
B.X可以是空气,且需过量
C.处理含NH4+废水时,发生的反应为:NH4++5NO2-+4H+=6NO+4H2O
D.捕获剂所捕获的气体主要是CO
高三化学单选题中等难度题
绿水青山是习近平总书记构建美丽中国的伟大构想,可用化学实现“化废为宝”。工业上利用废铁屑(含少量氧化铝、铁的氧化物等)生产碱式硫酸铁 (是一种用于污水处理的新型高效絮凝剂)工艺流程如下:
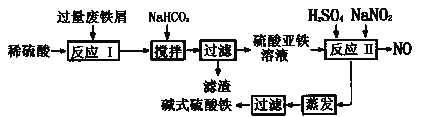
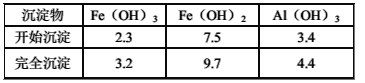
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)用稀硫酸浸废铁屑后溶液中主要的金属阳离子有______________。
(2)写出酸浸过程中Fe3O4发生的离子反应方程式:___________________________。
(3)加入少量NaHCO3的目的是调节pH在________________范围内。
(4)已知室温下,Al(OH)3 的Ksp=1.3×10-33,在pH=5时,溶液中的c(Al3+)=________。
(5)反应Ⅱ中入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为 _____。
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为__________________________。
(7)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00 mL溶液于带 塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应后, 再用0.1000 mol·L-1Na2S2O3 标准溶液滴定至终点,消耗标准溶液20.00 mL。已知:2Fe3++2I-=2Fe3++I2,I2+2S2O32-=2I-+S4O62-则溶液中铁元素的总含量为__________g·L-1。
高三化学综合题中等难度题查看答案及解析
绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
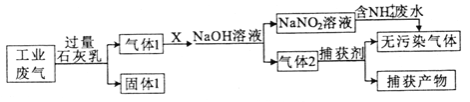
下列说法正确的是
A. 固体1中主要含有CaCO3、CaSO3
B. X可以是空气,且需过量
C. 捕获剂所捕获的气体主要是CO
D. 处理含NH4+废水时,发生的反应为:NH4++5NO2-+4H+=6NO↑+4H2O
高三化学单选题中等难度题查看答案及解析
绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

已知:NO+NO2+2OH-=2NO2-+H2O
下列说法正确的是
A.固体1中主要含有CaCO3、CaSO4
B.X可以是空气,且需过量
C.处理含NH4+废水时,发生的反应为:NH4++5NO2-+4H+=6NO+4H2O
D.捕获剂所捕获的气体主要是CO
高三化学单选题中等难度题查看答案及解析
绿水青山是习总书记构建美丽中国的伟大设想,研究碳、氮、硫等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)科学家研究利用某种催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g) 2NO(g) △H1=+179.5 kJ·mol-1
②NO2(g)+CO(g) NO(g)+CO2(g) △H2=-234 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) △H3=-112.3 kJ·mol-1
则反应2NO(g)+2CO(g) N2(g)+2CO2(g)的△H=__________kJ·mol-1;某温度下,反应①②③的平衡常数分别为K1、K2、K3,则该反应的K=__________用K1、K2、K3表示)
(2)用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图所示
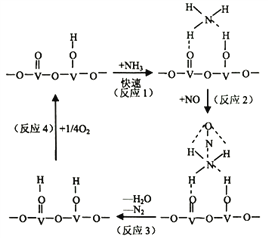
①写出总反应化学方程式__________________________________。
②测得该反应的平衡常数与温度的关系为:1gK=5.08+217.5/T,该反应是____________反应(填“吸热”或“放热”)。
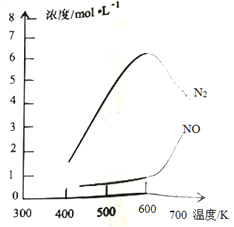
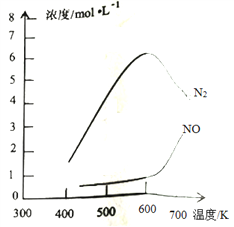
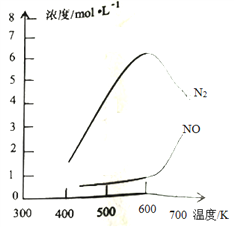
③该反应的含氮气体浓度随温度变化如图所示,则将NO转化为N2的最佳温度为____________;当温度达到700K时,发生副反应的化学方程式________________________。
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
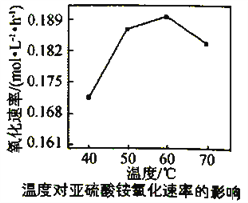
试解释在温度较高时,(NH4)2SO3 氧化速率下降的原因是________________________;相同条件下,等浓度的(NH4)2SO3和(NH4)2SO4溶液中,c(NH4+)前者____________(填“大”小”)
高三化学综合题困难题查看答案及解析
绿水青山是习总书记构建美丽中国的伟大设想,研究碳、氮、硫等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)科学家研究利用某种催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g) 2NO(g) △H1=+179.5 kJ·mol-1
②NO2(g)+CO(g) NO(g)+CO2(g) △H2=-234 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) △H3=-112.3 kJ·mol-1
则反应2NO(g)+2CO(g) N2(g)+2CO2(g)的△H=__________kJ·mol-1;某温度下,反应①②③的平衡常数分别为K1、K2、K3,则该反应的K=__________用K1、K2、K3表示)
(2)用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图所示
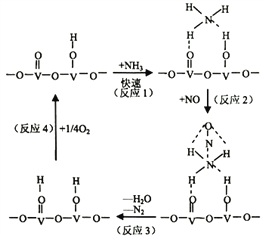
①写出总反应化学方程式__________________________________。
②测得该反应的平衡常数与温度的关系为:1gK=5.08+217.5/T,该反应是____________反应(填“吸热”或“放热”)。
③该反应的含氮气体浓度随温度变化如图所示,则将NO转化为N2的最佳温度为____________;当温度达到700K时,发生副反应的化学方程式________________________。
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
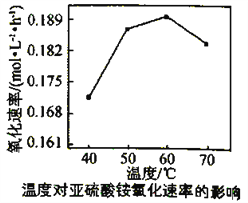
试解释在温度较高时,(NH4)2SO3 氧化速率下降的原因是________________________;相同条件下,等浓度的(NH4)2SO3和(NH4)2SO4溶液中,c(NH4+)前者____________(填“大”小”)
高三化学综合题困难题查看答案及解析
绿水青山是习总书记构建美丽中国的伟大设想,研究碳、氮、硫等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)科学家研究利用某种催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g) 2NO(g) △H1=+179.5 kJ·mol-1
②NO2(g)+CO(g) NO(g)+CO2(g) △H2=-234 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) △H3=-112.3 kJ·mol-1
则反应2NO(g)+2CO(g) N2(g)+2CO2(g)的△H=__________kJ·mol-1;某温度下,反应①②③的平衡常数分别为K1、K2、K3,则该反应的K=__________用K1、K2、K3表示)
(2)用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图所示
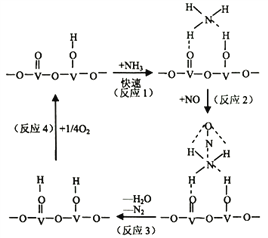
①写出总反应化学方程式__________________________________。
②测得该反应的平衡常数与温度的关系为:1gK=5.08+217.5/T,该反应是____________反应(填“吸热”或“放热”)。
③该反应的含氮气体浓度随温度变化如图所示,则将NO转化为N2的最佳温度为____________;当温度达到700K时,发生副反应的化学方程式________________________。
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
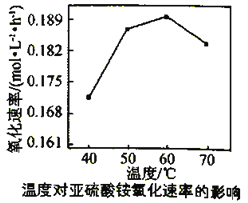
试解释在温度较高时,(NH4)2SO3 氧化速率下降的原因是________________________;相同条件下,等浓度的(NH4)2SO3和(NH4)2SO4溶液中,c(NH4+)前者____________(填“大”小”)
高三化学综合题困难题查看答案及解析
(14分)碱式硫酸铁[Fe(OH)SO4]可用作净水剂、媒染剂、颜料和药物。工业上利用废铁屑(含少量氧化铝、氧化铁等),生产碱式硫酸铁的部分工艺如下:
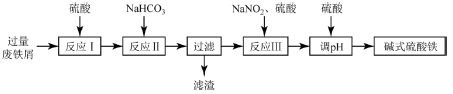
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

(1)反应I中发生的氧化还原反应的离子方程式是__________。
(2)反应II中加入NaHCO3调节体系的pH在____范围内。
(3)反应III中生成的气体遇空气变红棕色,则III中发生反应的离子方程式是_________ 。
(4)反应III中通入氧气可减少NaNO2的用量,若消耗1mol氧气可节约n(NaNO2)=____mol。
(5)用硫酸可知体系的pH。若硫酸加入量过小,溶液生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理分析其原因是_________。
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可发生水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式是____________。
高三化学实验题困难题查看答案及解析
碱式硫酸铁[Fe(OH)SO4]可用做净水剂、媒染剂等。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的部分工艺如下:
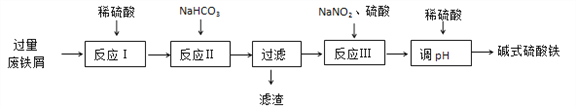
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应Ⅰ中氧化还原反应的离子方程式__________________ 、 ___________________。
(2)反应Ⅱ中加入NaHCO3调节体系的pH在_____________范围内。
(3)反应Ⅲ中生成的气体遇空气变红棕色,该反应的离子方程式是_____________________。
(4)若反应Ⅲ中通入O2可减少NaNO2的用量,当消耗1molO2可节约n(NaNO2)=_____mol。
(5)用稀硫酸调节体系的pH时,若硫酸加入量过少,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理说明其原因______________________________。
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为____________________________
高三化学综合题中等难度题查看答案及解析
碱式硫酸铁[Fe(OH)SO4]可用做净水剂、媒染剂等。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的部分工艺如下:
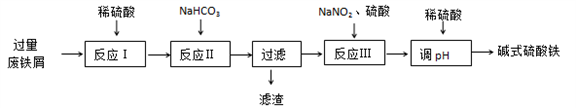
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应Ⅰ中氧化还原反应的离子方程式__________________ 、 ___________________。
(2)反应Ⅱ中加入NaHCO3调节体系的pH在_____________范围内。
(3)反应Ⅲ中生成的气体遇空气变红棕色,该反应的离子方程式是_____________________。
(4)若反应Ⅲ中通入O2可减少NaNO2的用量,当消耗1molO2可节约n(NaNO2)=_____mol。
(5)用稀硫酸调节体系的pH时,若硫酸加入量过少,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理说明其原因______________________________。
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为____________________________
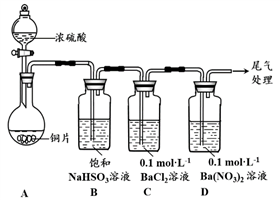
高三化学简答题困难题查看答案及解析
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]工艺流程如下:
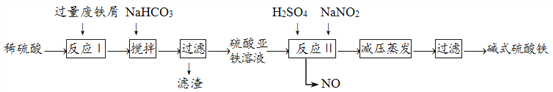
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)反应I溶液中存在的金属阳离子有___________________________。
(2)加入少量NaHCO3的目的是调节pH,使溶液中的________(填“Fe3+”、“Fe2+”或“Al3+”)沉淀。该工艺流程中“搅拌”的作用是______________________。
(3)反应Ⅱ的离子方程式为 ____________________________。在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作______________。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42-聚合离子。该水解反应的离子方程式为____________________________。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A. 氯水 B. KSCN溶液 C. NaOH溶液 D. 酸性KMnO4溶液
高三化学简答题困难题查看答案及解析