生物固氮与模拟生物固氮都是重大基础性研究课题。大连理工大学曲景平教授团队设计合成了一类新型邻苯二硫酚桥联双核铁配合物,建立了双铁分子仿生化学固氮新的功能分子模型。如图是所发论文插图。以下说法错误的是
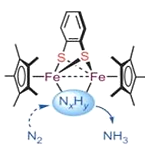
A.催化剂不能改变反应的焓变
B.催化剂不能改变反应的活化能
C.图中反应中间体NXHY数值X<3
D.图示催化剂分子中包含配位键
高三化学单选题中等难度题
生物固氮与模拟生物固氮都是重大基础性研究课题。大连理工大学曲景平教授团队设计合成了一类新型邻苯二硫酚桥联双核铁配合物,建立了双铁分子仿生化学固氮新的功能分子模型。如图是所发论文插图。以下说法错误的是

A.催化剂不能改变反应的焓变
B.催化剂不能改变反应的活化能
C.图中反应中间体NXHY数值X<3
D.图示催化剂分子中包含配位键
高三化学单选题中等难度题
生物固氮与模拟生物固氮都是重大基础性研究课题。大连理工大学曲景平教授团队设计合成了一类新型邻苯二硫酚桥联双核铁配合物,建立了双铁分子仿生化学固氮新的功能分子模型。如图是所发论文插图。以下说法错误的是

A.催化剂不能改变反应的焓变
B.催化剂不能改变反应的活化能
C.图中反应中间体NXHY数值X<3
D.图示催化剂分子中包含配位键
高三化学单选题中等难度题查看答案及解析
CO2的固定和转化是世界性课题。兰州大学景欢旺教授团队巧妙设计构建了系列新型光电催化人工光合成体系——光电催化池,p-n半导体异质结催化CO2在水中直接制备长碳链有机物并放出氧气,原理如图,下列说法不正确的是
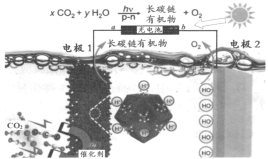
A.电极1的电势比电极2的电势高
B.该设计向大自然学习,模仿植物的光合作用
C.电子从a极流到电极1,从电极2流到b极
D.负极区,p-n为催化剂,CO2发生还原反应生成长碳链有机物
高三化学单选题中等难度题查看答案及解析
2018年3月南开大学教授叶萌春及其团队借助廉价金属镍和苯基硼酸共催化的烯基化反应,首次实现烯丙醇高效、绿色合成重大突破。成果也在最新一期《德国应用化学》上发表。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的价电子排布式为___________________。
(2)1 mol CH2=CH-CH2OH含____molσ键,烯丙醇分子中碳原子的杂化类型为____。
(3)丙醛(CHCH2CHO)的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是_______________________________。
(4)羰基镍[Ni(CO)4)用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是_________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2-和[Ni(SCN)2]-等。NH3的空间构型是_____________。
(6)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙中。
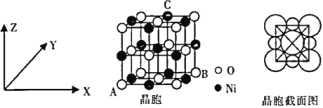
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为____________。
②已知:氧化镍晶胞密度为dg·cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为__________nm(用代数式表示)。
高三化学综合题中等难度题查看答案及解析
【化学-选修3:物质结构与性质】
南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破。请根据材料回答以下问题:
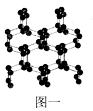
(1)N、O、F三种元素的第一电离能由大到小的顺序为____(填元素符号);与N2互为等电子体的全氧离子化学式为_______;具有空间网状结构的高聚氮结构如图一所示,则N70的沸点_____(填“>”、“<”或“=”)高聚氮的沸点,原因是_________________;N70和高聚氮属于_____(选填序号)。
A.同素异形体 B.同分异构体 C.同位素 D.同系物
(2)叠氮化物是研究较早的含全氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3) 等。叠氮化物能形成多种配合物,在[Co(N3)(NH3)5]SO4,其中钴显____价,它的配体是____,SO42-的立体构型为___________。
(3)HN3是一种全氮阴离子酸,可由肼(N2H4)被HNO2氧化制得。下列说法正确的是____。
A.酸性:HNO2>HNO2
B. N2H4分子中N原子均采取sp3杂化
C. NaN3的晶格能小于KN3的晶格能
D.上述生成氢叠氮酸的化学方程式为N2H4+HNO2=2H2O+HN3
(4)N8是一种由全氮阳离子和全氮阴离子构成的特殊物质,已知阳离子由5个氮原子排列成V 形,每个氮原子均达到八电子稳定结构,则阳离子的电子式为_______。
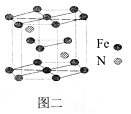
(5)一种氮铁化合物的结构如图二所示,若图中六棱柱的体积为Vcm3, 用NA表示阿伏加德罗常数的值,则该晶体的密度为______。
高三化学简答题困难题查看答案及解析
2017年,中科院大连化学物理研究所碳资源小分子与氢能利用创新特区研究组(DNL19T3)孙剑、葛庆杰研究员团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1) 工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5~26.5℃后用氨水吸收过量的CO2,该反应的化学方程式为_____________。在用氨水吸收前,烟气需冷却至15.5~26.5℃的可能原因是_________________。
(2) 该研究成果用CO2制取高辛烷值汽油的路线是先将CO2按逆水煤气反应生成CO,然后由CO与H2反应生成烃,产物中汽油组分占所有烃类产物的百分比近80%。
① 已知:H2 (g)+O2 (g) === H2O(l) ΔH1= —285.8 kJ·mol-1
C8H18(l)+O2(g) === 8CO2(g)+9H2O(l) ΔH3= —5518 kJ·mol-1
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方
程式__________________________。
② 在一实验容器中充入一定量的CO2和H2,若加入催化剂恰好完全反应,且产物只生成C5以上的烃类物质和水,则CO2与H2的物质的量之比不低于________。
(3) 二甲醚(CH3OCH3)的十六烷值高,燃烧尾气中污染物少,可代替柴油。CO、CO2混合加氢的方法是在一个反应器中将合成气直接转化为二甲醚,包括以下4个反应:
CO2(g)+3H2(g)CH3OH(g)+H2O(g) ①
CO2(g)+H2(g)CO(g)+H2O(g) ②
CO(g)+2H2(g)CH3OH(g) ③
2CH3OH(g)CH3OCH3(g)+H2O(g) ④
① 已知反应④在某温度下的平衡常数为K=400。此温度下,在一恒容密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
此时正、逆反应速率的大小:v(正) ______ v(逆) (填“>”、“<”或“=”)。
若加入CH3OH后,经10 min反应达到平衡,该时间内反应速率v(CH3OH)=_____。
② 某科研小组在反应温度503K~543K,反应压强分别是3、4、5、6、7MPa,n(CO)/n(CO+CO2)=0.5的情况下计算了二甲醚的平衡收率(二甲醚实际产量与反应物总量之比),结果如图1所示。
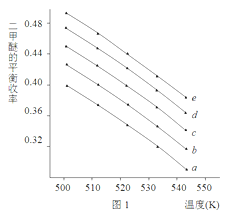
a~e曲线分别对应不同的压强条件,则e对应的压强是______,理由是___________。
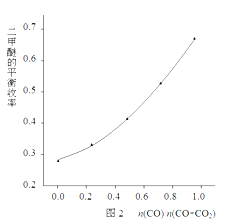
该科研小组在反应温度523K、反应压强5MPa的条件下,按照合成反应的化学计量比进料,改变n(CO)/n(CO+CO2)的比例,二甲醚的平衡收率的变化规律如图2所示。
由图2可知,二甲醚的平衡收率随着n(CO)/n(CO+CO2)比值的增大而单调上升,其原因是________________________________________________。
高三化学综合题困难题查看答案及解析
据2015年 4月 10 的报道,湖南大学 85后副教授鲁兵安参与斯坦福大学的团队刚刚发明出了一种“一分钟充满电”的新型铝离子电池。他们发现了一种新型石墨材料——泡沫石墨(graphite foam),泡沫石墨刚好可以充当电池的正极(负极用铝制成),而电解液则采用一种离子液体——即全由离子组成、室温下呈液态的离子化合物,具体成分为一种有机盐(化学表达式为[EMIm]Cl)与氯化铝的混合物。如图:
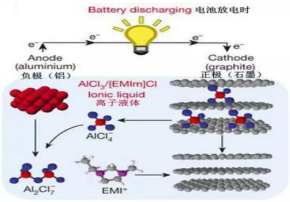
关于该电池的说法不正确的是( )
A.放电时,铝电极的电极反应式为:Al+7AlCl4—-3e—=4Al2Cl7—
B.[EMIm]Cl中既含离子键,又含共价键
C.电子流向为:石墨通过离子液体流向铝
D.充电时石墨电极的电极反应式为:Cn[AlCl4]-e—=Cn+ AlCl4—
高三化学选择题极难题查看答案及解析
氢能作为新型能源,可利用CO制得.北京大学马丁教授等团队向容积为VL的密闭容器中充入等物质的量的CO和H2O进行反应。
已知:
反应Ⅰ:FeO(s)+CO(g)Fe(s)+CO2(g) ΔH1
反应Ⅱ:FeO(s)+H2(g)Fe(s)+H2O(g) ΔH2
反应Ⅲ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH
反应Ⅲ在不同催化剂作用下(反应相同时间),温度与CO转化率的关系如图所示。

(1)反应Ⅲ的ΔH与ΔH1、ΔH2关系式:ΔH=_。
(2)若反应Ⅰ和反应Ⅱ的平衡常数分别为K1和K2,则反应Ⅲ的平衡常数K与K1、K2的关系式:K=___。
(3)随着温度的升高,CO的转化率先升后降,“后降”的可能原因是__。
(4)由图可知,ΔH__0(填“大于”或“小于”),催化剂应选择_(填“Au/α-MoC”或“Au/α-MoC/NaCN”)。
(5)已知T=1025K时,K=1。则平衡时CO的转化率α(0)=__。当T>1025K时,平衡时,H2的体积分数ω的取值范围为_。此时,CO还原FeO(s)的能力__H2(填“大于”或“小于”)。
(6)欲提高H2的体积分数,可采取的措施为__。
高三化学综合题中等难度题查看答案及解析
某研究团队设计出从污水“提取”潜在电能的新型微生物电池,该电池能将生活污水中有机物分解,电池结构如图所示。已知a电极为惰性材料,b电极为。下列说法不正确的是
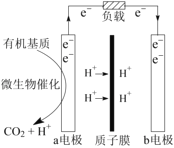
A.该法符合绿色化学“低能耗”的观点
B.b电极的反应式为
C.溶液中阴离子从右向左迁移
D.高温条件下,该电池不能正常工作
高三化学单选题简单题查看答案及解析
以北京大学马丁教授为代表的多个团队,研发出了高效的铁基(如、
、
、
)费托合成催化剂,以
和
为原料可高产率合成烯烃、烷烃,如
、
,为煤的气化、液化使用开拓了新途径。
⑴中能量最高的能级上的电子云有__________种伸展方向,位于不同方向中运动的电子的能量大小关系是_______________。当
原子电子排布由
时,体系的能量_________(填“增大”或“减小”)。
⑵、C、O三种元素的第一电离能由大到小的顺序为___________;
分子中碳原子的杂化轨道类型为________________;题干所述反应中
分子中断裂的化学键类型为__________(填字母)。
A.2个σ键、1个键B.1个σ键、2个
键C.非极性键
⑶新戊烷分子中5个碳原子形成的空间构型是_______________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高,其原因是_________。
⑷碳、铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:
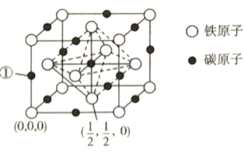
则编号为①的原子的坐标为_____________;该化合物的化学式为_____________;设该晶体的晶胞参数为,阿伏加德罗常数的值为
,则该晶体的密度为____________________
(列出计算式即可)。
高三化学综合题简单题查看答案及解析
氢叠氨酸(HN3)及其盐(NaN3、NH4N3、CuN3等) 都具有爆炸性,最近南京理工大学胡丙成教授团队成功合成出PHAC,其化学式为(N3)3 (NH4)4Cl。回答问题:
(1) PHAC中“N3”的化合价为_____________,N2F2的电子式为_____________。
(2)汽车安全气囊中NaN3可发生下列反应:
NaN3(s)=Na(s)+N2(g) △H1
2NaN3(s)+CuO(s)=Na2O(s)+3N2(g)+Cu(s) △H2
则反应CuO(s)+2Na(s)= Na2O(s)+ Cu(s) △H=_______(用△H1和△H2表示)
(3) 25℃,将1molNH4N3(s)投入一2L的恒容密闭容器中,0.5min后反应达到平衡,测得生成的两种单质的物质的量之和为1.6mol,则NH4N3的平衡转化率为________,25℃时该反应的平衡常数K=__________。
(4) 氢叠氨酸(HN3)易溶于水,且酸性与醋酸相近。
① HN3在水溶液中的电离方程式为_____________。
② 0.1mol·L-1的HN3溶液与0.1mol·L-1的NaN3等体积混合,混合溶液中各离子浓度有大到小的顺序为_________________。
③ 已知T℃时,Ksp(CuN3)=5.0×10-9,Ksp(Cu2S)=2.5×10-48,则相同温度下反应:
Cu2S(s)+2N3-(aq) 2CuN3(s)+S2-(aq)的平衡常数K=_______________。
高三化学综合题中等难度题查看答案及解析