-
2018年3月南开大学教授叶萌春及其团队借助廉价金属镍和苯基硼酸共催化的烯基化反应,首次实现烯丙醇高效、绿色合成重大突破。成果也在最新一期《德国应用化学》上发表。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的价电子排布式为___________________。
(2)1 mol CH2=CH-CH2OH含____molσ键,烯丙醇分子中碳原子的杂化类型为____。
(3)丙醛(CHCH2CHO)的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是_______________________________。
(4)羰基镍[Ni(CO)4)用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是_________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2-和[Ni(SCN)2]-等。NH3的空间构型是_____________。
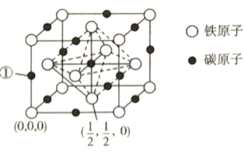
(6)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙中。
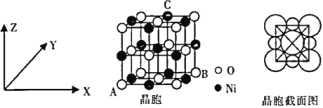
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为____________。
②已知:氧化镍晶胞密度为dg·cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为__________nm(用代数式表示)。
-
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为________。
② 键,烯丙醇分子中碳原子的杂化类型是__________。
键,烯丙醇分子中碳原子的杂化类型是__________。
(2)乙炔是有机合成的一种重要原料。实验室可用 与水反应得到乙炔。
与水反应得到乙炔。
①将乙炔通入 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为____。
的核外电子排布式为____。
②乙炔与 反应可得丙烯腈(
反应可得丙烯腈( ),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有
),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有 键的数目为___________。
键的数目为___________。
-
据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为____________________________________________。
(2)1 mol CH2=CH-CH2OH中σ键和π键的个数比为___________,丙烯醇分子中碳原子的杂化类型为___________。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是______________________。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)4]2-等。[Ni(NH3)6]2+中心原子的配位数是___________ ,与SCN-互为等电子体的分子为___________。
(6)“NiO”晶胞如图所示。
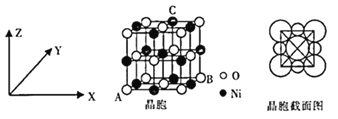
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___________。
②已知:氧化镍晶胞密度为dg/cm3,NA代表阿伏加德罗常数的值,则Ni2+半径为___________nm(用代数式表示)。
-
据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为___。
(2)1molCH2=CH-CH2OH中σ键和π键的个数比为___,丙烯醇分子中碳原子的杂化类型为___。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是___。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)2]2-等。[Ni(NH3)6]2+中心原子的配位数是___,与SCN-互为等电子体的分子为___。
(6)“NiO”晶胞如图所示。
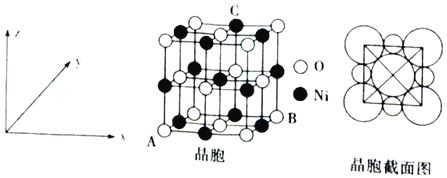
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___。
②已知:氧化镍晶胞密度为dg⋅cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为___nm(用代数式表示)。
-
镍是有机合成的重要催化剂。
(1)基态镍原子的价电子排布式___________________________
(2)镍和苯基硼酸共催化剂实现了丙烯醇(CH2=CH—CH2OH)的绿色高效合成.丙烯醇中碳原子的杂化类型有______________________;丙醛(CH3CH2CHO)与丙烯醇(CH2=CH—CH2OH)分子量相等,但丙醛比丙烯醇的沸点低的多,其主要原因是________________________。
(3)羰基镍[Ni(CO)4]用于制备高纯度镍粉.羰基镍[Ni(CO)4]中Ni、C、O 的电负性由大到小的顺序为______。
(4)Ni2+ 能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]- 等。NH3 的空间构型为:_______;与SCN- 互为等电子体的分子有:__________________(填分子式)
(5)“NiO”晶胞如图:
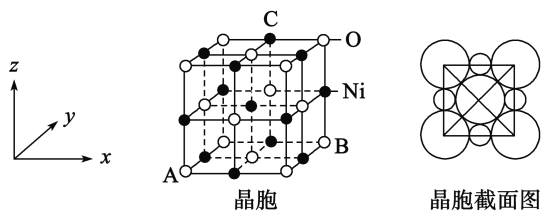
①氧化镍晶胞中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为_____________
②已知氧化镍晶胞密度dg/cm3,NA 代表阿伏加德罗常数的值,则Ni2+ 半径为________nm(用代数式表示)
-
以北京大学马丁教授为代表的多个团队,研发出了高效的铁基(如 、
、 、
、 、
、 )费托合成催化剂,以
)费托合成催化剂,以 和
和 为原料可高产率合成烯烃、烷烃,如
为原料可高产率合成烯烃、烷烃,如 、
、 ,为煤的气化、液化使用开拓了新途径。
,为煤的气化、液化使用开拓了新途径。
⑴ 中能量最高的能级上的电子云有__________种伸展方向,位于不同方向中运动的电子的能量大小关系是_______________。当
中能量最高的能级上的电子云有__________种伸展方向,位于不同方向中运动的电子的能量大小关系是_______________。当 原子电子排布由
原子电子排布由 时,体系的能量_________(填“增大”或“减小”)。
时,体系的能量_________(填“增大”或“减小”)。
⑵ 、C、O三种元素的第一电离能由大到小的顺序为___________;
、C、O三种元素的第一电离能由大到小的顺序为___________; 分子中碳原子的杂化轨道类型为________________;题干所述反应中
分子中碳原子的杂化轨道类型为________________;题干所述反应中 分子中断裂的化学键类型为__________(填字母)。
分子中断裂的化学键类型为__________(填字母)。
A.2个σ键、1个 键B.1个σ键、2个
键B.1个σ键、2个 键C.非极性键
键C.非极性键
⑶新戊烷 分子中5个碳原子形成的空间构型是_______________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高,其原因是_________。
分子中5个碳原子形成的空间构型是_______________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高,其原因是_________。
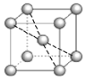
⑷碳、铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:
则编号为①的原子的坐标为_____________;该化合物的化学式为_____________;设该晶体的晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为____________________
,则该晶体的密度为____________________ (列出计算式即可)。
(列出计算式即可)。
-
2020年1月,南开大学研究团队“高效手性螺环催化剂的发现”获得2019年度国家自然科学技术一等奖,含多种金属元素的催化剂正在刷新合成化学的新高度。
回答下列问题:
(1)形成“刚性”螺环的元素是碳,基态碳原子的价电子轨道表达式是___。
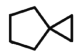
(2)如图是一种简单螺环烃,分子中碳原子的杂化方式为___,分子中___(填“含”或“不含”)手性碳原子。
(3)铁及其化合物羰基铁[Fe(CO)5]常用作催化剂。
①1mol Fe(CO)5分子中含有的σ键数目为____,写出一种与CO互为等电子体的离子___。
②Fe(CO)5是一种浅黄色液体,熔点-20℃,沸点103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。Fe(CO)5是___(填“极性”或“非极性”)分子;配体CO提供孤电子对的原子是C而不是O,原因是____。
③如图是某Fe单质的晶胞模型。已知晶体密度为d g·cm-3,则铁原子的半径为___nm(用含有d、NA的代数式表示)。
(4)在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”。羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是___。
-
【化学-选修3:物质结构与性质】
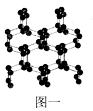
南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破。请根据材料回答以下问题:
(1)N、O、F三种元素的第一电离能由大到小的顺序为____(填元素符号);与N2互为等电子体的全氧离子化学式为_______;具有空间网状结构的高聚氮结构如图一所示,则N70的沸点_____(填“>”、“<”或“=”)高聚氮的沸点,原因是_________________;N70和高聚氮属于_____(选填序号)。
A.同素异形体 B.同分异构体 C.同位素 D.同系物
(2)叠氮化物是研究较早的含全氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3) 等。叠氮化物能形成多种配合物,在[Co(N3)(NH3)5]SO4,其中钴显____价,它的配体是____,SO42-的立体构型为___________。
(3)HN3是一种全氮阴离子酸,可由肼(N2H4)被HNO2氧化制得。下列说法正确的是____。
A.酸性:HNO2>HNO2
B. N2H4分子中N原子均采取sp3杂化
C. NaN3的晶格能小于KN3的晶格能
D.上述生成氢叠氮酸的化学方程式为N2H4+HNO2=2H2O+HN3
(4)N8是一种由全氮阳离子和全氮阴离子构成的特殊物质,已知阳离子由5个氮原子排列成V 形,每个氮原子均达到八电子稳定结构,则阳离子的电子式为_______。
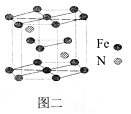
(5)一种氮铁化合物的结构如图二所示,若图中六棱柱的体积为Vcm3, 用NA表示阿伏加德罗常数的值,则该晶体的密度为______。
-
CO2的固定和转化是世界性课题。兰州大学景欢旺教授团队巧妙设计构建了系列新型光电催化人工光合成体系——光电催化池,p-n半导体异质结催化CO2在水中直接制备长碳链有机物并放出氧气,原理如图,下列说法不正确的是
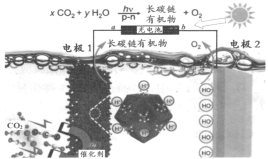
A.电极1的电势比电极2的电势高
B.该设计向大自然学习,模仿植物的光合作用
C.电子从a极流到电极1,从电极2流到b极
D.负极区,p-n为催化剂,CO2发生还原反应生成长碳链有机物
-
生物固氮与模拟生物固氮都是重大基础性研究课题。大连理工大学曲景平教授团队设计合成了一类新型邻苯二硫酚桥联双核铁配合物,建立了双铁分子仿生化学固氮新的功能分子模型。如图是所发论文插图。以下说法错误的是
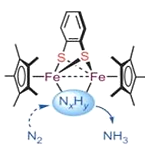
A.催化剂不能改变反应的焓变
B.催化剂不能改变反应的活化能
C.图中反应中间体NXHY数值X<3
D.图示催化剂分子中包含配位键











