-
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为________。
② 键,烯丙醇分子中碳原子的杂化类型是__________。
键,烯丙醇分子中碳原子的杂化类型是__________。
(2)乙炔是有机合成的一种重要原料。实验室可用 与水反应得到乙炔。
与水反应得到乙炔。
①将乙炔通入 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为____。
的核外电子排布式为____。
②乙炔与 反应可得丙烯腈(
反应可得丙烯腈( ),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有
),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有 键的数目为___________。
键的数目为___________。
-
据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为____________________________________________。
(2)1 mol CH2=CH-CH2OH中σ键和π键的个数比为___________,丙烯醇分子中碳原子的杂化类型为___________。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是______________________。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)4]2-等。[Ni(NH3)6]2+中心原子的配位数是___________ ,与SCN-互为等电子体的分子为___________。
(6)“NiO”晶胞如图所示。
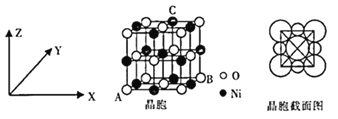
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___________。
②已知:氧化镍晶胞密度为dg/cm3,NA代表阿伏加德罗常数的值,则Ni2+半径为___________nm(用代数式表示)。
-
据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为___。
(2)1molCH2=CH-CH2OH中σ键和π键的个数比为___,丙烯醇分子中碳原子的杂化类型为___。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是___。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)2]2-等。[Ni(NH3)6]2+中心原子的配位数是___,与SCN-互为等电子体的分子为___。
(6)“NiO”晶胞如图所示。
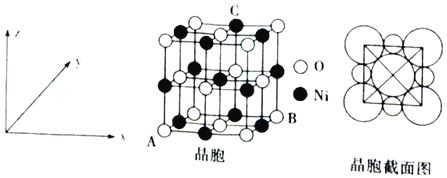
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___。
②已知:氧化镍晶胞密度为dg⋅cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为___nm(用代数式表示)。
-
2018年3月南开大学教授叶萌春及其团队借助廉价金属镍和苯基硼酸共催化的烯基化反应,首次实现烯丙醇高效、绿色合成重大突破。成果也在最新一期《德国应用化学》上发表。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的价电子排布式为___________________。
(2)1 mol CH2=CH-CH2OH含____molσ键,烯丙醇分子中碳原子的杂化类型为____。
(3)丙醛(CHCH2CHO)的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是_______________________________。
(4)羰基镍[Ni(CO)4)用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是_________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2-和[Ni(SCN)2]-等。NH3的空间构型是_____________。
(6)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙中。
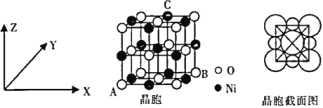
①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为____________。
②已知:氧化镍晶胞密度为dg·cm-3,NA代表阿伏加德罗常数的值,则Ni2+半径为__________nm(用代数式表示)。
-
镍是有机合成的重要催化剂。
(1)基态镍原子的价电子排布式___________________________
(2)镍和苯基硼酸共催化剂实现了丙烯醇(CH2=CH—CH2OH)的绿色高效合成.丙烯醇中碳原子的杂化类型有______________________;丙醛(CH3CH2CHO)与丙烯醇(CH2=CH—CH2OH)分子量相等,但丙醛比丙烯醇的沸点低的多,其主要原因是________________________。
(3)羰基镍[Ni(CO)4]用于制备高纯度镍粉.羰基镍[Ni(CO)4]中Ni、C、O 的电负性由大到小的顺序为______。
(4)Ni2+ 能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]- 等。NH3 的空间构型为:_______;与SCN- 互为等电子体的分子有:__________________(填分子式)
(5)“NiO”晶胞如图:
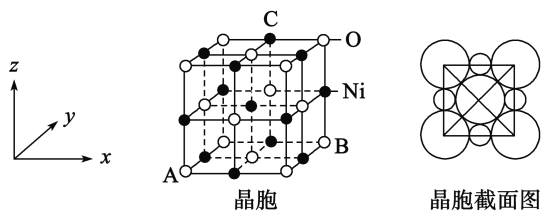
①氧化镍晶胞中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为_____________
②已知氧化镍晶胞密度dg/cm3,NA 代表阿伏加德罗常数的值,则Ni2+ 半径为________nm(用代数式表示)
-
2020年1月,南开大学研究团队“高效手性螺环催化剂的发现”获得2019年度国家自然科学技术一等奖,含多种金属元素的催化剂正在刷新合成化学的新高度。
回答下列问题:
(1)形成“刚性”螺环的元素是碳,基态碳原子的价电子轨道表达式是___。
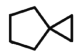
(2)如图是一种简单螺环烃,分子中碳原子的杂化方式为___,分子中___(填“含”或“不含”)手性碳原子。
(3)铁及其化合物羰基铁[Fe(CO)5]常用作催化剂。
①1mol Fe(CO)5分子中含有的σ键数目为____,写出一种与CO互为等电子体的离子___。
②Fe(CO)5是一种浅黄色液体,熔点-20℃,沸点103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。Fe(CO)5是___(填“极性”或“非极性”)分子;配体CO提供孤电子对的原子是C而不是O,原因是____。
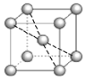
③如图是某Fe单质的晶胞模型。已知晶体密度为d g·cm-3,则铁原子的半径为___nm(用含有d、NA的代数式表示)。
(4)在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”。羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是___。
-
以北京大学马丁教授为代表的多个团队,研发出了高效的铁基(如 、
、 、
、 、
、 )费托合成催化剂,以
)费托合成催化剂,以 和
和 为原料可高产率合成烯烃、烷烃,如
为原料可高产率合成烯烃、烷烃,如 、
、 ,为煤的气化、液化使用开拓了新途径。
,为煤的气化、液化使用开拓了新途径。
⑴ 中能量最高的能级上的电子云有__________种伸展方向,位于不同方向中运动的电子的能量大小关系是_______________。当
中能量最高的能级上的电子云有__________种伸展方向,位于不同方向中运动的电子的能量大小关系是_______________。当 原子电子排布由
原子电子排布由 时,体系的能量_________(填“增大”或“减小”)。
时,体系的能量_________(填“增大”或“减小”)。
⑵ 、C、O三种元素的第一电离能由大到小的顺序为___________;
、C、O三种元素的第一电离能由大到小的顺序为___________; 分子中碳原子的杂化轨道类型为________________;题干所述反应中
分子中碳原子的杂化轨道类型为________________;题干所述反应中 分子中断裂的化学键类型为__________(填字母)。
分子中断裂的化学键类型为__________(填字母)。
A.2个σ键、1个 键B.1个σ键、2个
键B.1个σ键、2个 键C.非极性键
键C.非极性键
⑶新戊烷 分子中5个碳原子形成的空间构型是_______________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高,其原因是_________。
分子中5个碳原子形成的空间构型是_______________,该分子是________(填“极性”或“非极性”)分子。随着烃分子中碳原子数目的增加,同系物的沸点升高,其原因是_________。
⑷碳、铁之间可形成多种化合物,其中一种化合物的晶体结构(面心立方结构)如图所示:
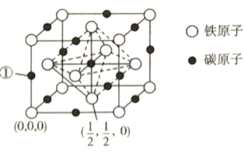
则编号为①的原子的坐标为_____________;该化合物的化学式为_____________;设该晶体的晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为____________________
,则该晶体的密度为____________________ (列出计算式即可)。
(列出计算式即可)。
-
近日,某科研团队成功合成了Ni—Fe双原子催化剂(Ni/Fe—C—N),并应用于高效催化CO2还原。回答下列问题:
(1)基态铁原子的价电子轨道排布图为__。铁元素常见的离子有Fe2+和Fe3+,稳定性Fe2+__Fe3+(填“>”或“<”),原因是__。
(2)C、N、O三种元素的第一电离能由大到小的顺序为__。
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与CO提供配位的电子总数之和为18,则n=___;该化合物易溶于苯及四氯化碳等有机溶剂,原因是___。
(4)二茂铁的结构为 ,由Fe2+和
,由Fe2+和 (环戊二烯基负离子)构成。一个
(环戊二烯基负离子)构成。一个 中σ键总数为__,C原子的杂化轨道类型为__。
中σ键总数为__,C原子的杂化轨道类型为__。
(5)某C、Fe合金的晶胞结构如图所示:
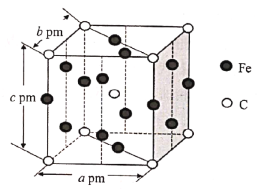
该合金的化学式为__,若该晶体的晶胞参数为apm、bpm、cpm,α=β=γ=90o,密度为ρg·cm-3,则NA为__(写出计算式即可)。
-
南开大学的周其林院士及其团队凭借“高效手性螺环催化剂”的发现,获得了2019年度国家自然科学奖一等奖。一种手性螺环分子的结构简式如图所示。下列关于该有机物说法错误的是
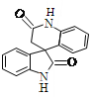
A.分子式为C16H12N2O2
B.分子中除氢原子之外的所有原子可能共平面
C.分子中只有一个手性碳原子
D.在酸性条件下能水解,且水解产物有8种化学环境不同的氢原子
-
二氧化碳捕集与封存是应对气候变化问题的解决方案之一。回答下列问题:
(l)我国科研团队利用低温等离子体协同催化技术,在常温常压下实现了将CO2和CH4一步转化为化工产品。试写出 CO2与CH4合成乙酸的热化学方程式:____。
(甲烷和乙酸的燃烧热分别为-890.31 kJ/mol、-876.72 kJ/mol)
(2)在某一钢性密闭容器中CH4、CO2的分压分别为15 kPa、20 kPa,加入Ni/α-Al2 O3催化剂并加热至1123 K使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
①研究表明CO的生成速率v(CO)=1.28 10-2﹒p(CH4)
10-2﹒p(CH4) p(CO2)(kPa
p(CO2)(kPa s-1),某时刻测得p(H2)=10 kPa,则 p(CH4)=___kPa,v(CO)=___kPa
s-1),某时刻测得p(H2)=10 kPa,则 p(CH4)=___kPa,v(CO)=___kPa s-1。
s-1。
②达到平衡后测得体系压强是起始时的 ,则该反应的平衡常数Kp=____kPa)2。
,则该反应的平衡常数Kp=____kPa)2。
(3)氮化镓(GaN)与Cu可组成如图所示的人工光合系统,该装置能以CO2和H2O为原料合成CH4。
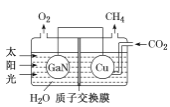
①该装置工作时H+移向____(填“GaN”或“Cu”)电极,该电极上的电极反应式为 ___。
②该装置每产生1 mol CH4,左极室溶液质量减少____g。
③本实验条件下,若CO2转化为烃(如甲烷、乙烯等)的转化率为10%,生成CH4的选择性为12%,现收集到12 mol CH4,则通入的CO2为____mol。(已知:选择性=生成目标产物消耗的原料量/原料总的转化量)
(4)上述人工光合系统装置也可以制备乙烯、乙炔等重要化工原料。2010年Sheth等研究得出乙炔在Pd表面选择加氢的反应机理,如下图所示。其中吸附在Pd表面的物质用“*”标注。
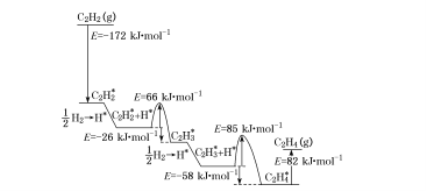
上述吸附反应为 ____填“吸热”或“放热”)反应,该过程中最小能垒(活化能)为___ kJ mol-1,该步骤的化学方程式为____。
mol-1,该步骤的化学方程式为____。
。请回答下列问题:
键,烯丙醇分子中碳原子的杂化类型是__________。
与水反应得到乙炔。
溶液中生成
红棕色沉淀。基态
的核外电子排布式为____。
反应可得丙烯腈(
),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有
键的数目为___________。











