-
利用pH传感器探究NaOH溶液与硫酸、硫酸铜混合溶液发生反应的离子反应顺序,绘得三份曲线图如图。已知实验使用的NaOH溶液浓度和滴速相同;硫酸溶液和硫酸铜溶液浓度相同;混合溶液中两溶质的浓度也相同。
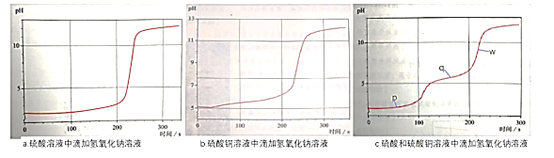
以下解读错误的是
A.三个时点的c(Cu2+):p>q>w
B.w点:c(Na+)>c(SO42-)>c(Cu2+)>c(H+)
C.混合溶液中滴加NaOH溶液,硫酸先于硫酸铜发生反应
D.q点时溶液离子浓度:c(SO42-)+c(OH-)=c(Cu2+)+c(H+)+c(Na+)
-
实验室使用pH传感器来测定 和
和 混合物中
混合物中 的含量,称取
的含量,称取 样品,溶于水配成
样品,溶于水配成 溶液,取出该溶液
溶液,取出该溶液 用
用 盐酸滴定,得到图曲线.下列说法不正确的是
盐酸滴定,得到图曲线.下列说法不正确的是

A.此样品
B.计量点 溶液中大量存在的阴离子是
溶液中大量存在的阴离子是
C.计量点 之间发生反应的离子方程式为
之间发生反应的离子方程式为
D.使用该方法测定 和NaOH混合溶液中的NaOH含量,将会得到1个计量点
和NaOH混合溶液中的NaOH含量,将会得到1个计量点
-
过硫酸钠 常用作漂白剂、氧化剂等。某研究小组利用如图装置制备
常用作漂白剂、氧化剂等。某研究小组利用如图装置制备 并探究其性质
并探究其性质 加热及夹持仪器略去
加热及夹持仪器略去 。
。
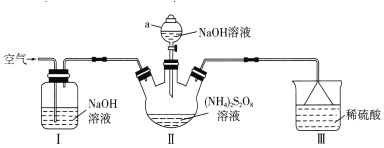
已知:





⑴仪器a的名称是______。装置Ⅰ中NaOH溶液的作用是______。
⑵装置Ⅱ发生反应的同时,需要持续通入空气的目的是______。
⑶装置Ⅲ的作用是______。
⑷ 溶液与铜反应只生成两种盐,且反应先慢后快。
溶液与铜反应只生成两种盐,且反应先慢后快。
①该反应的化学方程式为______。
②某同学推测反应先慢后快的原因可能是生成的 对反应起催化作用。设计实验方案验证该推测是否正确______。(供选试剂:Cu、
对反应起催化作用。设计实验方案验证该推测是否正确______。(供选试剂:Cu、 溶液、
溶液、 溶液、
溶液、 溶液、蒸馏水)
溶液、蒸馏水)
⑸测定产品纯度:称取 样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,用
样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,用 标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为
标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为 。(已知:
。(已知: )
)
①选用的指示剂是______;达到滴定终点的现象是______。
②样品的纯度为______%。
-
下列物质混合发生化学反应,且反应属于离子反应的是:
A.NaOH溶液和K2SO4溶液混合
B.锌片投入稀硫酸中
C.KClO3(固体)和MnO2(固体)混合加热制O2
D.H2和O2反应生成水
-
下列离子方程式不正确的是
A.硫酸型酸雨的形成会涉及反应:
B.纯碱溶液显碱性的原因:
C.盛放NaOH溶液的试剂瓶不能用玻璃塞的原因:
D.成分为盐酸的洁厕灵与“84”消毒液混合使用易中毒:
-
为探究铁和硫反应产物中铁的化合价,某同学设计了如下所示的实验过程:

已知:①铁和硫反应产物不溶于碱,能溶于硫酸
②硫可溶于热碱溶液,发生类似于 Cl2 和 NaOH 溶液的化学反应下列说法不正确的是
A.混合粉末应在 N2 氛围中进行加热,所用 H2SO4 溶液应先煮沸
B.取溶液 A,滴加 KSCN 溶液,未出现红色,可证明铁和硫反应只有+2 价铁生成
C.滤渣用稀 H2SO4 溶解时应在通风橱中进行
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH- 2S2-+SO32-+3H2O
2S2-+SO32-+3H2O
-
已知 + [AI(OH)4]— ===
+ [AI(OH)4]— ===
 向含有等物质的量的
向含有等物质的量的 、
、 、
、 的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:
的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:
① ===
=== ②
② ===[AI(OH)4]— ③
===[AI(OH)4]— ③ ===
===
④
 ===
=== 发生反应的先后顺序正确的是
发生反应的先后顺序正确的是
A.① ④
④ ③
③ ② B.①
② B.① ③
③ ②
② ④ C.①
④ C.① ③
③ ④
④ ② D.①
② D.① ②
② ③
③ ④
④
-
常温下,向10.00mL浓度均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH•H2O]的混合溶液中逐滴加入盐酸。利用传感器测得该过程溶液中的阳离子总浓度变化曲线如图;巳知二甲胺在水中电离与氨相似,常温下Kb[(CH3)2NH•H2O]=l.60×l0-4。下列说法正确的是( )
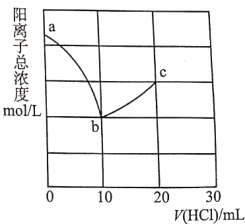
A.a点溶液中,c[(CH3)2NH2+]约为l.60×l0-4mol/L
B.从a到c的过程中,水的电离程度最大的是b点
C.c点溶液中:3c(Na+)+c[(CH3)2NH2+]=2c(Cl-)
D.V(HCl)=15.00mL时,c[(CH3)2NH2+]<c[(CH3)2NH•H2O]
-
已知浓硫酸和乙醇的混合液加热后可以产生乙烯。为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:将生成的气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。乙同学在甲同学的实验中,发现褪色后的溶液中有硫酸根离子,推测在制得的乙烯中还可能有少量还原性气体杂质,由此他提出必须先除去还原性杂质,再与溴水反应。
(1)甲同学实验中溴水褪色的主要化学方程式为__________________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生了加成反应,理由是
________。
a.使溴水褪色的反应未必是加成反应
b.使溴水褪色的反应就是加成反应
c.使溴 水褪色的物质未必是乙烯
水褪色的物质未必是乙烯
d.使溴水褪色的物质就是乙烯
(3)乙同学推测乙烯中必定含有的一种气体,可以用________(填试剂名称)来验证,这种气体与溴水反应的化学方程式是______________________________。
-
以铅蓄电池为电源电解制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向。下列说法正确的是( )
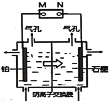
A.M发生的电极反应为PbO2+SO42-+4H+=PbSO4+2H2O
B.左侧气孔逸出的气体可能为副产物O2
C.电解槽中发生的总反应为:2MnSO4+2H2O 2Mn+O2↑+2H2SO4
2Mn+O2↑+2H2SO4
D.若用阳离子交换膜代替阴离子交换膜,阴极可能得到MnO2





