-
下列关于常见无机物的应用说法错误的是( )
A.用[Al2(OH)nCl6-n]m(碱式氯化铝)可除去水体中的悬浮杂质并消毒杀菌
B.铁粉和炭粉组成的微电池可用于处理工业废水
C.氨水可用于脱除工业烟气中的二氧化硫
D.将废铁屑加入氯化亚铁溶液中,可用于除去工业废气中的氯气
高三化学单选题中等难度题查看答案及解析
-
聚合氯化铝是新型、高效絮凝剂和净水剂,其单体是液态碱式氯化铝[Al2(OH)nCl6-n]。工业上常采用铝盐溶液部分水解制备碱式氯化铝,其工艺流程如下:
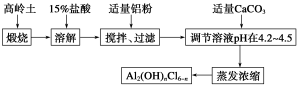
已知:高岭土:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)及少量杂质和水。Al3+以氢氧化物形式完全沉淀时,溶液的pH为5.2。根据流程图回答下列问题:
(1)写出溶解过程中反应的离子方程式________________________;
(2)加适量铝粉的主要目的是_________________________________。
(3)溶液的pH需控制在4.2~4.5的原因是__________________,__________________。
(4)“蒸发浓缩”需保持温度在90~100 ℃,控制该温度的操作名称是____________,写出该过程反应的化学方程式______________________。
高三化学填空题困难题查看答案及解析
-
聚合氯化铝是新型、高效絮凝剂和净水剂,其单体是液态碱式氯化铝[Al2(OH)nCl6-n],工业上常采用铝盐溶液部分水解制备碱式氯化铝,其工艺流程如下:

已知:高岭土:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)及少量杂质和水。
①Al3+以氢氧化物形式完全沉淀时,溶液的pH为5.2。
根据流程图回答下列问题:
(1)写出溶解过程中反应的离子方程式________、________;
(2)加适量铝粉的主要目的是 ;
(3)溶液的pH需控制在4.2~4.5的原因是________;
(4)“蒸发浓缩”需保持温度在90~100℃,控制该温度的操作名称是 ,写出该过程反应的化学方程式________。
高三化学填空题简单题查看答案及解析
-
(20分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭 土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
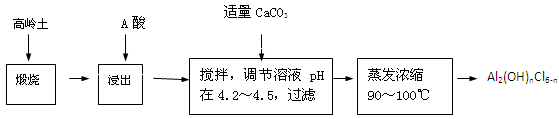
已知:Fe3+、Al3+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2。
根据流程图回答下列问题:
(1)“煅烧”的目的是_______________________________________________。
(2)“浸出”过程中发生反应的离子方程式为_______________________________。
(3)“浸出”选用的酸为_______。配制质量分数15%的A酸需要200mL30%的A酸(密度约为1.15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、______________。
(4)为提高铝的浸出率,可采取的措施有_______________(要求写出三条)。
(5)“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是_________________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是_________________________。
(6)实验中制备碱式氯化铝反应的化学方程式为_________________
高三化学填空题简单题查看答案及解析
-
(20分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭 土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
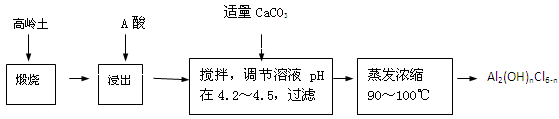
已知:Fe3+、Al3+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2。
根据流程图回答下列问题:
(1)“煅烧”的目的是_______________________________________________。
(2)“浸出”过程中发生反应的离子方程式为_______________________________。
(3)“浸出”选用的酸为_______。配制质量分数15%的A酸需要200mL30%的A酸(密度约为1.15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、______________。
(4)为提高铝的浸出率,可采取的措施有_______________(要求写出三条)。
(5)“调节溶液pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是_________________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是_________________________。
(6)实验中制备碱式氯化铝反应的化学方程式为_________________
高三化学填空题简单题查看答案及解析
-
(16分)聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
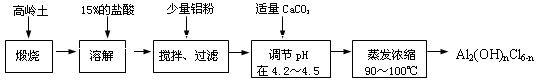
回答下列问题:
(1)“煅烧”的目的是________。
(2)“溶解”过程中发生反应的离子方程式为
________
(3)加少量铝粉的主要作用是________。
(4)“调节pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是________;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是________。
高三化学填空题中等难度题查看答案及解析
-
(16分)水处理剂在生产生活中有重要的应用。
(1)聚合氯化铝晶体([Al2(OH)nCl6-n∙xH2O]m)是一种高效无机水处理剂,它的制备原理是通过调节增大A1C13溶液的pH,促进其水解而结晶析出。利用高岭土制备聚合氯化铝,其制备过程有如下两种途径:
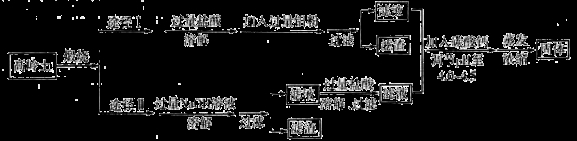
说明:①高岭土的化学组成为:Al2O3、SiO2、Fe2O3及少量有机杂质和水分,
②高岭土在煅烧的过程中可除去有机杂质和水分。
①途径I和途径Ⅱ中最合理的是_________。
②途径I中加入铝粉最主要的目的是__________(选填序号字母)。
a.中和过量的盐酸 b.将Fe3+还原为Fe2+
c.除去溶液中的铁元素 d.制备生成聚合氯化铝所需要的AlCl3
③加入碳酸钙调节溶液pH至4.0~4.5的目的是_______________________。
④蒸发浓缩过程中生成Al2(OH)nCl6-n∙xH2O的化学反应方程式是_______。
(2)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂。电解法制备Na2FeO4的装置如右图所示:
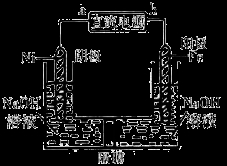
请根据图示回答:电解过程的化学方程式为_________;电路中每通过0.6 mol电子在Ni电极上产生的气体在标况下的体积为_________;隔膜应选择__________(填“阳离子交换膜”或“阴离子交换膜”)。
高三化学实验题极难题查看答案及解析
-
碱式氯化铝[ Al2(OH)nCl6-n ] 是利用工业铝灰和活性铝矾土为原料(主要含Al、Al2O3、SiO2及铁的氧化物)经过精制加工而成,此产品活性较高,对工业污水具有较好的净化效果。其制备流程如下:
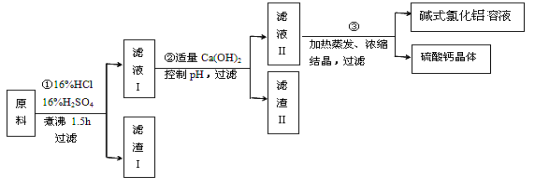
(1)原料需要粉碎,其目的是 ;滤渣I的主要成分是 ;
(2)步骤①在煮沸过程中,溶液逐渐变为浅绿色,检验溶液中呈浅绿色的阳离子常采用加入_________溶液进行检验(填试剂化学式)。
(3)步骤②中加入适量的Ca(OH)2并控制pH,其目的:一是生成碱式氯化铝;二是 ;已知碱式氯化铝的分散质粒子大小在1~100 nm之间,则区别滤液I与碱式氯化铝两种液体的物理方法是 ;若Ca(OH)2溶液过量,则步骤③得到的碱式氯化铝产率偏低,用离子方程式解释其原因为 ;
(4)某温度下若0.1 mol AlCl3溶于蒸馏水,当有2.5%水解生成Al(OH)3胶体时,吸收热量Q kJ ,该水解过程的热化学反应方程为 。
高三化学实验题简单题查看答案及解析
-
碱式氯化铝[ Al2(OH)nCl6-n ] 是利用工业铝灰和活性铝矾土为原料(主要含Al、Al2O3、SiO2及铁的氧化物)经过精制加工而成,此产品活性较高,对工业污水具有较好的净化效果。其制备流程如下:
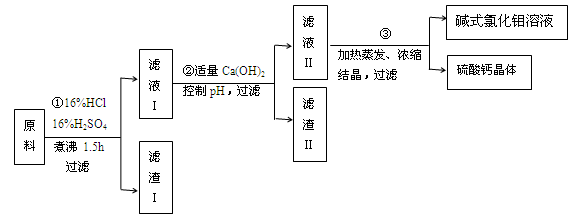
(1)原料需要粉碎,其目的是 ;滤渣I的主要成分是 ;
(2)步骤①在煮沸过程中,溶液逐渐变为浅绿色,此时溶液中呈浅绿色的阳离子常采用加入 试剂进行检验(填化学式);随后溶液又变为棕黄色,相关反应的离子方程式为 ;
(3)步骤②中加入适量的Ca(OH)2并控制pH,其目的:一是生成碱式氯化铝;二是 ;已知碱式氯化铝的分散质粒子大小在1~100 nm之间,则区别滤液I与碱式氯化铝两种液体的物理方法是 ;若Ca(OH)2溶液过量,则步骤③得到的碱式氯化铝产率偏低,该反应的离子方程式为 ;
(4)某温度下若0.1 mol AlCl3溶于蒸馏水,当有2.5%水解生成Al(OH)3溶液时,吸收热量Q kJ ,该过程的热化学反应方程式为 。
高三化学填空题极难题查看答案及解析
-
碱式氯化铝[Al2(OH)nCl6-n]是利用工业铝灰和活性铝矾土为原料(主要含Al、Al2O3、SiO2及铁的氧化物)经过精制加工而成,此产品活性较高,对工业污水具有较好的净化效果。其制备流程如下:

(1)原料需要粉碎,其目的是___________;滤渣I的主要成分是____________;
(2)步骤①在煮沸过程中,溶液逐渐变为浅绿色,检验溶液中呈浅绿色的阳离子常采用加入_________溶液进行检验(填试剂化学式)。
(3)步骤②中加入适量的Ca(OH)2并控制pH,其目的:一是生成碱式氯化铝;二是_________;已知碱式氯化铝的分散质粒子大小在1~100 nm之间,则区别滤液I与碱式氯化铝两种液体的物理方法是________;若Ca(OH)2溶液过量,则步骤③得到的碱式氯化铝产率偏低,用离子方程式解释其原因为__________;
(4)某温度下若0.1 mol AlCl3溶于蒸馏水,当有2.5%水解生成Al(OH)3胶体时,吸收热量Q kJ,该水解过程的热化学反应方程为__________________。
高三化学工业流程中等难度题查看答案及解析