-
H2CO3 和 H2C2O4 都是二元弱酸,不同 pH 环境下它们不同形态的粒子的组成百分率如图所示:
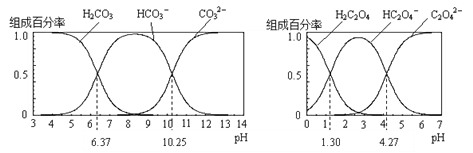
下列说法正确的是
A. 在 pH 为 6.37 及 10.25 时,溶液中 c(H2CO3)=c(HCO3-)=c(CO32-)
B. 反应 HCO3-+H2O H2CO3+OH-的平衡常数为 10-7.63
H2CO3+OH-的平衡常数为 10-7.63
C. 0.1 mol•L-1 NaHC2O4 溶液中 c(HC2O4-)+2c(C2O42-)+c(H2C2O4) =0.1 mol•L-1
D. 往 Na2CO3 溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+HC2O4-
-
H2CO3 和 H2C2O4 都是二元弱酸,常温下,不同 pH环境下它们不同形态的粒子的组成百分率如图所示:
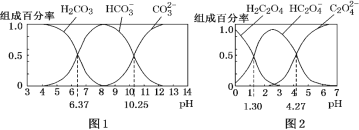
下列说法正确的是( )
A.在 pH为6.37及10.25时,溶液均存在 c(H2CO3)=c(HCO3-)=c(CO32-)
B.反应 CO32-+H2O HCO3-+OH- 的平衡常数为10-7.23
HCO3-+OH- 的平衡常数为10-7.23
C.0.1 mol·L-1NaHC2O4 溶液中 c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D.往Na2CO3溶液中加入少量草酸溶液,发生反应:2CO32−+H2C2O4=2HCO3−+C2O42−
-
H2CO3和H2C2O4都是二元弱酸,不同pH环境下它们不同形态的粒子的组成百分率如图所示:下列说法正确的是( )

A.在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-)
B.反应 HCO3-+H2O H2CO3+OH-的平衡常数为
H2CO3+OH-的平衡常数为
C.0.1 mol/L NaHC2O4溶液中c(C2O4-)+c(H2C2O4)=0.1 mol/L
D.往Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+ HC2O4-
-
 和
和  都是二元弱酸,不同 pH 环境下它们不同形态的粒子的组成百分率如图所示:
都是二元弱酸,不同 pH 环境下它们不同形态的粒子的组成百分率如图所示:

下列说法正确的是
A.在 pH 为  及
及  时,溶液中
时,溶液中 
B.反应  的平衡常数为
的平衡常数为 
C.
 溶液中
溶液中 

D.往  溶液中加入少量草酸溶液,发生反应:
溶液中加入少量草酸溶液,发生反应:
-
H2X为二元弱酸,常温下,将NaOH溶液加入到H2X溶液中,在不同pH环境下,不同形态的粒子(酸、酸式酸根、酸根离子)的组成分数如图所示。下列说法正确的是
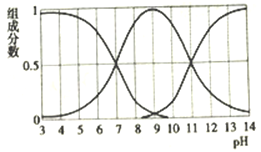
A. HX-的电离程度小于水解程度
B. 在pH=7的溶液中HX-和X2-能大量共存
C. 在pH=9时,H2X 与NaOH恰好完全中和
D. 1L.0.1 mol•L-1Na2X溶液中,n(HX-)+2n(X2-)+n(H2X)=0.1 mol
-
H2X为二元弱酸,常温下,将NaOH溶液加入到H2X溶液中,在不同pH环境下,不同形态的粒子(酸、酸式酸根、酸根离子)的组成分数如图所示。下列说法正确的是
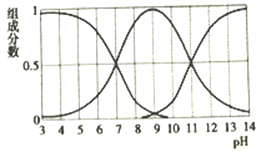
A.HX-的电离程度小于水解程度
B.在pH=7的溶液中HX-和X2-能大量共存
C.在pH=9时,H2X 与NaOH恰好完全中和
D.1L.0.1 mol•L-1Na2X溶液中,n(HX-)+2n(X2-)+n(H2X)=0.1 mol
-
H2X 和H2Y均为二元弱酸,常温下,将NaOH 溶液分别加到H2X 和H2Y的溶液中,在不同pH 环境下不同形态的粒子(即酸、酸式酸根、酸根离子)的组成分数如图所示:
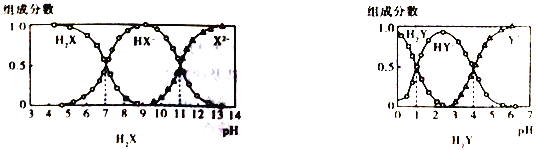
下列说法正确的是
A. 在pH=7的溶液中HX-、X2-、HY-和Y2-能大量共存
B. 向Na2X溶液中加入少量H2Y 溶液,发生反应:X2-+H2Y==HX-+HY-
C. 1L.0.1mol·L-1NaHY溶液中n(HY-)+2n(Y2-)+n(H2Y) =0.1mol
D. HX-的水解平衡常数为Kb=10-7
-
H2X 和H2Y均为二元弱酸,常温下,将NaOH 溶液分别加到H2X 和H2Y的溶液中,在不同pH 环境下不同形态的粒子(即酸、酸式酸根、酸根离子)的组成分数如图所示:
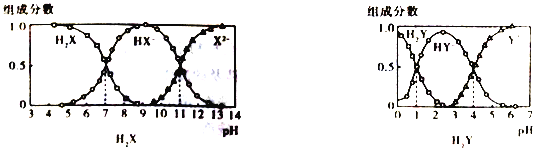
下列说法正确的是
A. 在pH=7的溶液中HX-、X2-、HY-和Y2-能大量共存
B. 向Na2X溶液中加入少量H2Y 溶液,发生反应:X2-+H2Y==HX-+HY-
C. 1L.0.1mol·L-1NaHY溶液中n(HY-)+2n(Y2-)+n(H2Y) =0.1mol
D. HX-的水解平衡常数为Kb=10-7
-
已知H2C2O4是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH 溶液,所得溶液中H2C2O4、HC2O4-、C2O42-的组成百分率与pH的关系如图所示,下列说法正确的是
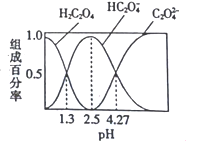
A. pH=4.27的溶液中:c(K+)+c(H+)=c(OH-)+3c(C2O42-)
B. 反应HC2O4-+H2O H2C2O4+OH-的平衡常数为10-4.27
H2C2O4+OH-的平衡常数为10-4.27
C. 向溶液中加入KOH溶液将pH 由1.3 调至4.27 的过程中水的电离程度先增大后减小
D. pH=2.5 的溶液中:c(H+)+2c(H2C2O4)=c(OH-)+c(C2O42-)
-
已知H2C2O4是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中H2C2O4、HC2O4—、C2O42—的组成百分率与pH的关系如图所示,下列说法正确的是
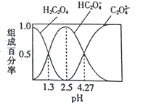
A. pH=4.27的溶液中:c(K+)+c(H+)=c(OH)+3c(C2O42—)
B. 反应HC2O4—+H2O H2C2O4+OH—的平衡常数为10-4.27
H2C2O4+OH—的平衡常数为10-4.27
C. 向溶液中加入KOH溶液将pH由1.3调至4.27的过程中水的电离程度先增大后减小
D. pH=2.5的溶液中:c(H+)+2c(H2C2O4)=c(OH—)+c(C2O42—)

H2CO3+OH-的平衡常数为








