室温下,某碳酸溶液中的H2CO3、HCO3-、CO32-的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是( )
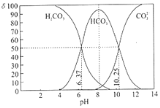
A.当溶液中δ(HCO3-)达到最大时:c(H2CO3)>c(CO32-)
B.Ka2(H2CO3)的数量级为10-11
C.调节溶液的pH由8~10的过程中减小
D.加入NaOH使溶液pH=9时,主要反应为HCO3-+OH-=CO32-+H2O
高三化学单选题中等难度题
室温下,某碳酸溶液中的H2CO3、HCO3-、CO32-的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是( )

A.当溶液中δ(HCO3-)达到最大时:c(H2CO3)>c(CO32-)
B.Ka2(H2CO3)的数量级为10-11
C.调节溶液的pH由8~10的过程中减小
D.加入NaOH使溶液pH=9时,主要反应为HCO3-+OH-=CO32-+H2O
高三化学单选题中等难度题
室温下,某碳酸溶液中的H2CO3、HCO3-、CO32-的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是( )

A.当溶液中δ(HCO3-)达到最大时:c(H2CO3)>c(CO32-)
B.Ka2(H2CO3)的数量级为10-11
C.调节溶液的pH由8~10的过程中减小
D.加入NaOH使溶液pH=9时,主要反应为HCO3-+OH-=CO32-+H2O
高三化学单选题中等难度题查看答案及解析
室温下,某碳酸溶液中的H2CO3、HCO3-、CO23-的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是( )
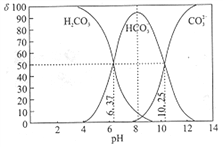
A. 当溶液中δ(HCO3-)达到最大时:c(H2CO3)>c(CO32-)
B. Ka2(H2CO3)的数量级为10-11
C. 调节溶液的pH由8~10的过程中减小
D. 加入NaOH使溶液pH=9时,主要反应为HCO3-+OH-=CO32-+H2O
高三化学单选题中等难度题查看答案及解析
25℃时,向H2CO3溶液中滴入NaOH溶液,溶液中H2CO3、HCO3-及CO32-的物质的量分数δ(X)随溶液pH的变化如图所示[δ(X)=[ ]×100%]。
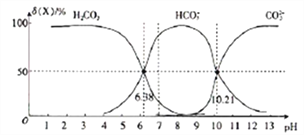
下列说法错误的是( )
A. H2CO3的一级电离平衡常数的对数值lgK1(H2CO3)=-6.38
B. pH=7时,c(HCO3-)>c(H2CO3)> c(CO32-)
C. pH=13时,c(Na+)+c(H+)=c(OH-)+2c(CO32-)
D. 25℃时,反应CO32-+H2OHCO3-+OH-的平衡常数对数值1gK=-3.79
高三化学单选题困难题查看答案及解析
25℃时,向H2CO3溶液中滴入NaOH溶液,溶液中H2CO3、HCO3-及CO32-的物质的量分数δ(X)随溶液pH 的变化如图所示{δ(X)=[c(X)/c(H2CO3)+c(HCO3-)+c(CO32-)]×100%}。
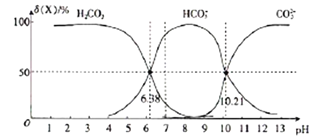
下列说法错误的是
A. H2CO3的一级电离平衡常数的对数值lgK1(H2CO3)=-6.38
B. pH=13时,c(Na+)十c(H+)=c(OH-)+2c(CO32-)
C. 25℃时,反应CO32-+H2OHCO3-+OH-的平衡常数对数值1gK=-3.79
D. pH=7时,c(HCO3-)>c(H2CO3)> c(CO32-)
高三化学单选题困难题查看答案及解析
已知25℃时,0.l mol/L的碳酸氢钠溶液的pH为8.4,则关于该溶液的叙述错误的是
A.滴加甲基橙溶液呈黄色 B.c(HCO3-)>c(H2CO3)>c(CO32-)
C.c(OH-)=c(H+)+c( H2CO3)-c (CO32-) D.加水稀释,c( H2CO3)/c(HCO3-)的比值减小
高三化学选择题中等难度题查看答案及解析
常温时,分别改变相同物质的量浓度的H2CO3和氨水的pH,H2CO3、HCO3-、CO32-物质的量分数 (δ)及NH3·H2O、NH4+的物质的量分数(δ)如下图所示(不考虑溶液中的CO2和NH3分子):
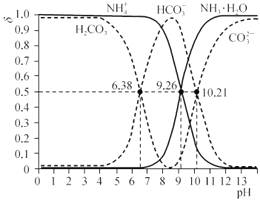
[已知δ=、δ=
]
下列说法正确的是
A. NH4HCO3溶液显酸性
B. pH=5时,c(HCO3-)>c(H2CO3) >c(CO32-)
C. lgK1(H2CO3)=6.38
D. HCO3-+ NH3·H2O=NH4++CO32-+H2O的lgK=-0.95
高三化学单选题中等难度题查看答案及解析
常温时,下列各溶液中,离子的物质的量浓度关系正确的是
A.饱和碳酸钠溶液中:c(Na+)= 2c(CO32-)+ 2c(HCO3-)+2c(H2CO3)
B.pH=2的醋酸中:c(H+)=0.02mol•L-1
C.0.1 mol•L-1氯化铵溶液中:c(H+)> c(OH-)> c(Cl-)> c(NH4+)
D.pH=12的NaOH溶液与等体积0.01 mol·L-1氯化铵溶液混合后所得溶液中:c(Na+) = c(NH4+)
高三化学选择题中等难度题查看答案及解析
室温下,下列溶液中粒子浓度关系正确的是
A.0.1mol/LNa2CO3溶液中:2c(Na+)=c(HCO3-)+ c(H2CO3)+ c(CO32-)
B.将0.2mol/LNaA溶液和某浓度的盐酸等体积混合所得中性溶液中:c(Na+)=c(A-) +c(Cl-) = 0.2mol/L
C.pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH>7
D.0.l mol·L-1氯化铵溶液滴加浓盐酸可能有c(NH4+) = c(H+)
高三化学选择题中等难度题查看答案及解析
下列有关电解质溶液中微粒的物质的量浓度关系错误的是( )
A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液: c(HCO3-) > c(CO32-)> c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7, c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
高三化学选择题简单题查看答案及解析
室温下,下列溶液中粒子关系关系正确的是
A.Na2CO3溶液:c(Na+)+c(H+)=c(H2CO3)+c(HCO3-)+c(OH-)+c(CO32-)
B.NaHSO3溶液:c(H+)+c(H2SO3)=c(HSO3-)+c(OH-)
C.KAl(SO4)2溶液:c(SO42-)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.NH4Cl和CaCl2混合溶液:c(Cl-)>c(Ca2+)>c(NH4+)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析