-
铜及其化合物在工业生产和日常生活中有着广泛的应用。
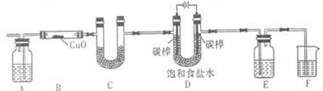
某化学小组拟采用如下装置(夹持和加热仪器已略去)来测定铜的相对原子质量,同时检验氯气的氧化性。

(1)装置甲中发生反应的化学方程式是:__________。
(2)已知装置甲中B处有黄绿色的气体产生,且 B连C ;则A连________(填写连接的字母)。
(3)乙装置的a瓶中溶液可以是________(填标号)
A 酸性KMnO4溶液 B CCl4溶液 C 滴加有KSCN溶液的FeCl2溶液 D 饱和食盐水
(4)在检查装置气密性后,加热丙装置硬质玻璃管里的CuO粉末前,还需要进行的操作为________。
(5)准确称量m g CuO进行实验,当CuO完全反应后测出b中增重n g。则Cu的相对原子质量为____________(只要求列出算式)。该实验方案的装置有不合理之处,若不加以改进会导致测定结果__________ (填“偏大”、“偏小”或“不变”)。
(6)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧CuCl2样品时,铜的焰色为__________(填标号)。
A 绿色 B 红色 C 紫色 D 黄色
(7)向CuCl2溶液中通人H2S气体,可产生CuS沉淀,反应离子方程式为:Cu2+ + H2S=CuS(s) + 2H+,则该反应的平衡常数K=_________(保留一位小数)。已知:CuS溶度积Ksp=1.0×10-36,H2S电离常数Ka1=1.3×10-7,Ka2=7.0×10-15。
-
完成下列填空:某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,并用电解产生的 H2 还原 CuO 粉末来测定 Cu 的相对原子质量,同时验证氯气的氧化性。

完成下列填空:
(1) 写出甲装置中反应的化学方程式______________________________。
(2) 为完成上述实验,正确的连接顺序为 A 连______,B连_____(填写接口字母)。
(3)乙装置中 a 试剂可以是_______________。
(4) 测定 Cu 的相对原子质量。将w g CuO 置于硬质玻璃管中,按以下两个方案测得的数据计算 Cu 的相对原子质量
| 方案 1 | 方案 2 |
| U 型管+固体 | 硬质玻璃管+固体 |
| 反应前的总质量/g | a | c |
| 反应后的总质量/g | b | d |
你认为较佳方案是_____________,另一个方案得到的 Cu 的相对原子质量会_______(选填“偏低”、或“偏高”)
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
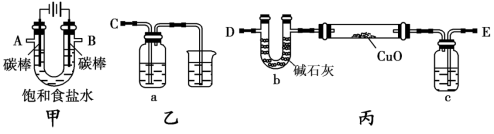
(1)写出甲装置中电解饱和食盐水的离子方程式 。
(2)为完成上述实验,正确的连接顺序为A连________;B连________(填写导管口字母)。
(3)对硬质玻璃管里的氧化铜粉末加热前,需要进行的操作为________________。
(4)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是______________,对应的现象为_______。
乙装置烧杯中发生反应的离子方程式是 。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案:精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g(假设CuO充分反应),实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答:________方案所测结果更准确。
你认为不合理的方案的不足之处是_____________________。
②若按合理方案测定的数据计算,Cu的相对原子质量为 。
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性.
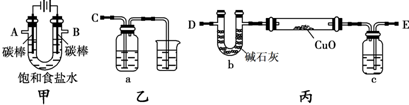
(1)写出甲装置中电解饱和食盐水的化学方程式______ 2NaOH+H2↑+Cl2↑
-
19.(12分)某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

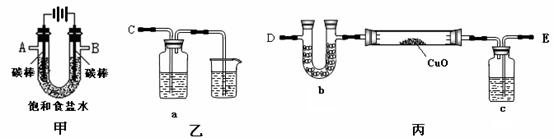
(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ________,作用是_______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量________。
-
(16分)
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性。
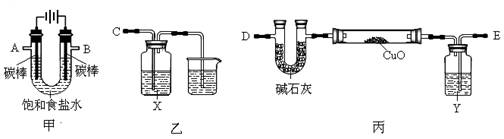
(1)写出甲中反应的化学方程式________。
(2)为完成上述实验,正确的连接顺序为A连______,B连______(填接口字母)。
(3)乙装置中X试剂可以是________,丙装置中Y试剂的作用是________。
(4)测定Cu的相对原子质量。
将w g CuO置于硬质玻璃管中,按以下两个方案测得的数据计算Cu的相对原子质量。
| 方案 质量[ | 方案一] | 方案二 |
| U型管+固体 | 硬质玻璃管+固体 |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
请你回答:
你认为方案 ________较佳,另一个方案得到的Cu的相对原子质量会________(填“偏低”、“偏高”)。按较佳方案计算,得到Cu的相对原子质量是________。
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性.
(1)D装置中电解饱和食盐水的离子反应方程式为:________
(2)为检验氯气的氧化性,则E装置的溶液可以是________.
A.淀粉碘化钾溶液 B.酸性KMnO4溶液 C.FeCl2溶液 D.Na2S溶液
(3)F装置的目的是________.
(4)为测定Cu的相对原子质量,某同学设计了如下的方案:
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g,实验完毕后(通过足量的氢气),通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量.
①对B装置中的氧化铜粉末加热前,需要进行的操作为________;
②A装置中盛放的试剂为________;
③根据测得结果进行计算,则Cu的相对原子质量为________.
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
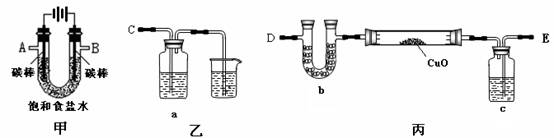
(1)为完成上述实验,正确的连接顺序为_______ 接A, B接_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液及对应的现象是________ ________ ________。
(4)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
请你分析并回答:你认为不合理的方案及其不足之处是________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量________。
-
某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,
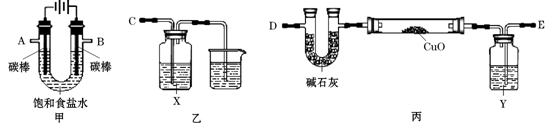
并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性。
(1)写出甲中反应的离子方程式 。
(2)为完成上述实验,正确的连接顺序为A连 ,B连 (填接口字母)。
(3)乙装置中X试剂可以是 ,丙装置中Y试剂的作用是 。
(4)测定Cu的相对原子质量。将w g CuO置于硬质玻璃管中,足量的H2与之充分反应后,按以下两个方案测得的数据计算Cu的相对原子质量。
| 方 案
质 量 | 方案一 | 方案二 |
| U型管+固体 | 硬质玻璃管+固体 |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
你认为方案 较佳,另一个方案得到的Cu的相对原子质量会 (填“偏低”、“偏高”)。按较佳方案计算,得到Cu的相对原子质量是 。
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu元素的相对原子质量,同时检验氯气的氧化性。

(1)为完成上述实验,正确的连接顺序为A连 ;B连 (填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为 。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ,作用是 。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案,精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g ,充分反应完全后。
甲方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
乙方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在 。
②按测得结果更准确的方案进行计算,Cu的相对原子质量是 。









