-
过滤在实验、生产、生活中有着广泛的应用。某研究性学习小组在实验室测定某含NaCl杂质的碳酸钠样品中Cl-的含量,其实验步骤如下:
①将100g样品溶于水得到溶液A。
②向A中加入稀HNO3酸化后,再加入沉淀剂B,使Cl-完全沉淀下来。
③进行如图所示操作,得到固体C,洗涤,干燥。
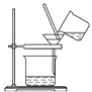
④称量得固体C的质量为2.87 g。
(1)沉淀剂B为________(填化学式)。
(2)向A中加入稀HNO3酸化的目的是_______________________。
(3)如何洗涤固体C: __________________。如果得到固体C后直接干燥、称量,会使样品中氯元素的质量分数________(填“偏大”“偏小”或“不变”)。
(4)该样品中氯元素的质量分数为________________。
-
铁及其化合物在生产、生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)绿矾是一种重要的硫酸盐,其化学式为FeSO4·7H2O,某化学兴趣小组通过实验探究来测定某绿矾样品中FeSO4·7H2O的含量,步骤如下:
i.称取上述样品9.0g,配成250 mL准确浓度的FeSO4溶液;
ii.最取25.00 mL上述溶液于锥形瓶中,用0.02000 mol·L-1的酸性KMnO4溶液与之完全反应,消耗KMnO4溶液30.00 mL(杂质不与KMnO4溶液反应)。
①配制FeSO4溶液时,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、___;配制溶液过程中未洗涤烧杯、玻璃棒,会造成所配溶液浓度____(填“偏大”、“偏小”或“无影响”)。
②步骤ii中反应的离子方程式为5Fe2++MnO4-+X=5Fe3++Mn2++4H2O,则X的化学式为______,其系数为______。
③该样品中FeSO4·7H2O的质量百分含量为____(计算结果保留1位小数)。
(2)工业上用氯化铁腐蚀铜箔制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁溶液,准备采用下列步骤:
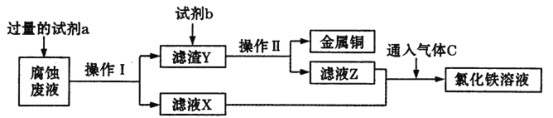
回答下列问题:
①请写出试剂a的化学式____,试剂b的名称____。
②滤液X、Z中均含有同一种溶质,它们转化为氯化铁溶液的离子方程式为________。
-
工业生产的纯碱中常含有少量的NaCl杂质。某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
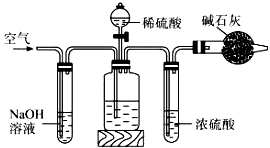
甲 乙 丙 丁
(1)甲装置反应的离子方程式是 。
(2)乙装置反应完成后,再通数分钟空气的作用是 。
(3)若取n g样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为m g,实验结束后称得干燥管丁的总质量为w g,则Na2CO3质量分数的计算式为 。
(4)若去掉丙装置,测得的CO2质量会 (填“偏大” “偏小”或“无影响”)。
(5)有同学认为在丁后面还要再连一个跟丁一样的装置,目的是 。
-
工业生产的纯碱中常含有少量的NaCl杂质,某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置,先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数。
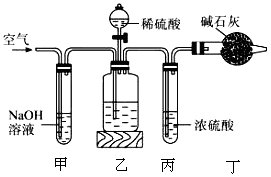
(1)甲装置反应的离子方程式是________________________。
(2)乙装置反应完成后,再通数分钟空气的作用是______________。
(3)若取ng样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为mg,实验结束后称得干燥管丁的总质量为wg,则Na2CO3质量分数的计算式为______________。
(4)若去掉丙装置,测得的CO2质量会______________(填“偏大”“偏小”或“无影响”)。
(5)有同学认为在丁后面还要再连一个跟丁一样的装置,目的是__________________。
-
碳酸钠与工农业生产、日常生活紧密相关。工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:方案一:沉淀分析法(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀_______(填操作)、洗涤、烘干、称量,洗涤沉淀的操作是____________________。方案二:气体分析法(2)把一定量的样品与足量盐酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用______________________,但选用该溶液后实验结果仍然不够准确,其原因是___________________。
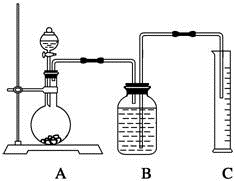
方案三:质量差分析法(3)把一定质量的样品和足量的稀硫酸反应,采用下图所示装置,通过称量反应前后盛有碱石灰的干燥管的质量,利用其质量差求算样品的纯度。
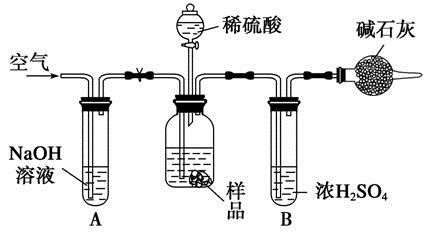
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g;②取n g样品装入广口瓶中;③检验装置的气密性;④缓慢鼓入空气数分钟,再称量干燥管质量为w g;⑤关闭止水夹;⑥打开止水夹;⑦缓慢加入稀硫酸至不再产生气体为止;⑧缓慢鼓入空气数分钟。Ⅰ.正确的操作顺序是(填序号):③→__________→⑥→________→⑤→________→⑦→_______→④。Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、“偏小”或“无影响”)。
-
某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | m |
| 4 | 20 | 8 |
根据实验数据计算:
(1)表中m的值是 。
(2)反应后所得溶液的质量为: g。
(3)求盐酸中溶质的质量分数(要求写出计算过程)。
-
碳酸钠俗称纯碱,在日常生产和生活中有着广泛的应用.某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl),然后再将NaHCO3制成Na2CO3.
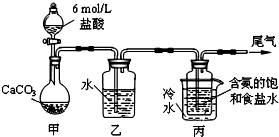
(1)装置乙的作用是__________.为防止污染空气,尾气中含有的__________需要进行吸收处理.
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________、__________、__________.
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究。取加热了t1min的NaHCO3样品19g完全溶于水制成溶液,然后向此溶液中不断滴加1mol•L﹣1的稀盐酸直到不再产生气泡,共消耗300ml稀盐酸.问该样品中NaHCO3和Na2CO3的物质的量之比是__________.
-
(10分)工业碳酸钠由于在生产过程中原料盐和工艺等的原因,常会含有Na2SO4 、NaCl中的一种或两种杂质。现有工业碳酸钠样品,某化学兴趣小组就工业碳酸钠中是否含有这两种杂质进行探究。
实验室有以下的仪器和药品可供使用:
烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹
1.0mol·L-1 H2SO4 溶液,1.0mol·L-1HNO3 溶液,1.0mol·L-1 HCl溶液, 1.0mol·L-1 NaOH溶液, 0.1mol·L-1 AgNO3溶液,0.1mol·L-1 BaCl2 溶液, 0.1mol·L-1 Ba(NO3)2溶液,蒸馏水
以下是部分实验探究过程:
⑴ 提出假设:根据题意,工业碳酸钠中含有杂质有________种可能的情况。
⑵ 设计实验方案,进行实验,写出实验操作步骤,预期的现象和涉及反应的离子方程式
| 编号 | 实验操作 | 预期现象 | 相关离子方程式 |
| ① | | | |
| ② | | | |
| ③ | | | |
-
制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀 (填操作名称)、洗涤、烘干、称量、计算.洗涤沉淀的具体操作是 .
方案二:把一定量的样品与足量硫酸反应后,用图1所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用 .图1装置中实验仪器a的名称是 .
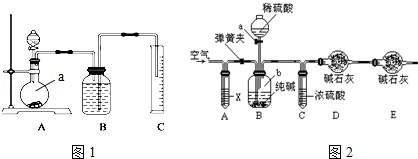
方案三:利用图2所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为33.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为35.6g.
(1)若④⑤两步的实验操作太快,则会导致测定结果 (填“偏大”或“偏小”).
(2)装置A中试剂X应选用 .
(3)E装置的作用是 .
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为 (结果保留小数点后一位).
-
制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀____________(填操作名称)、洗涤、烘干、称量、计算。洗涤沉淀的具体操作是_____________________________。
方案二:把一定量的样品与足量硫酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用_________________。下图装置中实验仪器a的名是_________________。
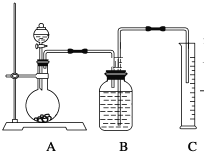
方案三:利用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:
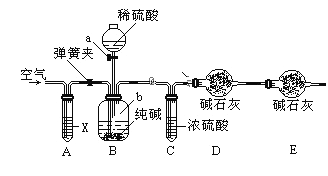
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为33.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为35.6g。
(1)若④⑤两步的实验操作太快,则会导致测定结果__________(填“偏大”或“偏小”)。
(2)装置A中试剂X应选用________________________。
(3)E装置的作用是_______________________________。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为___________(结果保留小数点后一位)。









