-
1,2二溴乙烷的制备原理是:CH3CH2OH CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
某课题小组用下图所示的装置制备1,2-二溴乙烷。

回答下列问题
(1)组装仪器后进行该实验前必须进行的操作是_________。
(2)装置B的作用是_______。
(3)三颈烧瓶内加入一定量的乙醇一浓硫酸混合液和少量粗砂,其加入粗砂目的是_______,仪器E的名称是_________________。
(4)装置C内发生的主要反应的离子方程式为__________________________。
(5)加热三颈烧瓶前,先将C与D连接处断开,再将三颈烧瓶在石棉网上加热,待温度升到约120℃时,连接C与D,并迅速将A内反应温度升温至160-180℃,从滴液漏斗中慢慢滴加乙醇一浓硫酸混合液,保持乙烯气体均匀地通入装有3.20ml液溴( 3g/cm3)和3ml水的D中试管,直至反应结束。
3g/cm3)和3ml水的D中试管,直至反应结束。
①将C与D连接处断开的原因是_____________________,
②判断反应结束的现象是______________________________。
(6)将粗品移入分液漏斗,分别用水、氢氧化钠溶液、水洗涤,产品用无水氯化钙干燥,过滤后蒸馏收集129-133℃馏分,得到7.896g1,2-二溴乙烷。1,2-二溴乙烷的产率为___________。
(7)下列操作中,不会导致产物产率降低的是________ (填正确答案的标号)
a.乙烯通入溴水时速率太快 b.装置E中的NaOH溶液用水代替.
c.去掉装置D烧杯中的水 d.实验时没有C装置 e. D中的试管里不加水
-
1,2二溴乙烷的制备原理是:CH3CH2OH CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
某课题小组用下图所示的装置制备1,2-二溴乙烷。
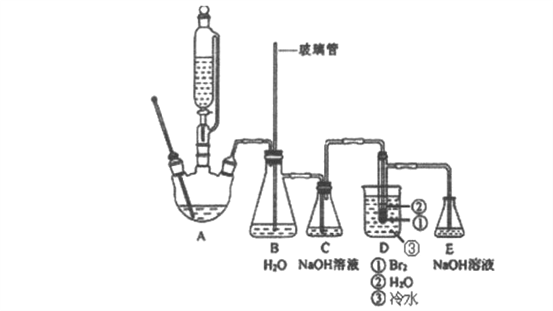
回答下列问题
(1)组装仪器后进行该实验前必须进行的操作是_________。
(2)装置B的作用是_______。
(3)三颈烧瓶内加入一定量的乙醇一浓硫酸混合液和少量粗砂,其加入粗砂目的是_______,仪器E的名称是_________________。
(4)装置C内发生的主要反应的离子方程式为__________________________。
(5)加热三颈烧瓶前,先将C与D连接处断开,再将三颈烧瓶在石棉网上加热,待温度升到约120℃时,连接C与D,并迅速将A内反应温度升温至160-180℃,从滴液漏斗中慢慢滴加乙醇一浓硫酸混合液,保持乙烯气体均匀地通入装有3.20ml液溴( 3g/cm3)和3ml水的D中试管,直至反应结束。
3g/cm3)和3ml水的D中试管,直至反应结束。
①将C与D连接处断开的原因是_____________________,
②判断反应结束的现象是______________________________。
(6)将粗品移入分液漏斗,分别用水、氢氧化钠溶液、水洗涤,产品用无水氯化钙干燥,过滤后蒸馏收集129-133℃馏分,得到7.896g1,2-二溴乙烷。1,2-二溴乙烷的产率为___________。
(7)下列操作中,不会导致产物产率降低的是________ (填正确答案的标号)
a.乙烯通入溴水时速率太快 b.装置E中的NaOH溶液用水代替.
c.去掉装置D烧杯中的水 d.实验时没有C装置 e. D中的试管里不加水
-
实验室制备1,2-溴乙烷的反应原理如下:
CH3CH2OH CH2=CH2+H2O CH2=CH2+Br2
CH2=CH2+H2O CH2=CH2+Br2 BrCH2CH2Br
BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
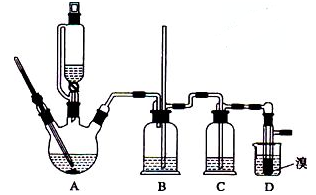
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度(g/cm3) | 0.79 | 2.2 | 0.71 |
| 沸点(℃) | 78.5 | 132 | 34.6 |
| 熔点(℃) | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___(填正确选项前的字母)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是______。
(3)在装置c中应加入____(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应己经结束的最简单方法是_______。
(5)将1, 2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____层(填“上”、“下”)。
(6)若产物中有少量未反应的Br2,最好用______(填正确选项前的字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用________的方法除去。
(8)反应过程中应用冷水冷却装置D,其主要目的是_________;但又不过度冷却(如用冰水),其原因是______________________。
-
实验室制备1,2—二溴乙烷的反应原理如下:CH3CH2OH CH2=CH2,CH2=CH2+Br2→CH2BrCH2Br
CH2=CH2,CH2=CH2+Br2→CH2BrCH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚;浓硫酸把乙醇氧化为CO2等。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示:

回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是__。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入__,(填序号)其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是__。
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__层(填“上”、“下”)
(5)若产物中有少量未反应的Br2,最好用___洗涤除去(填序号)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用___的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是__,但又不能过度冷却(如用冰水),其原因是___。
-
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH CH2===CH2↑+H2O
CH2===CH2↑+H2O
CH2===CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃脱水生成乙醚
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132. | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是________(填正确选项前的字母)。
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入________(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是__________________________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”或“下”)。
(5)若产物中有少量未反应的Br2,最好用________(填正确选项前的字母)洗涤除去。
a.水 b.氢氧化钠溶液
c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是__________________;但又不能过度冷却(如用冰水),其原因是___________________________________。
-
葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH CH2=CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
CH2=CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
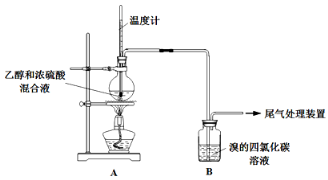
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| …… |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有 性。
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是 ;
②乙根据现象认为实验中产生的SO2和 ,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)
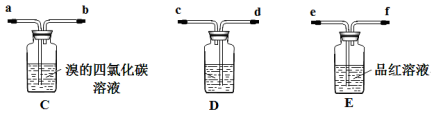
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是 ;乙设计的实验D中盛放的试剂是 ,装置连接顺序为 。
b.能说明确实是SO2使E中溶液褪色的实验是 。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是 。由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时发生的化学方程式 。

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤ mol·L-1。
-
葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ.已知:实验室制乙烯原理为CH3CH2OH CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| …… |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有___性。
(2)对产生的气体进行分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①写出实验室制取SO2的化学反应方程式是___;
②乙根据现象认为实验中产生的SO2和___,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
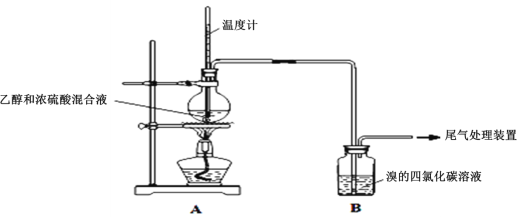
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是___;乙设计的实验D中盛放的试剂是___,装置连接顺序为___ (用仪器接口字母编号)。
b.能说明确实是SO2使E中溶液褪色的实验是___。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是___。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色。
Ⅱ.葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时溶液中离子浓度由大到小的排列顺序___。

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤___mol·L-1。
-
实验室制备1,2-二溴乙烷的原理:
CH3CH2OH  CH2=CH2↑+H2O
CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
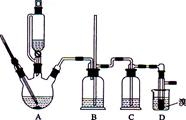
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm -3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在反应中若加热后发现未加沸石,应采取的正确方法是________________;判断该制备反应已经结束的最简单方法是_________________。
(2)装置C中应加入______________,吸收反应中产生的某些有影响的杂质气体(填写正确选项前的字母)
a.水 b.浓硫酸 c.NaOH溶液 d.KMnO4溶液
(3)装置B中竖直的长导管起安全管的作用,其原理是_____________。
(4)若产物中有少量Br2,最好用_________洗涤除去(填写正确选项前的字母)
a.水 b.乙醇 c.KI溶液 d.NaHSO3溶液
发生反应的化学方程为____________________。
(5)若产物中有少量副产物乙醚,可用__________的方法除去。
(6)反应过程中应用冷水冷却装置D,主要目的是__________________,但又不能过度冷却(如用冰水),其原因是_________________。
-
某研究性学习小组为合成1-丁醇,查阅资料得知下列合成路线:CH3CH=CH2+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO  CH3CH2CH2OH;CO的制备原理:HCOOH
CH3CH2CH2OH;CO的制备原理:HCOOH CO↑+H2O,并设计出原料气的制备装置如图所示。
CO↑+H2O,并设计出原料气的制备装置如图所示。
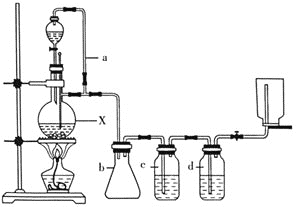
请填写下列空白:
(1)若用以上装置制备干燥纯净的CO,仪器X的名称是________;装置中b的作用是________;c和d中盛装的试剂分别是________,________。
(2)实验室现有浓硫酸、2-丙醇,请写出制备丙烯的化学方程式:________________________。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________(填序号)。
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:

试剂1为________,操作2为________,操作3为________。
-
实验室制乙烯通常采用95%的乙醇与浓硫酸 体积比为1:3混合加热到170℃方法制得,其制备原理可表示如下:CH3CH2OH+H2SO4(浓)
体积比为1:3混合加热到170℃方法制得,其制备原理可表示如下:CH3CH2OH+H2SO4(浓) CH3CH2OSO2OH+H2O①
CH3CH2OSO2OH+H2O①
CH3CH2OSO2OH(浓) CH2= CH2 + H2SO4②
CH2= CH2 + H2SO4②
(1)浓硫酸在乙烯生成中作用为 ______ ,反应①属于 ______ 反应,反应②属于 ______ 反应.
(2)此法在实际操作中由于浓H2SO4的用量大、比热容高,加热至170℃所需时间长,有人将乙醇和浓H2SO4的混合液加热到80℃时,一次性投入一些小碎块的生石灰,大大缩短了反应所需时间,提高了乙烯的产率,试用速率和平衡理论解释之 ______
(3)反应过程中乙醇常被炭化,使溶液有黑色物质出现,随着反应进行炭化现象越来越严重,同时还可使制得的乙烯气体中含有CO2、SO2等气体,为了减少反应过程中炭化现象又不影响乙烯的生成,下列措施合理的是 ______ .
A.调整乙醇和浓硫酸的体积比为1:4
B.调整乙醇和浓硫酸的体积比为1:2
C.用大理石代替碎瓷片
D.降低反应体系温度至140℃
E.用其他脱水剂(如P2O5)代替浓硫酸
(4)如图为有人设计确认混合气体中含有乙烯和二氧化硫的实验装置图.(下列试剂可供选择:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾)

A.①②③④中可盛放的试剂分别为①______ ; ②______ ;③ ______ ; ④ ______ ;
B.能说明二氧化硫气体存在的现象是 ______ ;
C.能确认含有乙烯的现象是 ______ 。
CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br

3g/cm3)和3ml水的D中试管,直至反应结束。




 CH2===CH2↑+H2O
CH2===CH2↑+H2O









