工业用强氧化剂PbO2来制备KClO4的工业流程如下:
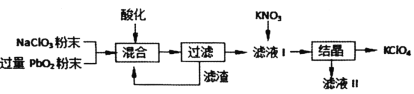
根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
高三化学单选题中等难度题
工业用强氧化剂PbO2来制备KClO4的工业流程如下:

根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
高三化学单选题中等难度题
工业用强氧化剂PbO2来制备KClO4的工业流程如下:

根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
高三化学单选题中等难度题查看答案及解析
工业用强氧化剂PbO2来制备KClO4的工业流程如下:

根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
高三化学单选题中等难度题查看答案及解析
工业用强氧化剂PbO2来制备KClO4的工业流程如下:

根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
高三化学单选题中等难度题查看答案及解析
高氯酸钾是一种白色粉末,可用作发烟剂、引火剂、氧化剂和化学分析试剂,医药工业用作解热和利尿等药剂。用PbO2来制备KClO4的工业流程如下:

(1)如图过滤装置中有两处明显错误,一处是未用玻璃棒引流,另一处是__。
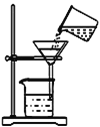
(2)写出NaClO3与PbO2反应的离子方程式_______________
(3)工业上可以利用滤液Ⅰ与KNO3发生反应制备KClO4的原因是______________
(4)用电解法也可以制备KClO4,在无隔膜、微酸性条件下,电解食盐水得到NaClO3溶液,再通过一系列转化和操作得到产品。
I.写出电解食盐水阳极电极反应式:______________________________
II.该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:准确称取5.7635 g样品溶于水中,配成250 mL溶液,从中取出25.00 mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-,反应为:
3KClO4+C6H12O6=6H2O+6CO2↑+3KCl,加入少量K2CrO4溶液作指示剂,用0.20mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积21.50 mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
①已知:Ksp(AgCl)=1.8×l0-10,Ksp(Ag2CrO4)=1.1×10-12,若终点时c(Cl-)=1.8×10-6 mol·L-1,则此时c(CrO42-)=______________mol·L-1。
②KClO4样品的纯度为______________。(精确到0.01%)
高三化学综合题困难题查看答案及解析
KIO3 是一种重要的无机化合物,常作为食盐中的补碘剂,工业上常用“KClO3 氧化法”制备 KIO3,其中酸化反应的产物有 KH(IO3)2、Cl2 和 KCl,流程如下:
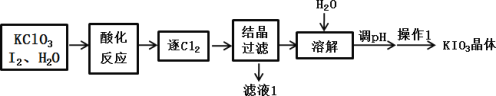
下列说法错误的是
A.酸化反应中还原产物为 KH(IO3)2
B.结晶过滤得到滤液 1 为 KCl 溶液
C.调节 pH 可加入 KOH,发生反应 KH(IO3)2+ KOH=2KIO3+ H2O
D.操作 1 可采用蒸发浓缩、冷却结晶的方法
高三化学单选题中等难度题查看答案及解析
四氧化三铅(Pb3O4,也可写作2PbO·PbO2)俗名“铅丹”或“红丹”,可用作防锈剂。工业上以废旧铅酸电池的铅膏(主要成分是PbSO4和PbO2)为原料制备Pb3O4的流程如下:
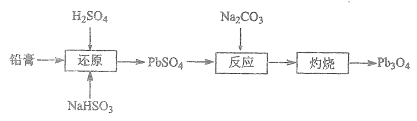
(1)“还原”时的化学方程式为__________。
(2)已知: Ksp[PbCO3]=1.5×10-13。 若使溶液中Pb2+的浓度小于1×10-5 mol/L,此时溶液中的c(CO32-)>_____mol/L。
(3)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6 mol/LHNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000mol/L Na2S2O3溶液滴定,终点时用去30.00mL。已知:I2+ 2 Na2S2O3 = Na2S4O6 + 2NaI。
①所加KI必须过量,原因是_____________________________。
②计算试样中Pb3O4的质量分数____________。(写出计算过程)
高三化学综合题中等难度题查看答案及解析
某实验小组用工业废弃固体(主要成分为Cu2S和Fe2O3)制备有关物质,整个流程如下图所示。请回答:

(1)气体a的化学式为________。
(2)溶液B加入硫酸酸化后再加入适宜氧化剂X得到溶液C,写出该反应的离子方程式________。
(3)制备硫酸铜溶液。常温下,O2、铜粉和稀硫酸三者在一起,几乎不反应,当加入溶液D后,随即生成硫酸铜。经理阅资料发现FeSO4对铜的氧化起催化作用。
A.第一步反应的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O,则第二步反应的郭子方程式为________。
B.⑦操作中,配制Fe2(SO4)3溶液时应注意________。
(4)操作⑧的目的是得到较纯的硫酸铜溶液。加入适宜试剂Y调节pH至铁元素全部沉淀(离子浓度小于10-5mol/L),然后再过滤,浓缩、结晶等,则pH至少调节为_____。
已知:Ksp[Cu(OH)2]≈1×10-22,Ksp[Fe(OH)2] ≈1×10-16,Ksp[Fe(OH)3] ≈1×10-38
(5)科学家发现纳米级的Cu2O在太阳光照射下可以催化分解水。
A.一定温度下,在2L密闭容器中加入纳米级Cu2O,通入2mol水蒸气,发生如下反应:
2H2O(g)=2H2(g)+O2(g) △H=+484kJ/mol
20min末测得n(O2)=0.16mol,则这段时间的反应速率υ(H2)=_________;该温度下,此反应的平衡常数表达式K=___________________。
B.已知:2Cu2O(s)+O2(g)=4CuO(s) △H=-292kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
请写出炭粉还原CuO(s)制备Cu2O(s)的热化学方程式_________________。
高三化学填空题极难题查看答案及解析
高锰酸钾是锰的重要化合物和常用的氧化剂,工业用软锰矿制备高锰酸钾的实验流程如下:
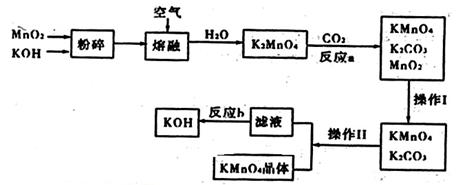
(1)上述流程中可以循环使用的物质有________(写化学式)
(2)从经济环保角度考虑,要完全反应b需要的试剂最好是________,并写出相应的化学方程式________。
(3)高锰酸钾是氧化还原滴定分析时常用的一种试剂,在滴定操作时,应将高锰酸钾标准溶液盛放在________(填“酸式”或“碱式”)滴定管中,用酸性KMnO4溶液滴定硫酸亚铁晶体(FeSO4?7H2O)溶液, 写出滴定反应的离子方程式________。
(4)KMnO4、双氧水、活性炭常用于饮用水的处理,但三者在联合使用时必须有先后顺序。①氧化反应:H2O2 - 2e- → 2H+ + O2↑;还原反应:MnO4- + 5e- + 8H+ → Mn2+ + 4H2O
写出该氧化还原反应的化学方程式________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投放,否则会发生KMnO4+ C+ H2O→MnO2 + X + K2CO3(未配平),其中X的化学式为________。
高三化学填空题简单题查看答案及解析
(8分)碘化钠是实验室中常用的分析试剂,工业上用铁屑还原法制备NaI的流程如下图:
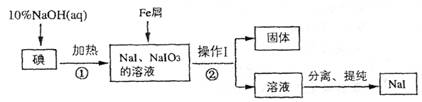
请回答下列问题:
(1) 判断反应①中碘是否反应完全的方法是_____________________
(2) 操作I的名称是_____________________;
(3) 反应①的离子方程式为_____________________
(4) 反应②中NaIO3被Fe单质还原为NaI,同时生成Fe(OH)3,该反应的化学方程式是______;
在该反应中若有99 g NaIO3被还原,则转移电子的物质的量为_______mol
高三化学填空题简单题查看答案及解析
工业废水中含有的和CrO42-会对水体产生很大的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:

下列说法不正确的是
A. ①中,酸化后发生反应为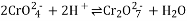
B. ②中,反应的氧化剂与还原剂的物质的量之比为3∶1
C. ③中,所得沉淀Cr(OH)3中含有Fe(OH)3
D. ③中调pH所用物质可以是NH3或Fe2O3
高三化学单选题中等难度题查看答案及解析