-
已知 可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:
可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:
实验一:探究亚硫酸与次氯酸的酸性强弱。选用的装置和药品如下。
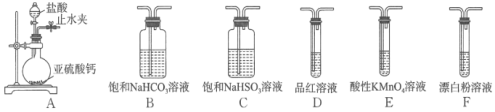
 装置A气密性检查的方法是________。
装置A气密性检查的方法是________。
 装置连接顺序为A、________、B、E、________、F,其中装置E中反应的离子方程式为________,通过现象________即可证明亚硫酸的酸性强于次氯酸。
装置连接顺序为A、________、B、E、________、F,其中装置E中反应的离子方程式为________,通过现象________即可证明亚硫酸的酸性强于次氯酸。
实验二:探究氯气与硫化氢气体混合能发生反应。选用的装置和药品如下。
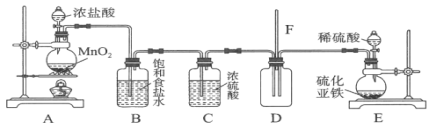
 通过现象________即可证明氯气与硫化氢发生了反应。
通过现象________即可证明氯气与硫化氢发生了反应。
 该装置存在一个不妥之处,你的改进措施为________。
该装置存在一个不妥之处,你的改进措施为________。
实验三:探究氯元素和硫元素非金属性强弱。
 为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是________。
为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是________。
A.实验一能说明硫元素非金属性强于氯元素 B.实验二能说明硫元素非金属性弱于氯元素
C.通过测定盐酸和氢硫酸的pH来判断非金属性强弱 D.已知硫化氢的沸点为 ,氯化氢的沸点为
,氯化氢的沸点为 ,则硫元素非金属性强于氯元素
,则硫元素非金属性强于氯元素
-
某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去)。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:
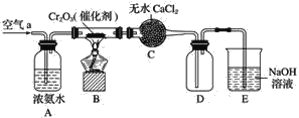
(1)B中发生反应的化学方程式是________________________________。
(2)证明氨气发生了催化氧化的现象是____________________________。
(3)写出(2)中反应的化学方程式______________________。
(4)装置E作用是________________________________________。
-
某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去)。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:

(1)B中发生反应的化学方程式是______________________________。
(2)证明氨气发生催化氧化的现象是________________,反应的方程式是________________。
(3)E中铜发生反应的离子方程式是________________________________。
(4)E中缓缓通入空气的目的是____________________________________。
-
某化学兴趣小组在学习“硫的化合物的某些性质”中,进行了如下实验:
【实验一】探究SO2的性质,
按下图所示装置进行实验。
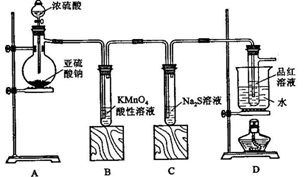
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为________;
(2)实验过程中,装置B、C中发生的现象分别是________、________,这些现象分别说明SO2具有的性质是________和________;装置B中发生反应的离子方程式为________;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象________
______________________________________________;
(4)该装置有一明显缺陷,请指明_______________________,并在框图内画出补充装置(注明药品)。

【实验二】验证足量锌与浓硫酸反应产生的气体成分是二氧化硫和氢气。按下图装置进行实验(锌与浓硫酸共热时产生的气体为X,且该装置略去)。试回答:
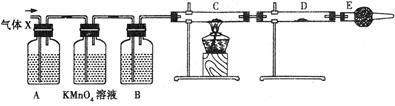
(5)A中加入的试剂可能是____________,作用是_______________;
B中加入的试剂可能是____________,作用是_______________;
E中加入的试剂可能是____________,作用是_______________。
(6)可以证明气体X中含有氢气的实验现象是:C中:____________,D中:__________;
-
某化学课外兴趣小组为探究足量的铜跟浓硫酸的反应情况,用下图所示装置进行有关实验。
已知:①SO2难溶于饱和亚硫酸氢钠溶液。②SO2能与酸性高锰酸钾溶液发生氧化还原反应。请回答下列问题:
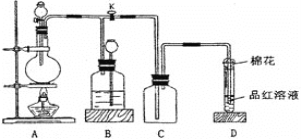
(1)装置A中发生的化学反应方程式为____________;此反应表明浓硫酸具有_________(填字母)。
a. 酸性 b. 脱水性 c. 强氧化性 d. 吸水性
(2)装置D中试管口放置的棉花中浸入__________溶液,其作用是_____________。
(3)装置B的作用是贮存多余的气体,B中应放置的液体是__________(填字母)。
a. 水 b. 饱和NaHSO3溶液 c. 酸性KMnO4溶液 d. NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是____________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
a. 银粉 b. 铁粉 c. BaCl2溶液 d. NaHCO3溶液
-
铁做为重要的金属元素与人类生产生活密切相关,某课外活动小组在学习了氧化剂和还原剂后,要利用实验验证铁及其化合物的性质。
请你帮助他们完成以下实验报告:
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片
(3)仪器:胶头滴管, (你认为本实验必不可少的一种玻璃仪器)。
(4)实验记录(虚线部分不必填写)
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | | Zn+Fe2+=Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | | 溶液由黄色变为蓝色 | | Fe3+具有氧化性 |
(5)实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
①根据以上结论判断,下列物质中既有氧化性,又有还原性的有: (填序号)。
A Cl2 B Na C Na+ D Cl- E NO2
②亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该加入少量 防止亚铁盐被氧化。
-
氮及其化合物与生产生活关系密切。请完成下列填空:
(1)某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
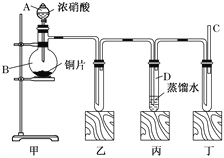
①装置甲中盛放浓硝酸的仪器A的名称是______, 装置丙中的试管内发生反应的离子方程式为:_______________________。
②为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是____________。
(2)NO在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为aL的试管盛满NO后倒扣于水槽中,再向试管中通入一定体积O2后,试管内气体的体积为试管容积的一半,则通入的O2的在相同条件下体积为_________。
A 0.75aL B 0.375aL C 0.625aL D 1.25aL
(3)实验室常用下图所示装置制取并收集氨气。
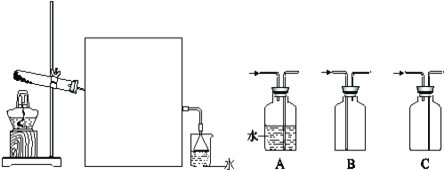
①实验室制取氨气反应的化学方程式为____________________________________;
②图中方框内收集氨气的装置可选用_________________(填字母序号);
③尾气处理装置中使用倒扣漏斗的作用是_________________________________。
(4)在盛有一定量浓硝酸的试管中加入6.4g的铜片发生反应。请回答下列问题:
①开始阶段,反应的化学方程式为____________________________________,后一阶段生成气体的颜色为____________,若整个反应过程共产生标准状况下气体2.24L,则反应过程中被还原的HNO3的物质的量为_______。
②反应结束后铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为____________________________________________________。
-
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图1所示装置进行有关实验.
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.
请回答:
(1)装置A中发生的化学反应方程式为______ CuSO4+SO2↑+2 H2O
-
某课外兴趣小组为探究铜跟浓硫酸反应情况,用下图所示装置进行实验。已知:①SO2难溶于饱和亚硫酸氢钠溶液;②SO2能与酸性高锰酸钾溶液发生氧化还原反应使之褪色(化学方程式为5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4)。
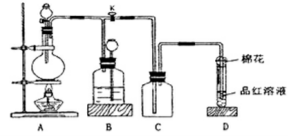
回答下列问题(注:E为止水夹,F为旋塞):
(1)检查A装置的气密性的方法 。
(2)装置A中反应的化学方程式为 。
(3)装置D中试管口放置的棉花应蘸有NaOH溶液,
其作用是 。
(4)装置B具有贮存气体的作用。当D处有明显的现象后,关闭旋塞F并移去酒精灯,由于余热的作用,A处仍有气体产生,此时B中的现象是 ,B中应放置的液体是(填字母) 。
A. 水 B. 饱和NaHSO3溶液 C. 酸性KMnO4溶液 D. NaOH溶液
(5)该小组学生做了如下实验:取一定质量的铜片和一定体积18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中没有铜片剩余。往反应后的溶液中加入足量的BaCl2溶液,获得沉淀3.495 g;产生的气体恰好使200ml 0.01mol·L-1的酸性高锰酸钾溶液褪色,则实验中取用的硫酸的物质的量为 。
-
某学习小组以氢氧化钡、水、硫酸为实验对象探究离子反应发生的条件。
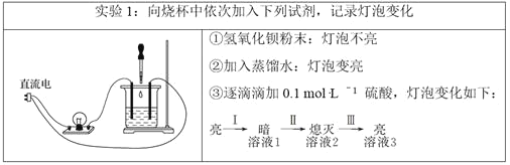
(1)氢氧化钡与硫酸在溶液中能发生________(填字母)。
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加水后,灯泡变亮的原因是氢氧化钡发生了_______________________________。
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因_________________________________。
(4)查阅有关物质溶解度数据如下表:

比较溶液1、溶液2中c(SO42-)的大小:______>______。
(5)实验2:用硫酸钠溶液替代稀硫酸,重复实验进行对照。
①硫酸钠溶液的浓度是________。
②加入硫酸钠溶液过程中灯泡不熄灭,原因是________________________________。
可以和HClO发生氧化还原反应。某学习小组对氯、硫及其化合物的性质进行下列实验探究活动:

装置A气密性检查的方法是________。
装置连接顺序为A、________、B、E、________、F,其中装置E中反应的离子方程式为________,通过现象________即可证明亚硫酸的酸性强于次氯酸。

通过现象________即可证明氯气与硫化氢发生了反应。
该装置存在一个不妥之处,你的改进措施为________。
为探究氯元素和硫元素的非金属性强弱,下列实验方案或有关说法中正确的是________。
,氯化氢的沸点为
,则硫元素非金属性强于氯元素










