-
按要求回答下列问题。
(1)SO2是形成酸雨的罪魁祸首。 64 g SO2的物质的量为 ,在标准状况下的体积约为 ,所含原子数为 。
(2)写出除去下列物质所含杂质(括号内为杂质)所用的试剂或方法:
①Na2CO3固体(NaHCO3) ②FeCl3溶液(FeCl2)
③Mg粉(Al) ④CO2(SO2)
高一化学填空题中等难度题查看答案及解析
-
(1)目前,我国火力发电厂燃料主要是煤.煤燃烧会排放出SO2和NO2,这些气体不仅污染空气,而且与空气中的物质反应后,生成的物质溶于雨水,会形成“酸雨”.请按要求回答下列问题:
①二氧化硫与空气中水份反应生成亚硫酸(H2SO3),亚硫酸易与氧气反应生成硫酸.其中亚硫酸与氧气的化学方程式是______.
②NO2是一种红棕色气体.在盛有NO2的集气瓶中放入一块活性炭,过一会儿,瓶内红棕色变淡甚至消失,活性炭具有的这种性质叫做______.
③对于SO2和NO2,小余同学归纳出了如下一些共同点,其中正确的是______
A.都是非金属氧化物 B.硫元素和氮元素化合价都为+2价
C.同温同压下密度相等 D.常温常压下都是有颜色的气体
(2)十.一节放假结束后,小王来到实验室,发现一瓶氢氧化钠固体敞放着,这引起了她的研究欲望.
(提出问题)氢氧化钠是否变质?若发生变质,其程度如何?
(查阅资料)碳酸钠水溶液显碱性,氯化钠、氯化钙水溶液显中性.
(进行试验)Ⅰ.取样品少许,加入稀盐酸有气泡产生;
Ⅱ.取样品少许,加水溶解后,滴入酚酞显红色;
Ⅲ.按如图所示过程,进一步实验:
请你与小王同学一道完成下列问题的分析解答:
①氢氧化钠变质的化学反应方程式是______.
②开始两个步骤中的实验操作a、b,都要使用的两件玻璃仪器是______.
③步骤b中,不能用Ca(OH)2代替CaCl2的原因是(用化学方程式表示原因):______.
④根据上述实验,若直接测定wg样品中氢氧化钠的质量而求其质量分数,须测定的数据是______
A.测定沉淀A 的质量
B.溶液B蒸发溶剂,测定残留固体的质量
C.溶液B与稀硫酸中和,测定消耗H2SO4的质量.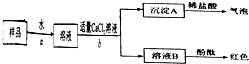
高一化学解答题中等难度题查看答案及解析
-
请按要求,回答下列问题:
(1)相同物质的量的SO2和SO3,所含O的质量之比为________。
(2)标准状况下,4.48 L 的NH3中,所含H的数目约为________。
(3)标准状况下,1 mol H2O、11.2 L CH 4、8 g O2中,体积最小的是________。
(4)某气体的质量为3.4 g,含有6.02×1022个分子,则该气体的摩尔质量为________。
(5)10 mL 0.5 mol·L-1 Al (NO3)3 溶液中NO3-的物质的量浓度为________。
(6)标准状况下,89.6 L HCl 气体溶于1 L水(ρ = 1 g·mL-1)中,所得盐酸的密度为1.146 g·mL-1,则此盐酸的物质的量浓度为________。
高一化学计算题中等难度题查看答案及解析
-
某燃煤发电厂的废气中有SO2,它是形成酸雨的罪魁之一。处理SO2一般用生石灰或类似物质来吸收。下图是处理该废气的装置示意图。
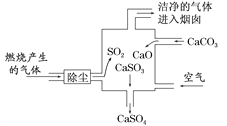
下列说法不正确的是( )
A. 此过程中既有分解反应,也有化合反应
B. CaSO4既是氧化产物,又是还原产物
C. 使用此废气处理装置可减少酸雨的形成
D. 理论上整个过程每转移电子1 mol,会对应生成1 mol CO2
高一化学单选题中等难度题查看答案及解析
-
某燃煤发电厂的废气中有SO2,它是形成酸雨的罪魁之一。处理SO2一般用生石灰或类似物质来吸收。下图是处理该废气的装置示意图。下列说法不正确的是
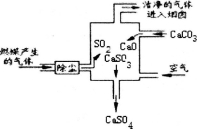
A.此过程中既有分解反应,也有化合反应
B.CaSO4既是氧化产物,又是还原产物
C.使用此废气处理装置可减少酸雨的形成
D.理论上整个过程每转移电子1mol,会对应生成1molCO2
高一化学选择题中等难度题查看答案及解析
-
二氧化硫是形成酸雨的“罪魁祸首”,为了保护环境,应减少二氧化硫在大气中的排放。请回答下列问题:
(1)二氧化硫与水反应可生成亚硫酸,那么二氧化硫是电解质还是非电解质?__________。
(2)工业尾气中的二氧化硫常用氢氧化钠溶液吸收,生成亚硫酸钠或亚硫酸氢钠:
①亚硫酸钠溶于水的电离方程式是______________________;
②亚硫酸氢钠溶于水的电离方程式是______________________。
(3)二氧化硫在催化剂的作用下可被氧气氧化成三氧化硫,三氧化硫与水反应生成硫酸:
①三氧化硫是电解质还是非电解质?__________;
②氧气属于电解质或非电解质吗?__________。
(4)三氧化硫与氢氧化钠溶液反应可生成硫酸氢钠:
①硫酸氢钠溶于水的电离方程式是________________________;
②硫酸氢钠是酸类物质吗?__________。
高一化学填空题中等难度题查看答案及解析
-
硫酸型酸雨的形成原理可简化表示如下:

回答下列问题:
(1)A物质的化学式_________,B物质的化学式_________。
(2)根据SO2的性质,可让工厂的烟道气通过________除去SO2,达到减少污染的目的。
(3)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:

注 溶液的pH越大,H+的物质的量浓度就越小。
①雨水样品的pH变化的原因是____________(用化学方程式表示)。
②如果将刚取样的上述雨水和用氯气消毒的自来水相混合,pH将_________(填“增大”“减小”或“不变”),原因是(用化学方程式表示):_____________。
(4)你认为减少酸雨产生可采用的措施是_________(填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
高一化学综合题中等难度题查看答案及解析
-
下列叙述正确的是
A.1 mol H2O的质量为18g
B.摩尔是表示物质微粒数目的一个物理量
C.3.01×1023个SO2分子的质量为64g
D.标准状况下,1 mol任何物质体积均约为22.4L
高一化学选择题中等难度题查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为 NA
C. 标准状况下,22.4 L H2O的分子数为NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
高一化学单选题简单题查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为 NA
C. 标准状况下,22.4 L H2O的分子数为NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
高一化学单选题简单题查看答案及解析