常温下,HNO2的电离平衡常数为K=4.6×10-4(已知2.14),向20mL0.01mol・L-1HNO2溶液中逐滴加入相同浓度的NOH溶液,测得混合液的 pH随NaOH溶液体积的变化如图所示,下列判断正确的是
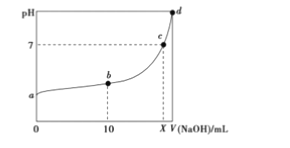
A. X=20
B. a、b、c、d四点对应的溶液中水的电离程度逐渐减小
C. a点溶液中c(H-)=2.14×10-3mol・L-1
D. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>c(NO2-)
高三化学单选题中等难度题
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知2.14),向20mL0.01mol・L-1HNO2溶液中逐滴加入相同浓度的NOH溶液,测得混合液的 pH随NaOH溶液体积的变化如图所示,下列判断正确的是

A. X=20
B. a、b、c、d四点对应的溶液中水的电离程度逐渐减小
C. a点溶液中c(H-)=2.14×10-3mol・L-1
D. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>c(NO2-)
高三化学单选题中等难度题
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知2.14),向20mL0.01mol・L-1HNO2溶液中逐滴加入相同浓度的NOH溶液,测得混合液的 pH随NaOH溶液体积的变化如图所示,下列判断正确的是

A. X=20
B. a、b、c、d四点对应的溶液中水的电离程度逐渐减小
C. a点溶液中c(H-)=2.14×10-3mol・L-1
D. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>c(NO2-)
高三化学单选题中等难度题查看答案及解析
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知=2.14),向20 mL 0.01 mol·L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )

A. HNO2的电离方程式为HNO2===NO+H+
B. a点H2O电离出的c(H+)=2.14×10-3 mol·L-1
C. b点溶液中离子浓度大小关系为c(NO)>c(Na+)>c(H+)>c(OH-)
D. X值等于20
高三化学单选题中等难度题查看答案及解析
常温下,HNO2的电离平衡常数为K=4.6×10-4(已知=2.14),向20 mL 0.01 mol·L-1HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是
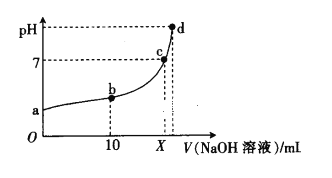
A. X=20
B. a点溶液中c(H+)=2.14×10-3 mol·L-1
C. a、b、c、d四点对应的溶液中水的电离程度逐渐减小
D. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>c()
高三化学单选题中等难度题查看答案及解析
常温下, HNO2的电离平衡常数为K=4.6×10-4(已知, 向20ml 0.01mol.L-1HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
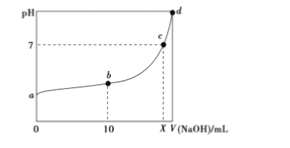
A. X=20
B. a、b、c、d四点对应的溶液中水的电离程度逐渐减小
C. a点的溶液中c(H+)=2.14×10-3mol·L-1
D. b点溶液中微粒浓度的大小关系为c(HNO2)>c(Na+)>(NO2)
高三化学单选题困难题查看答案及解析
常温下,已知醋酸的电离常数为1.75×10-5,向20mL0.01mol·L-1CH3COOH溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液中水电离的c(H+)随加入NaOH溶液的体积变化如图所示,下列说法正确的是(已知=4.2)
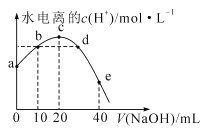
A.b、d两点溶液的pH相同
B.b点溶液中离子浓度大小顺序是:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.e点所示溶液中,c(Na+)=2[c(CH3COO-)+c(CH3COOH)]=0.005mol/L
D.a点坐标为(0,2.4×10-11)
高三化学单选题中等难度题查看答案及解析
常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1HA溶液所得滴定曲线如图。下列说法不正确的是
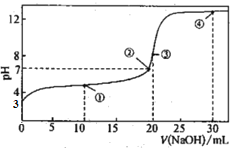
A.HA的电离平衡常数Ka=10-5
B.点①所示的溶液中:2c(Na+)=c(A-)+c(HA)
C.点③所示的溶液中:c(HA)>c(OH-)-c(H+)
D.点④所示的溶液中:2c(OH-)-2c(H+)=c(A-)+3c(HA)
高三化学单选题困难题查看答案及解析
若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
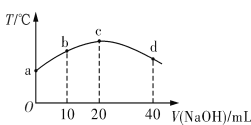
A. HNO2的电离平衡常数:c点>b点
B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c点混合溶液中:c(OH-)>c(HNO2)
D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
高三化学单选题困难题查看答案及解析
若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
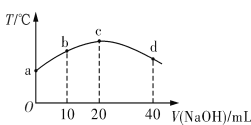
A. HNO2的电离平衡常数:c点>b点
B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c点混合溶液中:c(OH-)>c(HNO2)
D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
高三化学单选题困难题查看答案及解析
若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
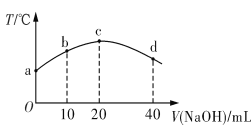
A. HNO2的电离平衡常数:c点>b点
B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c点混合溶液中:c(OH-)>c(HNO2)
D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
高三化学单选题困难题查看答案及解析
若往20 mL 0.01 mol·L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示。下列有关说法不正确的是
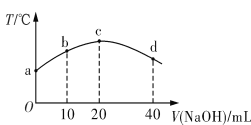
A. HNO2的电离平衡常数:c点>b点
B. b点混合溶液显酸性:c(Na+)>c(NO2-)>c(H+)>c(OH-)
C. c点混合溶液中:c(OH-)>c(HNO2)
D. d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+)
高三化学单选题困难题查看答案及解析