高氯酸在化工生产中有广泛应用,工业上以NaClO4为原料制备高氯酸的原理如图所示.下列说法正确的是
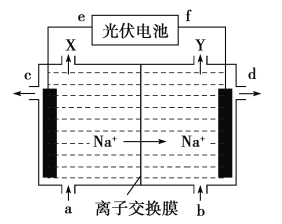
A. 上述装置中,f极为光伏电池的正极
B. 阴极的电极反应为2H2O-4e- =4H++O2↑
C. d处得到较浓的NaOH 溶液,c处得到HClO4
D. 若转移2mol电子,理论上生成100.5gHClO4
高三化学单选题中等难度题
高氯酸在化工生产中有广泛应用,工业上以NaClO4为原料制备高氯酸的原理如图所示.下列说法正确的是

A. 上述装置中,f极为光伏电池的正极
B. 阴极的电极反应为2H2O-4e- =4H++O2↑
C. d处得到较浓的NaOH 溶液,c处得到HClO4
D. 若转移2mol电子,理论上生成100.5gHClO4
高三化学单选题中等难度题
高氯酸在化工生产中有广泛应用,工业上以NaClO4为原料制备高氯酸的原理如图所示.下列说法正确的是

A. 上述装置中,f极为光伏电池的正极
B. 阴极的电极反应为2H2O-4e- =4H++O2↑
C. d处得到较浓的NaOH 溶液,c处得到HClO4
D. 若转移2mol电子,理论上生成100.5gHClO4
高三化学单选题中等难度题查看答案及解析
水合肼是重要的化工原料,广泛地应用于医药、农药、染料等。其在工业上常利用尿素氧化法制备,反应原理为
。某同学在实验室模仿工业制备方法制备
。回答下列问题:
(1)溶液的制备,装置如图所示。
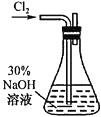
①实验室利用二氧化锰和浓盐酸制备氯气的离子方程式为_________________。
②实验需要用到的NaOH溶液,配制该溶液所需玻璃仪器除量筒外还有_____。
③锥形瓶中发生反应的化学方程式为___________________________。
④因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液中NaOH的浓度。利用所提供试剂,设计实验方案:____________________________所提供的试剂有:溶液、
溶液、
的盐酸、酚酞试液。
(2)水合肼的制备,装置如图所示。
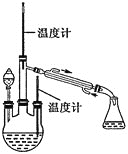
实验步骤:控制反应温度加热装置已省略
,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应后,持续加热蒸馏三颈烧瓶内的溶液,收集
馏分于锥形瓶中。已知
。分液漏斗中的溶液是_________
填“
溶液”或“NaOH和NaClO混合溶液”
,选择的理由是___________。
(3)馏分中水合肼含量的测定。
称取馏分,加入适量的
固体
滴定过程中,控制溶液的pH保持在
左右
,加水配成
溶液,移出
,用
的
溶液滴定。实验测得消耗
溶液的平均值为
,馏分中水合肼
的质量分数为_____。
已知:
高三化学实验题中等难度题查看答案及解析
亚硝酸钠是工业盐的主要成分,在漂白、电镀等方面应用广泛。已知:室温下,
,以木炭、浓硝酸、
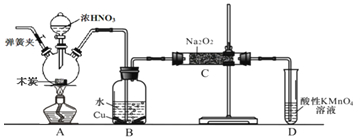
为主要原料制备亚硝酸钠的装置如图所示
部分夹持装置已略去
。下列说法正确的是( )
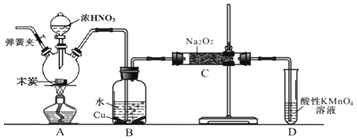
A.可以将B中药品换成NaOH溶液
B.应在B、C之间加一个盛放无水的干燥管
C.实验开始前先向装置中通入,实验结束时先停止通入
再熄灭酒精灯
D.装置D可用于尾气处理,标况下每吸收 L的尾气消耗
mol高锰酸钾
高三化学单选题中等难度题查看答案及解析
亚硝酸钠是工业盐的主要成分,在漂白、电镀等方面应用广泛。已知:室温下,
,以木炭、浓硝酸、
为主要原料制备亚硝酸钠的装置如图所示
部分夹持装置已略去
。下列说法正确的是( )
A.可以将B中药品换成NaOH溶液
B.应在B、C之间加一个盛放无水的干燥管
C.实验开始前先向装置中通入,实验结束时先停止通入
再熄灭酒精灯
D.装置D可用于尾气处理,标况下每吸收 L的尾气消耗
mol高锰酸钾
高三化学单选题中等难度题查看答案及解析
膜技术原理在化工生产中有着广泛的应用,有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。下列说法不正确的是
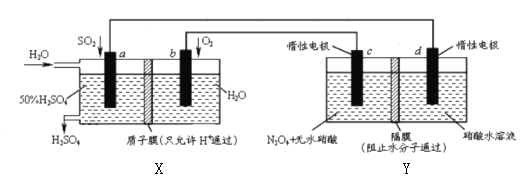
A. X是原电池,能够生产硫酸;Y是电解池,能够生产N2O5
B. C电极的电极反应方程式为N2O4+2HNO3-2e-=2N2O5+2H+
C. 当电路中通过2mole,X、Y中各有2molH+从左边迁移到右边
D. 电路中电子流向为ad
c
b
a形成闭合回路
高三化学单选题中等难度题查看答案及解析
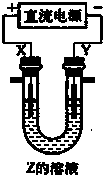
重铬酸钾(K2Cr2O7)具有强氧化性,是一种重要的化工原料,广泛应用于制革、印染、电镀等工业。以铬酸钾(K2CrO4)和氢氧化钾为原料,用电化学法制备重铬酸钾的实验装置如图所示。已知水溶液中存在平衡:2CrO42-+2H+Cr2O72-+H2O。下列说法中正确的是
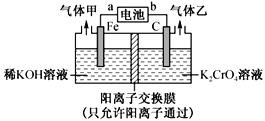
A. 气体甲和乙分别为O2和H2
B. 该装置中阴极区的pH减小
C. Fe电极反应式4OH--4e-=O2↑+2H2O
D. 当铬酸钾的转化率达到80%时,右池中=
高三化学单选题中等难度题查看答案及解析
碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:饱和
.
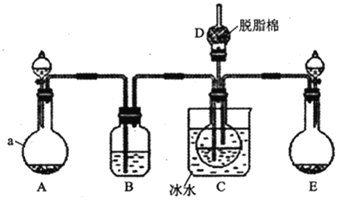
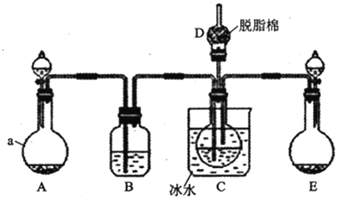
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
请回答下列问题
(1)仪器a的名称是______.
(2)中应选用的药品是______
填序号
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)中脱脂棉应浸润的试剂是______
填写字母编号
浓硫酸
稀硫酸
氢氧化钠溶液
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度假设晶体中不含碳酸盐杂质
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

操作Ⅲ中的方法是______,______,______
所得晶体中碳酸氢钠的纯度是______
不必化简
高三化学实验题中等难度题查看答案及解析
碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:饱和
.
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
请回答下列问题
(1)仪器a的名称是______.
(2)中应选用的药品是______
填序号
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)中脱脂棉应浸润的试剂是______
填写字母编号
浓硫酸
稀硫酸
氢氧化钠溶液
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度假设晶体中不含碳酸盐杂质
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

操作Ⅲ中的方法是______,______,______
所得晶体中碳酸氢钠的纯度是______
不必化简
高三化学实验题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
氯酸钾在工业上具有广泛的应用,某研究性学习小组利用如图所示的实验装置制备氯酸钾。回答下列问题:

(1)写出装置C中发生反应的离子方程式:_______________________。
(2)若无B装置,则装置C中氯酸钾的产率将___________ (填“提高” “降低”或“无影响”)。
(3)在不同条件下KC1O3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0. 20mol • L-1KI/mL | V1 | 1.0 | 1.0 | 1.0 |
| KC1O3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol • L-1H2SO4/mL | 0 | 3.0 | V2 | 9.0 |
| 蒸馏水 | 9.0 | V3 | 3.0 | 0 |
| 实验现象 |
①实验设计表中V1=____________; V2 =_____________; V3 =_______________。
②设计1号试管实验的作用是_________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__________________。
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂C1O2,该反应的化学方程式为______________________ ;利用该反应原理,若工业上使用122.5吨KClO3与足量的Na2SO3反应,生成的ClO2用于除去工业废水中的Mn2+,可得到MnO2固体165吨,则该反应的产率约为___________。
高三化学实验题困难题查看答案及解析