汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是
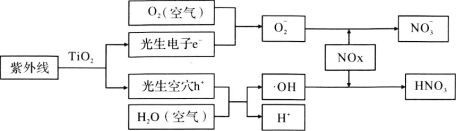
A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
高三化学单选题中等难度题
汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是

A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
高三化学单选题中等难度题
汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是
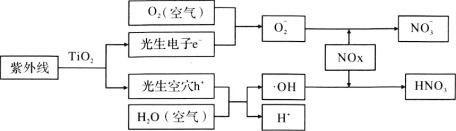
A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
高三化学单选题中等难度题查看答案及解析
汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现TiO2的混凝土或沥青可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是

A. 部分光能转变为化学能
B. 消除总反应为:4NOx+(5-2x)O2+2H2O4HNO3
C. 使用纳米TiO2,产生的光生电子和空穴更多,NOx消除效率更高
D. 1 mol比1 mol羟基(·OH)多9NA个电子(NA为阿伏伽德罗常数)
高三化学单选题中等难度题查看答案及解析
科学家研究发现纳米TiO2的混凝土可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是( )
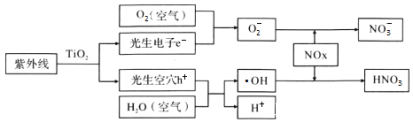
A.纳米TiO2作催化剂,NOx消除效率更高
B.NOx消除总反应为:4NOx+(5-2x)O2+2H2O4HNO3
C.1mol羟基(-OH)比1molO2少8NA个电子(NA为阿伏加德罗常数)
D.纳米TiO2属于胶体,能产生丁达尔现象
高三化学多选题中等难度题查看答案及解析
当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:
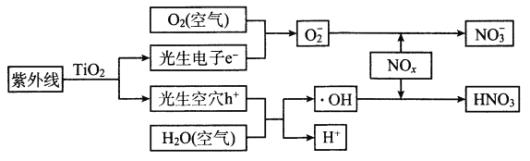
下列关于该“消除”过程的叙述不正确的是
A. 部分光能转变为化学能
B. 消除总变化为NOx+O2+H2O→HNO3
C. 消除反应能全天候发生
D. 使用纳米TiO2的消除效率更高
高三化学单选题简单题查看答案及解析
当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下
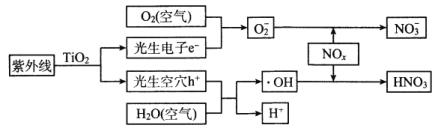
下列关于该“消除”过程的叙述不正确的是
A. 部分光能转变为化学能
B. 消除总变化为NO2+O2+H2O→HNO3
C. 消除反应能全天候发生
D. 使用纳米TiO2的消除效率更高
高三化学单选题中等难度题查看答案及解析
汽车尾气的主要成分有CO、SO2、氮氧化物等,科学家们-直致力于污染物的有效消除。
(1)利用氨水可以将SO2、氮氧化物吸收,原理如下图所示。
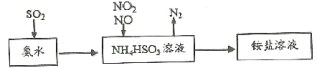
请写出NO2和NO按体积比1:1被吸收时反应的离子方程式_________________________。
(2)科研工作者目前正在尝试以二氧化钛(TiO2)催化分解汽车尾气的研究。
①己知:2NO(g)+O2(g)=2NO2(g) △H1=-113.0kJ· mol-1
2SO2(g)+O2(g)=2SO3(l) △H2=-288.4kJ· mol-1
N2(g)+O2(g)2NO(g) △H3=+180.5kJ· mol-1
请判断反应NO2(g)+SO2(g)=NO(g)+SO3(l) △H4,在低温下能否自发进行_______(填“能”或“否”),理由是__________________________。
②己知TiO2催化尾气降解原理为:
2CO(g)+O2(g)2CO2(g);2H2O(g)+4NO(g)+3O2(g)
4HNO3(g)
i、在一定条件下,模拟CO、NO的降解,得到降解率(即转化率)随时间变化如图所示,
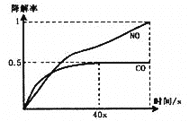
反应40秒后检测到混合气体中N2浓度上升,HNO3气体浓度有所降低,请用化学方程式并结合化学反应原理知识解释可能的原因____________________________________________。
ii,沥青混凝土也可降解CO。如图为在不同颗粒间隙的沥青混凝土(α、β型)在不同温度下,反应相同时间,测得CO降解率变化。结合图表回答下列问题:
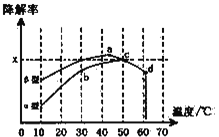
已知在50℃时在α型沥青混凝土容器中,平衡时O2浓度为0.01mol·L-1,求此温度下CO降解反应的平衡常数____________________(用含x的代数式表示);以β型沥青混凝土颗粒为载体,将TiO2改为催化效果更好的TiO2纳米管,在10~60℃范围内进行实验,请在图中用线段与阴影,仿照“示例”描绘出CO降解率随温度变化的曲线可能出现的最大区域范围(示例:)_____________________。
(3)利用如图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2,b极的电极反应式为_______________________________。
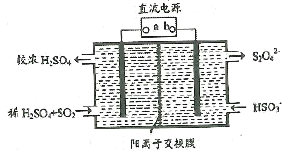
高三化学综合题困难题查看答案及解析
(7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:_______________________;
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g)N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为 。
②下列各项能判断该反应达到平衡状态的是 。
A.容器内压强保持不变
B.速率关系:2v(NO)(正) = v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放人生石灰,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。
高三化学填空题困难题查看答案及解析
(7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为 。
②下列各项能判断该反应达到平衡状态的是 。
A.容器内压强保持不变
B.速率关系:2v(NO)(正) = v (N2)(逆)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。
高三化学填空题困难题查看答案及解析
近年来雾霾天气经常出现,研究雾霾成因和治理是当前环保的重要话题。汽车尾气和燃煤是造成空气污染的原因之一。因此研究氮氧化物的反应机理,对消除和防治环境污染有重要意义。
(1)①对于2NO(g)+2H2(g)=N2(g)+2H2O(g) △H=-665kJ/mol的反应分三步完成:
a:2NO(g)=N2O2(g)(快)
b:N2O2(g)+H2(g)=N2O(g)+H2O(g)(慢)
c:N2O(g)+H2(g)=N2(g)+H2O(g)(快)
决定此总反应速率的是第步的反应___(填序号)。
②已知:H2(g)+CO2(g)=H2O(g)+CO(g) △H=+41kJ/mol
汽车尾气的净化原理主要是用催化剂把NO与CO反应转化为两种对大气无污染的气体,试写出该反应的热化学方程式:___。
(2)升高温度能让绝大多数的化学反应加快反应速率,但是研究发现2NO(g)+O2(g)=2NO2(g) △H<0存在一些特殊现象。现有某化学小组通过实验测得不同温度下该反应速率常数k(代表反应速率的一个常数)的数值如表:
| T(K) | k | T(K) | k | T(K) | k |
| 143 | 1.48×105 | 273 | 1.04×104 | 514 | 3.00×103 |
| 195 | 2.58×104 | 333 | 5.50×103 | 613 | 2.80×103 |
| 254 | 1.30×104 | 414 | 4.00×103 | 663 | 2.50×103 |
由实验数据测到v正与c(O2)的关系如图1所示,当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为___点(填字母),并解析原因:
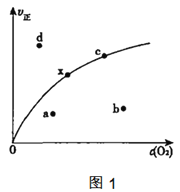
①___
②___
(3)NOx的排放主要来自于汽车尾气,包含NO2和NO,有人得出用活性炭对NOx进行吸收,发生如下反应:
反应a:C(s)+2NO(g)⇌N2(g)+CO2(g) △H=-34.0kJ/mol
反应b:2C(s)+2NO2(g)⇌N2(g)+2CO2(g) △H=-64.2kJ/mol
对于反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如表:
| 时间(min) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0〜10min内,NO的平均反应速率v(NO)=___,当升高反应温度,该反应的平衡常数K___(选填“增大”、“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是___(填字母)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
(4)实验室模拟反应2C(s)+2NO2(g)=N2(g)+2CO2(g) △H=-64.2kJ/mol,在密闭容器中加入一定量的碳和NO2,维持温度是T2℃,如图2为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。
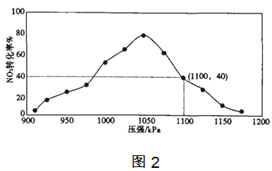
①请从动力学角度分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因___;
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数___(用计算表达式表示,不必化简);已知:气体分压(p分)=气体总压(p总)×体积分数。
高三化学综合题中等难度题查看答案及解析
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
Ⅰ.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:l、4:1时,NO脱除率随温度变化的曲线如图所示。
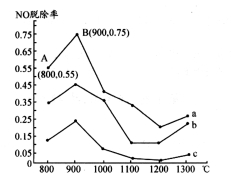
(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为 mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是 ,其理由是
(2)已知在25℃,101kPa时:
N2(g)+3H2(g) === 2NH3(g) △H=-Q1/mol
2H2(g)+O2(g) === 2H2O(1) △H=- Q2kJ/mo1
N2(g) +O2(g) === 2NO(g) △H=+ Q3kJ/mo1
请写出用NH3脱除NO的热化学方程式 。
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下:
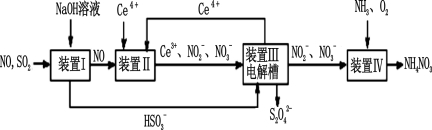
(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为 。
(4)装置Ⅲ制得Na2S2O4的同时还能让Ce4+再生,原理如图所示。其阴极的电极反应式为 : 。
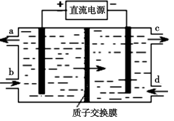
(5)按上述流程处理含有amolSO2、bmolNO的雾霾(b>a),并制取Na2S2O4和NH4NO3。装置Ⅰ中SO2、装置Ⅱ中NO、装置Ⅲ中HSO3-和Ce3+、装置Ⅳ中NO2-全部转化,处理完毕后装置Ⅱ中Ce4+的剩余量与加入量相比没有变化,则至少需向装置Ⅳ中通入标准状况下的O2 L(用含a、b的代数式表示)。
高三化学填空题极难题查看答案及解析