-
胆矾(CuSO4·5H2O)是重要的中药,有解毒、催吐、祛腐的功效。回答下列问题:
(1)实验小组利用某有色金属加工企业的废次材制得含杂质的CuSO4溶液,由该溶液制得胆矾粗产品需进行的实验操作是___________、__________、过滤、洗涤、干燥,过滤操作需要用到的玻璃仪器有烧杯、漏斗、___________。
(2)制得的粗产品中可能含有Fe2(SO4)3、FeCl3杂质。已知:Cu(OH)2能溶于氨水得到深蓝色溶液。选用下列试剂,确定所含杂质。可选用试剂:
蒸馏水、稀硫酸、氨水、 BaCl2溶液、 Ba(NO3)2溶液、KI溶液、AgNO3溶液
实验步骤
实验现象
实验结论
①取一定量样品,加入蒸馏水
固体溶解,得到蓝色澄清溶液
⑤该产品含有_____杂质
②取少量①所得溶液,滴入____至过量,过滤、洗涤
先析出沉淀,后沉淀部分溶解得深蓝色溶液,过滤,滤渣为红褐色
③另取少量①所得溶液,加入足量的______溶液
出现白色沉淀
④向③所得上层清液中加入_____溶液
无明显现象
(3)CuSO4·5H2O的含量通常利用“间接碘量法”测定,步骤如下:
①称取1.250g产品配成100mL溶液。
②取其中25.00mL溶液,加入足量的NaF溶液后,滴加KI溶液至不再产生沉淀。
③用0.1000mol·L-1Na2S2O3标准溶液滴定,平行滴定3次。
已知:Cu2+与F-不反应,Fe3+与F-反应生成FeF63-;I2+2Na2S2O3=2NaI+Na2S4O6
步骤②中,若不加足量的NaF溶液,最终的测量值将___________(填“偏大”、“偏小”、“无影响”)。滴加KI溶液,有白色碘化物沉淀生成,反应的离子方程式为___________;若Na2S2O3标准溶液的平均用量为10.00mL,则胆矾样品纯度为___________%。
高三化学实验题困难题查看答案及解析
-
某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:
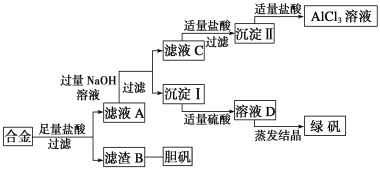
请回答下列问题:
(1)过滤用的玻璃仪器有___________________________________________________。
(2)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:______________________________________________。
写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:_____________________________。
(3)小组成员经过检测,发现制得的绿矾不纯,试分析其主要含有哪些杂质:_______________________________,要想由沉淀Ⅰ最终制得纯度较高的绿矾,应如何改进___________________________________
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为_______________________________。
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱,重新设计方案,也能最终制得三种物质,你认为第二种方案相对于第一种方案________(填“更合理”或“不合理”),理由是________________________。
高三化学工业流程困难题查看答案及解析
-
某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O),其实验方案如下:
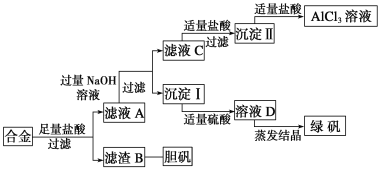
请回答下列问题:
(1)过滤用的玻璃仪器有___________________________________________________。
(2)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:______________________________________________。
写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:_____________________________。
(3)小组成员经过检测,发现制得的绿矾不纯,试分析其主要含有哪些杂质:_______________________________,要想由沉淀Ⅰ最终制得纯度较高的绿矾,应如何改进___________________________________
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为_______________________________。
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱,重新设计方案,也能最终制得三种物质,你认为第二种方案相对于第一种方案________(填“更合理”或“不合理”),理由是________________________。
高三化学工业流程困难题查看答案及解析
-
某学校化学兴趣小组为探究金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的AlCl3溶液和胆矾晶体(CuSO4∙5H2O),其实验方案如下:
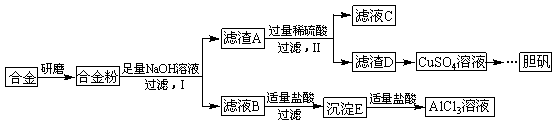
请回答下列问题:
(1)将合金研磨成合金粉的目的是________。
(2)分别写出步骤Ⅰ、Ⅱ中发生反应的化学方程式:
Ⅰ:;
Ⅱ:________。
(3)在滤液B转化为沉淀E的过程中盐酸的用量不易控制,可将加入适量的盐酸改为通入一种气体,该气体的电子式为________,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:________。
(4)该小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣D中加入稀硫酸和H2O2可制得CuSO4,该反应的总化学方程式为________。
高三化学填空题困难题查看答案及解析
-
铝、铁、铜及其合金具有广泛的应用,某学校化学兴趣小组为探究金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的AlCl3溶液和胆矾晶体(CuSO4·5H2O),其实验方案如下:
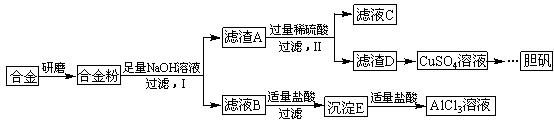
请回答下列问题:
(1)将合金研磨成合金粉的目的是 。
(2)写出步骤I中发生反应的化学方程式: 。
(3)硫酸铜溶液经过“一系列步骤”制得胆矾,此“一系列步骤”依次为 、 和过滤。
(4)在滤液B转化为沉淀E的过程中盐酸的用量不易控制,可将加入适量的盐酸改为通入一种气体,该气体的电子式为 ,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式: 。
(5)该小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣D中加入稀硫酸和H2O2可制得CuSO4,写出该反应的离子方程式: 。
(6)下面两种方法也可以制备硫酸铜:
方法一:2Cu+O2
2CuO,CuO+H2SO4=CuSO4+H2O
方法二:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
假如某工厂欲生产CuSO4,请选择一种方法,并说明理由: 。
高三化学填空题困难题查看答案及解析
-
某实验小组利用Fe2O3、Cu2O的混合物制取较纯净的胆矾(CuSO4·5H2O),实验方案如图所示
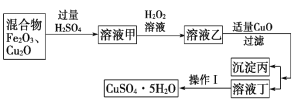
(1)稀硫酸溶解混合物时发生反应的离子方程式为Cu2O+2H+===Cu+Cu2++H2O、_________________________。
(2)加H2O2的目的是_______________,其反应的离子方程式为________________。
(3)溶液乙中加入适量CuO时发生反应的离子方程式为_________________。
(4)操作Ⅰ主要包括________、________、过滤、洗涤、晾干等步骤。
高三化学填空题中等难度题查看答案及解析
-
铜及其化合物在很多领域有重要的用途,如氧化亚铜(Cu2O)可做半导体材料,胆矾 (CuSO4·5H2O)用于杀菌剂,磷酸氧铜[Cu4O(PO4)2]能充当电极的活性物质。请回答下列相关问题。
(1)写出基态Cu+离子的核外电子排布式____________________,与Cu同周期且与Cu原子最外层电子数相等的元素有______________________(填元素符号)。
(2)胆矾和磷酸氧铜中含有的非金属元素,其电负性由大到小的顺序为______________________。
(3)PO43-的VSEPR模型为______________________,中心原子P的杂化类型为 ___________,与其互为等电子体的离子有______________________(写出两种)。
(4)胆矾(CuSO4• 5H2O)的结构示意图如下图,请结合示意图完成下列问题。
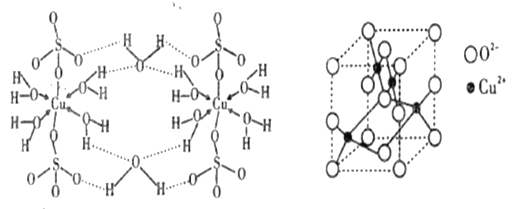
①将胆矾的化学式写成配合物的形式为______________________。
②胆矾中含有的微粒间作用力有______________________(填序号)。
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(5)胆矾在高温条件下会失水、分解生成CuO,加热CuO还会继续分解为Cu2O。
①Cu2O的熔点比Cu2S的__________(填“髙”或“低”),原因是____________________。
②CuO的晶胞结构如上图所示,可确定该晶胞中阴离子的个数为,O2-的配位数是__________。
高三化学综合题中等难度题查看答案及解析
-
CuSO4∙5H2O是铜的重要化合物,有着广泛的应用。CuSO4∙5H2O的实验室制法如下:
Ⅰ.实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀)
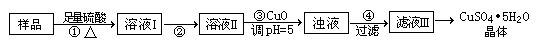
回答下列问题:
⑴用98%的浓硫酸配制溶解所用的4.5 mol∙L-1的稀硫酸,只需________种玻璃仪器
⑵步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是________
发生反应的离子方程式:________
⑶如何证明Fe2+已经充分转化?________
⑷步骤④之后的实验操作是________,所需仪器是铁架台(带铁圈)、
________及抽滤装置。
Ⅱ.实验室用铜粉制备的CuSO4∙5H2O流程图如下:
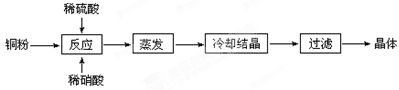
根据题意完成下列填空:
⑴理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为________,
发生反应的离子方程式为________。
⑵实际制得的胆矾晶体中还是含有一些杂质,通常采用法提纯。
⑶实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是________
________。
请在图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
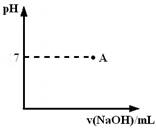
⑷上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是________。
A.醋酸 B.草酸 C.苯甲酸 D.苯酚
高三化学实验题中等难度题查看答案及解析
-
(13分)实验室以含有少量铁的粗铜粉和硫酸与硝酸的混合溶液为原料制备CuSO4·5H2O(胆矾)晶体。设计的工艺流程图如下:
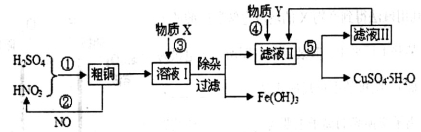
请回答下列问题:
(1)根据反应原理,操作①所需的混酸溶液中硝酸和硫酸的理论配比(物质的量之比)为________。操作②中需要把NO与_____气体混合通入水中,混入该气体的目的是__________________________(用化学方程式表示)。
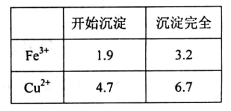
(2)溶液I中存在一定浓度的Fe3+、Cu2+,在该浓度时生成氢氧化物沉淀的pH如下表。操作③中某学生设计物质X为H2O,若加水调整溶液pH,则Fe(OH)3开始沉淀的pH_______1.9(填“<”、“>”或“=”);而实际操作中一般不用此法调节溶液pH,其主要原因是___________________。
(3)操作④中物质Y为_______。查阅资料知CuSO4·5H2O的溶解度曲线如图所示,则操作⑤应采取的措施是蒸发浓缩、______________、过滤、洗涤、干燥等。
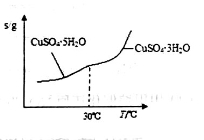
(4)为测定胆矾中结晶水的数目,称取25.0g胆矾品体在坩埚中加热,固体质量随温度升高而变化的曲线如图。
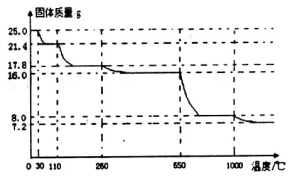
当固体质量为8.0g时,观察到固体完全呈黑色。请列式计算开始称取的胆矾中结晶水的数目。
高三化学填空题困难题查看答案及解析
-
(10分)信息时代产生的大量电子垃圾对环境构成严重威胁。某研究性学习小组将一批废弃的线路板简单处理后,得到含Cu、Fe及少量Au、Pt等金属的混合物,并用如下流程制备胆矾晶体(CuSO4•5H2O):
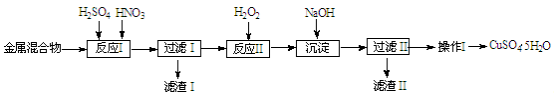
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子
Fe3+
Fe2+
Cu2+
开始沉淀
1.5
6.4
4.2
完全沉淀
3.2
8.9
6.7
(1)滤渣Ⅰ的主要成份是(写化学式)__________。
(2)反应Ⅱ中加入H2O2的作用是___________________。
(3)生成沉淀反应的离子方程式有______________________。
(4)操作Ⅰ的步骤是 、过滤、洗涤、干燥。
(5)测定胆矾晶体纯度的实验步骤如下:
A. 准确称取3.125g胆矾晶体样品配成100mL溶液;
B. 取10.00 mL溶液于带塞锥形瓶中,加适量水稀释,加入过量KI固体,发生反应:2Cu2+ +4Iˉ= 2CuI↓ + I2
C. 继续向上述混合物中,逐滴加入0.1000 mol·L-1Na2S2O3溶液至恰好完全反应,共消耗12. 00mL Na2S2O3溶液:I2+2S2O
= 2Iˉ+S4O
, 则样品中胆矾晶体的质量分数______。
高三化学实验题困难题查看答案及解析