-
由碳棒、铁片和200mL稀H2SO4组成的原电池中,当在碳棒上共放出3.36L(标准状况)气体时,求消耗铁多少克?有多少个电子通过了电线?____________、_______________________________
高二化学填空题中等难度题查看答案及解析
-
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,硫酸恰好用完,则:
(1)产生这些气体消耗的锌的质量是多少?
(2) 通过导线的电子的物质的量是多少?
(3)原稀硫酸的物质的量浓度是多少?
高二化学计算题中等难度题查看答案及解析
-
如图所示由锌片、铜片和稀H2SO4(密度为1.25g·cm-3)组成的原电池,一段时间后,若锌片只发生电化学反应,当在铜片上放出1.68L(标准状况下)气体时,H2SO4恰好消耗一半。则原硫酸溶质的质量分数为( )

A. 0.75% B. 2.94% C. 5.88% D. 11.76%
高二化学单选题中等难度题查看答案及解析
-
由锌片、铜片和200mL稀硫酸组成的原电池如图所示。
(1)原电池的负极反应是___,正极反应是___。
(2)电流的方向是___。

(3)一段时间后,当在铜片上放出1.12L(标准状况下)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗___g锌,___个电子通过了导线,原硫酸的物质的量浓度是__ (设溶液体积不变)。
高二化学填空题简单题查看答案及解析
-
在由铜片、锌片和150 mL稀硫酸组成的原电池中,当在铜片上放出6.72 L(标准状况)的H2时,硫酸恰好用完,则:
(1) 产生这些气体消耗的锌的质量是____g;
(2) 通过导线的电子的物质的量是_____mol;
(3) 该原电池正极的电极反应式为___________________________。
高二化学计算题中等难度题查看答案及解析
-
有一块镁铝合金,其中镁与铝的质量比是8∶9。加入200 mL稀HNO3使其恰好完全溶解,产生NO气体在标准状况下的体积为3.36 L,然后向溶液中再加入NaOH溶液至沉淀质量不再发生变化,过滤、洗涤、干燥、称量。
(1)合金中铝的物质的量为_________,最后所得沉淀的质量为_________。
(2)另取200 mL原稀HNO3和300 mL稀硫酸组成混合液,向其中加铜粉使之充分反应,得到只含一种溶质的溶液,求所加稀硫酸的物质的量浓度。(无解题过程不给分)____________
高二化学计算题中等难度题查看答案及解析
-
将铜片、锌片和250mL稀硫酸组成的原电池,假设锌片只发生电化学腐蚀.当在铜片上放出6.72L(标准状况下)的气体时,H2S04恰好反应完全.
(1)该原电池的负极反应式为______
(2)原稀硫酸的物质的量浓度是______mol•L-1
(3)列式计算锌片减少的质量.高二化学解答题中等难度题查看答案及解析
-
将3.84 g的铜加入100 mL H2SO4和HNO3混合液中,铜全部溶解并放出无色气体。向溶液中加入2.70 g铝粉,充分反应后过滤,得到溶液X、滤渣Y和气体Z,气体Z遇空气不变色,在标准状况下的体积为672 mL。下列说法正确的是
A. 溶解铝粉的质量为0.54 g
B. 滤渣Y中可能只含有Cu
C. 原混合液中的c(H2SO4):c(HNO3)=9:4
D. 若向溶液X中加入100 mL 2.0 mol·L-1氢氧化钠溶液,充分反应,所得沉淀为4.68 g
高二化学单选题中等难度题查看答案及解析
-
将Na2CO3•nH2O和NaHCO3的混合物4.0g溶于水,配制成100mL溶液,向其中加入2.0mol/L盐酸至不再产生气体时,消耗盐酸20.0mL,放出气体0.672L(标准状况).试计算:
(1)原混合物中NaHCO3的质量分数.
(2)Na2CO3•nH2O中n的值.高二化学解答题中等难度题查看答案及解析
-
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积V L。则下列说法正确的是
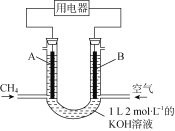
A.OH-由A端移向B端
B.0<V≤22.4 L时,电池总反应的化学方程式为CH4 +2O2 +KOH=KHCO3 +2H2O
C.22.4 L<V≤44.8 L时,负极电极反应为:CH4 +9CO32-+3H2O-8e-=10HCO3-
D.V=33.6 L时,溶液中阴离子浓度大小关系为c(CO32-)>c(HCO3-)>c(OH-)
高二化学单选题困难题查看答案及解析