-
常温下有0.1 mol·L-1五种溶液NaOH、 NH3·H2O、 CH3COOH、HCl、NH4HSO4。
(1)已知CH3COOH溶液的pH=3,其电离度为________,由水电离的c(H+)=_________________________________________。
(2)NH3·H2O溶液和HCl溶液等体积混合后,溶液呈酸性的原因是(离子方程式表示)_________________________________________________________________________。
此时,该混合溶液中的微粒 浓度关系正确的是________(填字母)。
浓度关系正确的是________(填字母)。
A.c(Cl-)>c(H+) >c(NH )>c(OH-)
)>c(OH-)
B .c(Cl-)=c(NH
.c(Cl-)=c(NH )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
C.c(NH )+c(NH3·H2O)=0.1 mol·L-1
)+c(NH3·H2O)=0.1 mol·L-1
D.c(H+) =c(NH3·H2O)+c(OH-)
(3)已知NH3·H2O和NH4Cl等浓度混合时溶液呈碱性,向NH4HSO4溶液中逐滴滴入NaOH溶液至中性时,溶液中各离子浓度的大小关系是________________________________。
-
常温下有四种溶液NaOH、 NH3·H2O、 HCl 、CH3COOH。
(1)相同pH的CH3COOH溶液和HCl溶液加水稀释,其 pH变化情况如图,其中表示HCl溶液的是曲线________,a、b两点中,导电能力更强的是________。
pH变化情况如图,其中表示HCl溶液的是曲线________,a、b两点中,导电能力更强的是________。

(2)NH3·H2O溶液和HCl溶液混合,已知体积V(NH3·H2O)>V(HCl),当溶液中c(NH3·H2O)=c(NH )时,溶液的pH=_______。[已知:Kb(NH3·H2O)=1.77×10-5,lg 1.77=0.25]
)时,溶液的pH=_______。[已知:Kb(NH3·H2O)=1.77×10-5,lg 1.77=0.25]
-
甲、乙、丙、丁、戊五种溶液的溶质分别是HCl、CH3COOH、NaOH、NH3•H2O、Na2CO3中的一种. 常温下如下实验:
①将0.1L pH=9的甲溶液分别与a L 0.001mol/L的乙溶液、b L 0.001mol/L的丁溶液充分反应后溶液呈中性时,a>b;
②浓度均为0.1mol/L的丙和丁溶液等体积混合后,溶液呈酸性;
③0.1mol/L的甲溶液pH小于0.1mol/L的戊溶液pH.
下列判断正确的是( )
A.甲的溶质是NH3•H2O
B.乙的溶质是CH3COOH
C.丙的溶质是NaOH
D.戊的溶质是HCl
-
甲、乙、丙、丁、戊五种溶液的溶质分别是HCl、CH3COOH、NaOH、NH3·H2O、Na2CO3中的一种。 常温下如下实验:①将0.1 L pH=9的甲溶液分别与a L 0.001 mol/L的乙溶液、b L 0.001 mol/L的丁溶液充分反应后溶液呈中性时,a>b;②浓度均为0.1 mol/L的丙和丁溶液等体积混合后,溶液呈酸性;③0.1 mol/L的甲溶液pH小于0.1 mol/L的戊溶液pH。下列判断正确的是
A.甲的溶质是NH3·H2O B.乙的溶质是CH3COOH
C.丙的溶质是NaOH D.戊的溶质是HCl
-
甲、乙、丙、丁、戊五种溶液的溶质分别是HCl、CH3COOH、NaOH、NH3·H2O、Na2CO3中的一种。常温下如下实验:①将0.1 L pH=9的甲溶液分别与a L 0.001 mol/L的乙溶
液、b L 0.001 mol/L的丁溶液充分反应后溶液呈中性时,a>b;②浓度均为0.1 mol/L
的丙和丁溶液等体积混合后,溶液呈酸性;③0.1 mol/L的甲溶液pH小于0.1 mol/L
的戊溶液pH。下列判断正确的是
A.甲的溶质是NH3·H2O B.乙的溶质是CH3COOH
C.丙的溶质是NaOH D.戊的溶质是HCl
-
常温下有0. 1 mol/L的以下几种溶液,①H2SO4溶液②NaHSO4溶液③CH3COOH溶液④HCl溶液⑤HCN溶液⑥NH3·H2O,其中如下几种溶液的电离度(即已经电离的占原来总的百分数)如下表(已知H2SO4的第一步电离是完全的),回答下面问题:
| ①H2SO4溶液HSO4- | ②NaHSO4溶液HSO4- | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
(1)常温下,pH相同的表格中几种溶液,其物质的量浓度由大到小的顺序是(填序号,下同)_________
(2)常温下,将足量的锌粉投人等体积pH=1的表格中几种溶液中,产生H2的体积(同温
同压下)由大到小的顺序是__________
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3 COOH应选用_________作指示剂,若终点时溶液pH = a,则由水电离的。c(H+)为_________。
(4)在25℃时,将b mol·L-1的KCN溶液与0. O1 mol·L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH = 7,则KCN溶液的物质的量浓度b_________0.01 mol·L-1填“>”、“<”或“=”);用含b的代数式表示HCN的电离常数Ka=________
-
常温下有浓度均为0.1 mol·L-1的四种溶液:①Na2CO3、②NaHCO3、③HCl、④NH3·H2O。
(1)有人称溶液①是油污的“清道夫”,原因是 (用离子方程式解释)。
(2)溶液②中,c(CO32-)+c(HCO3-)+ c(H2CO3)=__________mol·L-1。
(3)将10 mL溶液③加水稀释至100 mL,则此时溶液中由水电离出的c( H+)=______。
(4)取④的溶液5mL,向其中加入含0.1molNH4NO3的溶液后呈中性,则NH3·H2O电离平衡常数Kb= 。
-
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5mol·L-1。向20mL浓度均为0.1mol·L-1 NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的电导率与加入CH3COOH溶液的体积(V)关系如图所示。下列说法错误的是
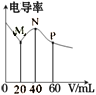
A. M点:c(Na+)>c(CH3COO-)>c(NH3·H2O)>c(NH4+)
B. 溶液呈中性的点处于N、P之间
C. 已知1g3≈0.5,P点的pH=5
D. P点:3[c(CH3 COO-)+ c(CH3COOH)]=2[ c(Na+)+c(NH4+)+c(NH3·H2O)]
-
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是
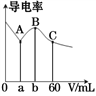
A. a=20,b=40,且溶液呈中性处于A、B两点之间
B. B点溶液中:c(CH3COO-)>c(Na+)>c(NH )
)
C. 已知lg3≈0.5,则C点的pH≈5
D. A、B、C三点中,B点溶液中水的电离程度最大
-
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是
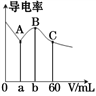
A.a=20,b=40,且溶液呈中性处于A、B两点之间
B.B点溶液中:c(CH3COO-)>c(Na+)>c(NH )
)
C.已知lg3≈0.5,则C点的pH≈5
D.A、B、C三点中,B点溶液中水的电离程度最大
浓度关系正确的是________(填字母)。
)>c(OH-)
.c(Cl-)=c(NH
)>c(OH-)=c(H+)
)+c(NH3·H2O)=0.1 mol·L-1



