-
在 100℃时,将 0.40 mol NO2 气体充入 2 L 的密闭容器中,发生如下反应:2NO2(g) N2O4(g) ∆H < 0。监测反应获得如下数据:
N2O4(g) ∆H < 0。监测反应获得如下数据:
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法正确的是
A.0~20 s 内,v(NO2) = 0.005 mol·L-1.s-1
B.若上述反应在 120℃时进行,则反应至 80 s 时,n(N2O4) < 0.08 mol
C.若仅将起始时充入 NO2 的量增至 0.80 mol,达平衡时 NO2 转化率将减少
D.59 s 时,c(NO2)一定大于 0.12 mol·L-1
-
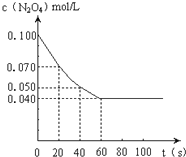
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4⇌2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)计算在20至40秒时间内,NO2的平均生成速率为________mol•L-1•S-1.
(2)该反应的化学平衡常数表达式为________.
-
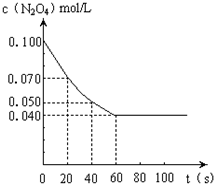
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4
 2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)计算在20至40秒时间内,NO2的平均生成速率为________mol•L-1•S-1.
(2)该反应的化学平衡常数表达式为K=________.
(3)下表是不同温度下测定得到的该反应的化学平衡常数.
| T/K | 323 | 373 |
| K值 | 0.022 | 0.36 |
据此可推测该反应(生成NO2)是________反应(选填“吸热”或“放热”).
-
将0.1mol N2O4置于1L密闭烧瓶中,然后将烧瓶放入100℃的恒温槽,烧瓶内的气体逐渐变为红棕色:N2O4(g)(无色)═2NO2(g)(红棕色)下列结论不能说明上述反应在该条件下已经达到平衡状态的是( )
A.烧瓶内气体的颜色不变,不再加深
B.N2O4的消耗速率与NO2的生成速率之比为1:2
C.NO2的生成速率与NO2的消耗速率相等
D.NO2的物质的量浓度不变
-
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)⇌N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
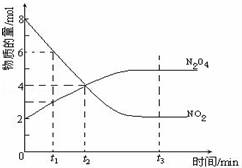
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: mol•L﹣1•s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率.
-
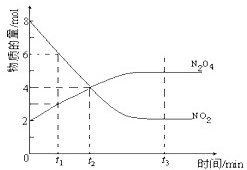
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)⇌N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:________
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率:________mol•L-1•s-1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:________
(4)t1时,正反应速率________(填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向________ 移动 (填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色________(填“变深”、“变浅”或“不变”)
-
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)⇌N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
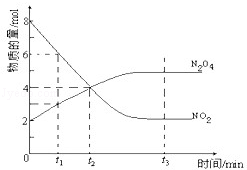
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: mol•L﹣1•s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向 移动(填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色 (填“变深”、“变浅”或“不变”)
-
8分)一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8 mol NO2,发生如下反应:2NO2(红棕色) N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:________
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: ________mol·L-1·s-1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 ________ (填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向 移动
(填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色 ________ ________
(填“变深”、“变浅”或“不变”)
-
一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g) 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2)=____________mol·L-1·s-1。
(2)升高温度时,气体颜色加深,则正反应是____________(填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为_____________。
(4)相同温度下,若开始时向该容器中充入的是0.20 molN2O4和0.40molNO2,则达到平衡后,c(NO2)=_____________。
-
80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为 mol/(L.s)
②计算在80℃时该反应的N2O4的转化率= 此温度下
③反应进行至110s后将反应混合物的温度降低,混合气体的颜色 ;如果此时加入NO2,则此时容器内颜色 (填“变浅”、“变深”或“不变”)
④要增大该反应NO2 的体积分数,可采取的措施有(填序号)
A.增大N2O4的起始浓度 B.通入N2气体
C.使用高效催化剂 D.升高温度
N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:

N2O4(无色)达平衡的是_________




